课 程 进 度 表
课程名称 分析化学实验 课程代码 070183 上课班级号 年级2012级
学生所在院(系)化学与环境科学学院 专业/班级 化学121、122 20##-2014学年第一学期
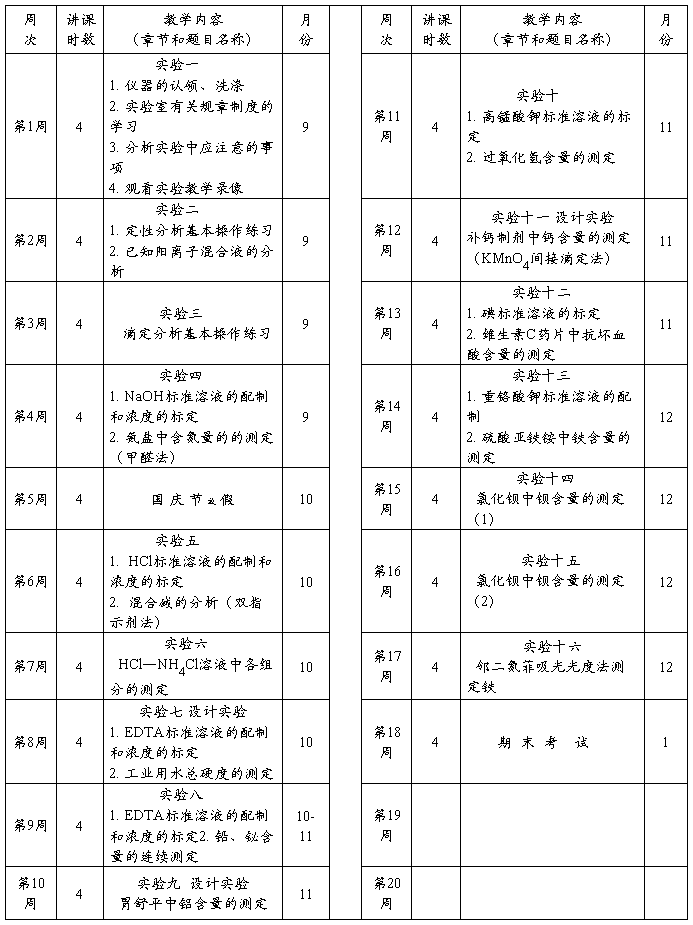
授课教师签字:陈明凯 霍彩霞 系主任签字:
20##年7月 4日 年 月 日
说明:1、上课班级号为“课程代码-上课班序号”,可由教务网络管理系统查得。
2、本表一式四份,一份向上课班级公布,两份报院(系)办公室,一份教师自留。
3、院(系)于第三周将本院、系进度表汇总上报教务处一份。
工业用水的总硬度的测定
实验目的 1.了解配位滴定法基本原理和方法。 2.了解水的硬度的概念及其表示方法。 实验原理 含有钙、镁离子的水叫硬水。测定水的总硬度就是测定水中钙、镁离子的总含量,可用EDTA配位滴定法测定: 滴定前: M + EBT M-EBT (红色) 主反应: M + Y MY 终点时: M-EBT + Y MY + EBT (红色) (蓝色) 滴定至溶液由红色变为蓝色时,即为终点。 滴定时,Fe3+、Al3+等干扰离子可用三乙醇胺予以掩蔽;Cu2+、Pb2+、Zn2+等重属离子,可用KCN、Na2S或巯基乙酸予以掩蔽。 水的硬度有多种表示方法,本实验要求以每升水中所含Ca2+、Mg2+总量(折算成CaO的质量)表示,单位mg·L-1。 器材和药品 1.器材 天平(0.1g、0.1mg),容量瓶(100mL),移液管(20mL),酸式滴定管(50mL),锥形瓶(250mL)等。 2.药品 HC1(1∶1),乙二胺四乙酸二钠(Na2H2Y·2H2O,A.R.),碱式碳酸镁[Mg(OH)2·4MgCO3·6H2O,基准试剂],NH3-NH4Cl缓冲溶液(pH=10.0),三乙醇胺(1∶1),铬黑T指示剂(0.2%氨性乙醇溶液)等。 实验方法 一、Mg2+标准溶液的配制(约0.02mol·L-1) 准确称取碱式碳酸镁基准试剂0.2~0.25g,置于100mL烧杯中,用少量水润湿,盖上表面皿,慢慢滴加1∶1 HC1使其溶解(约需3~4mL)。加少量水将它稀释,定量地转移至100mL容量瓶中,用水稀释至刻度,摇匀。 其浓度计算: 二、EDTA标准溶液的配制与标定 1.EDTA标准溶液的配制(约0.02mol·L-1) 称取2.0g乙二胺四乙酸二钠(Na2H2Y·2H2O)溶于250mL蒸馏水中,转入聚乙烯塑料瓶中保存。 2.EDTA标准溶液浓度的标定 用20mL移液管移取Mg2+标准溶液于250mL锥形瓶中,加入10mL氨性缓冲溶液和3~4滴EBT指示剂,用0.02mol·L-1EDTA标准溶液滴定,至溶液由紫红色变为蓝色即为终点。平行标定3次。 EDTA浓度计算: ,取三次测定的平均值。 三、水的总硬度测定 用20mL移液管移取水样于250mL锥形瓶中,加氨性缓冲溶液6mL,1∶1三乙醇胺溶液3mL,EBT指示剂3~4滴,用EDTA标准溶液滴定,至溶液由紫红色变为蓝色即为终点。平行测定3次。 水的总硬度计算: ,取三次测定的平均值。
第二篇:进度表:化工分析化学实验-20xx-12-1-48学时1
广东工业大学实验(上机)教学进度表
(20##—20##学年度第一学期)
专业班级 化学工程与工艺10(4) 学生人数 48 实验(上机)学时数 48
课程名称 分析化学实验 共1页第 1 页
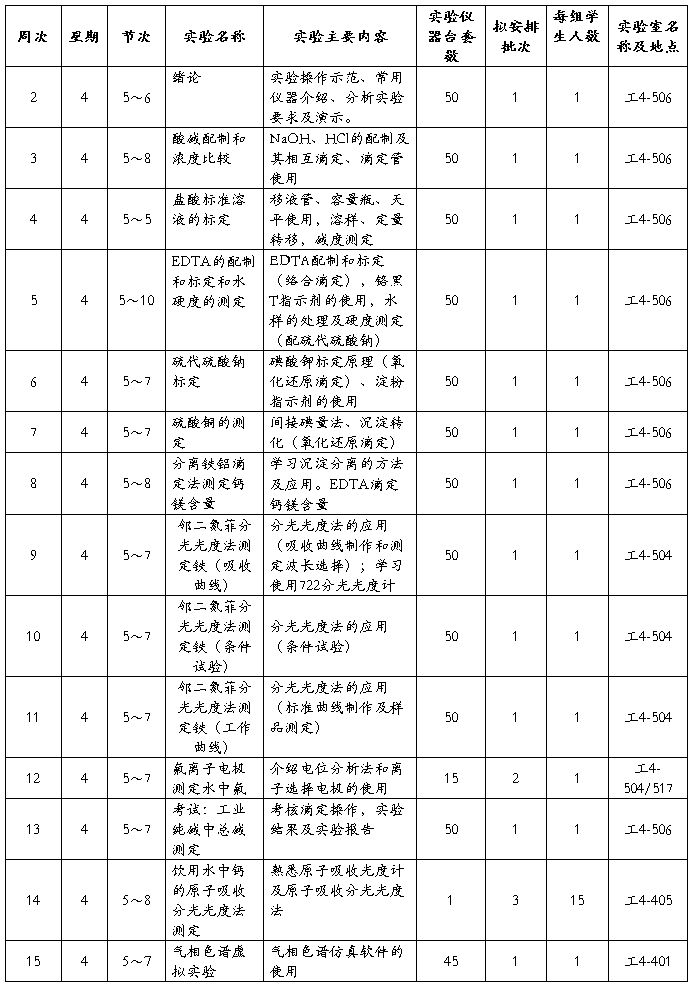
说明:
1、本表由承担实验教学任务的教师到实验室落实实验安排后填写,编写时按《广东工业大学本科教学进度表的编制及管理规定》要求,经基层教学单位教学负责人及学院教学主管审核批准执行。
2、本表须在每学期开学后第1周内送交基层教学单位审核,第2周内学院审核,第3周内交学生所在学院2份和发给学生班1份。
教师签名: 填写日期: 2011 年 8 月 31 日
基层教学单位教学负责人签章: 审核日期: 2011 年 8 月 31 日
学院教学主管签章: 审核日期: 年 月 日
