实验二十一 可溶性总糖的测定(蒽酮比色法)
一、目的
掌握蒽酮法测定可溶性糖含量的原理和方法。
二、原理
强酸可使糖类脱水生成糠醛,生成的糠醛或羟甲基糖醛与蒽酮脱水缩合,形成糠醛的衍生物,呈蓝绿色,该物质在 620 nm 处有最大吸收 . 在 10 -100ug 范围内其颜色的深浅与可溶性糖含量成正比。
这一方法有很高的灵敏度,糖含量在 30ug 左右就能进行测定,所以可做为微量测糖之用。一般样品少的情况下,采用这一方法比较合适。
三、仪器、试剂和材料
1 .仪器
( 1) 分光光度计
(2 )电子顶载天平
(3 )三角瓶: 50m1 X 1
( 4 )大试管: 9 支
( 5) 试管架,试管夹
( 6 )漏斗,漏斗架
( 7 )容量瓶: 50rnl X 2
( 8 )刻度吸管: 1m1X3 , 2m1X1 , 5mlX1
( 9 )水浴锅
2 .试剂
( 1) 葡萄糖标准液: l00ug/ml
(2 )浓硫酸
(3) 蒽酮试剂 :0.2g 蒽酮溶于 100 ml 浓 H2SO4 中当日配制使用。
3 .材料
小麦分蘖节。
四、操作步骤
1 .葡萄糖标准曲线的制作
取 7 支大试管,按下表数据配制一系列不同浓度的葡萄糖溶液:
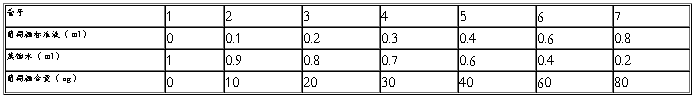
在每支试管中立即加入蒽酮试剂 4.0m1 ,迅速浸于冰水浴中冷却,各管加完后一起浸于沸水浴中,管口加盖玻璃球,以防蒸发。自水浴重新煮沸起,准确煮沸 l0min 取出,用流水冷却,室温放置 10min ,在 620 nm 波长下比色。以标准葡萄糖含量( ug) 作横坐标,以吸光值作纵坐标,作出标准曲线。
2 .植物样品中可溶性糖的提取
将小麦分蘖节剪碎至 2mm 以下,准确称取 Ig, 放入 50m1 三角瓶中,加沸水 25m1 ,在水浴中加盖煮沸 10min ,冷却后过滤,滤液收集在 50m1 容量瓶中,定容至刻度。吸取提取液 2m1 ,置另一 50m1 容量瓶中,以蒸馏水稀释定容,摇匀测定。
3 .测定
吸取 lml 已稀释的提取液于大试管中,加入 4.Oml 蒽酮试剂,以下操作同标准曲线制作。比色波长 620nm ,记录吸光度,在标准曲线上查出葡萄糖的含量( ug )。
查表所得糖含量( ug )×稀释倍数
五、结果处理

六、注意事项
1 .该显色反应非常灵敏,溶液中切勿混入纸屑及尘埃。
2 . H 2 SO 4 要用高纯度的。
3. 不同糖类与蒽酮的显色有差异,稳定性也不同。加热、比色时间应严格掌握。
七、思考题
1 .用水提取的糖类有哪些?
2 .制作标准曲线时应注意哪些问题?
第二篇:蒽酮比色法测糖 .doc
蒽酮比色法测糖
一 目的
掌握蒽酮比色法测糖的原理和方法
二 原理
蒽酮比色法是一个快速而简便的定糖方法。蒽酮可以与游离的已糖或多糖中的已糖基、戊糖 基及已糖醛酸起反应,反应后溶液呈蓝绿色,在620nm处有最大吸收。 本法多用于测定糖原的含量,也可用于测定葡萄糖的含量。
三 实验器材及试剂
马铃薯干粉、 可调试移液器或移液管 、可见分光光度计(723型)、电子分析天平 、水浴锅 、电炉子
蒽酮试剂:取2g蒽酮溶解到80%H2SO4中,以80%H2SO4定容到1000ml,当日配制使用。
标准葡萄糖溶液(0.1mg/ml):100mg葡萄糖溶解到蒸馏水中,定容到1000ml备用。
葡萄糖标准溶液:称取已在80℃烘箱中烘至恒重的葡萄糖100mg,配制成500ml溶液,即得每ml含糖为200μg的标准溶液。
蒽酮试剂:称取1g经过纯化的蒽酮,溶解于1000ml稀硫酸中即得。硫酸溶液由760ml浓硫酸(比重1.84)稀释成1000ml而成。
2g/L蒽酮试剂:溶解2g蒽酮于1L浓硫酸(98%的浓硫酸)中,当日配制使用。
四、操作
1.可溶性糖的提取
称取重约5g的新鲜植物叶子,于研钵中乙醚少许,仔细研磨成均匀的浆状物,倒入烧杯中,用70℃热水洗涤研钵,洗液并入烧杯中,再加蒸镏水30─40ml。将烧杯放在水浴锅中加热,保持温度70─80℃约半小时,冷却后1滴1滴地加入饱和中性醋酸铅,以除去蛋白质,直至加入醋酸铅时不再形成白色沉淀为止。然后将此混合物连同残渣一并洗入100ml容量瓶中,加水至刻度,充分振荡。以干燥漏斗将滤液过滤于一干燥的三角烧瓶中,瓶中事先放有少量(约0.2─0.4g)草酸钠粉末,以除去滤液中过量的醋酸铅,使生成草酸铅沉淀,再行过滤,所得的透明滤液即为可溶性糖提取液。
2.显色及比色
吸取上述糖提取液1ml,放入一干洁的试管中,加蒽酮试剂5ml混合之,于沸水浴中煮沸10分钟,取出冷却,然后于分光光度计上进行测定,波长为625nm,测得吸光度。从标准曲线上查得滤液中的糖含量(或经直线回归公式计算),然后再行计算样品中含糖百分数。
3.绘制标准曲线
准确称取0.1g葡萄糖(分析纯),溶解并用蒸馏水定容至100ml后,分别取出1ml,2ml,3ml,4ml,5ml分别加入到50的容量瓶中,并用蒸馏水定容到50ml,配成浓度分别为20ug/ml,40ug/ml,60ug/ml,80ug/ml,100ug/ml,各取1ml于试管中,再加入3ml的蒽酮试剂,迅速浸入冰水中冷却,待几支试管均匀加完后,一起浸入100℃恒温水浴箱中,为防止水分蒸发,应在试管口上加盖一个玻璃球或者加一个塞子,自温度重新升至100℃起计时,准确保温10min后取出,用流动水冷却,然后,于室温中平衡片刻(约10min左右),在分光光度计上,波长620nm处,用0.5cm厚度的比色杯,以空白管做对照空白(此处的空白是指不加葡萄糖的蒽酮试剂,其他反应条件都一致),进行比色。
既得标准曲线。
如下表格
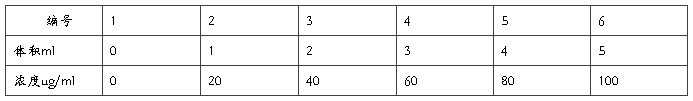
2.样品含量的测定
样品液的制作:
精确称取马铃薯干粉0.1g置于锥形瓶中—→加入30ml沸水—→沸水浴30min(不时摇动)—→取出, 3000rpm离心10min(或过滤)—→反复洗涤残渣2次—→合并滤液—→冷却至室温—→定容到50ml的锥形瓶中—→再从中取出1ml,再定容到10ml的容量瓶中
样品液的测定:
(1)取4支试管,按照表2加样(加蒽酮时需要冰水浴5min冷却)
(2)加样冷却完成后置沸水中煮沸10min,取出流水冷却放置10min,620nm处比色测量各管OD值。
(3)以1号试管作为调零管,2、3、4号管的OD值取平均后从标准曲线上查出样品液相应的含糖量。
3.结果计算:
C×V
w = ————×100%
m,
式中w:糖的质量分数(%)
C:从标准曲线中查出的糖质量分数(mg/ml)
V:样品稀释后的体积(ml)
m:样品的质量(ml)
注意事项:
1.一定要注意温度要控制在100℃
2.从100℃开始准确计时10min,然后迅速冷却,于室温中平衡10min.
3.蒽酮要注意避光保存。配置好的蒽酮试剂也应注意避光,当天配制好的当天使用。
4.试管要保证干燥清洁,无残留水滴。
