实验三 平板菌落计数
一、目的要求
学习 菌种的 平板菌落计数的基本原理和方法。
二、基本原理
平板菌落计数法是将待测样品经适当稀释之后,其中的微生物充分分散成单个细胞,取一定量的稀释样液接种到平板上,经过培养,由每个单细胞生长繁殖而形成肉眼可见的菌落,即一个单菌落应代表原样品中的一个单细胞。统计菌落数,根据其稀释倍数和取样接种量即可换算出样品中的含菌数。但是,由于待测样品往往不易完全分散成单个细胞,所以,长成的一个单菌落也可能来自样品中的2~3或更多个细胞。因此平板菌落计数的结果往往偏低,为了清楚地阐述平板菌落计数的结果,现在已倾向使用菌落形成单位(colony-forming units,cfu)而不以绝对菌落数来表示样品的活菌含量。
平板菌落计数法虽然操作较繁,结果需要培养一段时间才能取得,而且测定结果易受多种因素的影响,但是该计数方法的最大优点是可以获得活菌的信息,所以被广泛用于生物制品检验(如活菌制剂),以及食品、饮料和水(包括水源水)等的含菌指数或污染程度的检测。
三、器材
1 . 菌种:大肠杆菌菌悬液。
2 . 培养基:LB培养基。
3 . 仪器或其他用具: 1ml 无菌吸管,无菌平皿,盛有 4.5ml 无菌水的试管,试管架,恒温培养箱等。
四、操作步骤
1 . 编号
取无菌平皿 9 套,分别用记号笔标明 10-4 、 10-5 、 10-6 (稀释度)各 3 套,另取 6 支盛有 4.5ml 无菌水的试管,依次标是 10-1 、 10-2 、 10-3 、 10-4 、 10-5 、
10-6 。
2 . 稀释
用 1ml 无菌吸管吸取 1ml 已充分混匀的大肠杆菌菌悬液(待测样品),精确地放 0.5ml 至 10-1 的试管中,此即为 10 倍稀释。将多余的菌液放回原菌液中。
将 10-1 试管置试管振荡器上振荡,使菌液充分混匀。另取一支 1ml 吸管插入 10-1 试管中来回吹吸菌悬液三次,进一步将菌体分散、混匀。吹吸菌液时不要太猛太快,吸时吸管伸入管底,吹时离开液面,以免将吸管中的过滤棉花浸湿或使试管内液体外溢。用此吸管吸取 10-1 菌液 1ml ,精确地放 0.5ml 至 10-2 试管中,此即为 100 倍稀释。······其余依次类推。
放菌液时吸管不要碰到液面,即每一支吸管只能接触一个稀释度的菌悬液,否则稀释不精确,结果误差较大。
3 . 倒平板法:1)取样。用三支 1ml 无菌吸管分别吸取 10-4 、10-5 和 10-6 的稀释菌悬液各 1ml ,对号放入编好号的无菌平皿中,每个平皿放 0.2ml 。 不要用 1ml 吸管每次只靠吸管尖部吸 0.2ml 稀释菌液放入平皿中,这样容易加大同一稀释度几个重复平板间的操作误差。 2) 倒平板。尽快向上述盛有不同稀释度菌液的平皿中倒入融化后冷却至 45 ℃左右的LB培养基约 15 毫升 / 平皿,置水平位置迅速旋动平皿,使培养基与菌液混合均匀,而又不使培养基荡出平皿或溅到平皿盖上。 由于细菌易吸附到玻璃器皿表面,所以菌液加入到培养皿后,应尽快倒入融化并已冷却至 45 ℃左右的培养基,立即摇匀,否则细菌将不易分散或长成的菌落连在一起,影响计数。 3)待培养基凝固后,将平板倒置于 37 ℃恒温培养基中培养。
4.涂布法:涂抹平板计数法与倒平板法基本相同,所不同的是先将培养基熔化后趁热倒入无菌平板中,待凝固后编号,然后用无菌吸管吸取0.1ml菌液对号接种在不同稀释度编号的琼脂平板上(每个编号设三个重复)。再用无菌刮铲将菌液在平板上涂抹均匀(图22-3),每个稀释度用一个灭菌刮铲,更换稀释度时需将刮铲灼烧灭菌。在由低浓度向高浓度涂抹时,也可以不更换刮铲。将涂抹好的平板平放于桌上20—30min,使菌液渗透入培养基内,然后将平板倒转,保温培养,至长出菌落后即可计数。
5 . 计数
培养 48h 后,取出培养平板,算出同一稀释度三个平板上的菌落平均数,并按下列公式进行计算:
每毫升中菌落形成单位( cfu ) = 同一稀释度三次重复的平均菌落数×稀释倍数× 5
一般选择每个平板上长有 30~300 个菌落的稀释度计算每毫升的含菌量较为合适,同一稀释度的三个重复对照的菌落数不应相差很大,否则表示试验不精确。实际工作中同一稀释度重复三个对照平板不能少于三个,这样便于数据统计,减少误差。由 10-4 、 10-5 和 10-6 三个稀释度计算出的每毫升菌液中菌落形成单位数也不应相差太大。
平板菌落计数法,所选择倒平板的稀释度是很重要的,一般三个连续稀释度中的第二个稀释度倒平板培养后,所出现的平均菌落数在 50 个左右为好,否则要适当增加或减少稀释度加以调整。
五、实验结果
将培养后菌落计数结果填入下表:
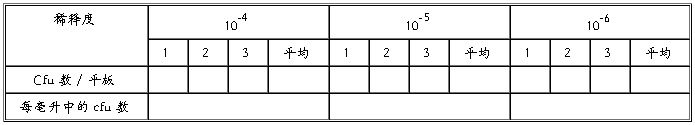
六、 思考题
( 1 )为什么融化后的培养基要冷却至 45 ℃左右才能倒平板?
( 2 )要使平板菌落计数准确,需要掌握哪几个关键?为什么?
( 3 )试比较平板菌落计数法和显微镜下直接计数法的优缺点及应用。
( 4 )当你的平板上长出的菌落不是均匀分散的而是集中在一起时,你认为问题出在哪里?
( 5 )用倒平板法和涂布法计数,其平板上长出的菌落有何不同?为什么要培养较长时间( 48h )后观察结果?
第二篇:微生物平板菌落计数法具体实验步骤
微生物平板菌落计数法具体实验步骤
20##-4-3 11:17
提问者:下雪的下雪 |浏览次数:1760次
手头现在没有实验课本,故求微生物平板菌落计数法的具体实验步骤!详细的,包括稀释倍数及取样量!
20##-4-3 14:32
最佳答案
一、目的要求
学习平板菌落计数的基本原理和方法。
二、基本原理
平板菌落计数法是根据微生物在固体培养基上所形成的一个菌落是由一个单细胞繁殖而成的现象进行的,也就是说一个菌落即代表一个单细胞。计数时,先将待测样品作一系列稀释,再取一定量的稀释菌液接种到培养皿中,使其均匀分布于平皿中的培养基内,经培养后,由单个细胞生长繁殖形成菌落,统计菌落数目,即可换算出样品中的含菌数。
这种计数法的优点是能测出样品中的活菌数。此法常用于某些成品检定(如杀虫菌剂),生物制品检定以及食品、水源的污染程度的检定等。但平板菌落计数法的手续较繁,而且测定值常受各种因素的影响。
三、器材
大肠杆菌悬液,牛肉膏蛋白胨培养基, 1ml无菌吸管,无菌平皿,盛有4. 5 ml无菌水的试管,试管架和记号笔等。
四、操作步骤
1.编号:
取无菌平皿 9套,分别用记号笔标明10-4、10-5、10-6各3套。另取6支盛有4.5ml无菌水的试管,排列于试管架上,依次标明10-1、10-2、10-3、10-4、10-5、10-6。
2.稀释
用1ml无菌吸管精确地吸取0.5ml大肠杆菌悬液放入10-1的试管中,注意吸管尖端不要碰到液面,以免吹出时,管内液体外溢。然后仍用此吸管将管内悬液来回吸吹三次,吸时伸入管底,吹时离开水面,使其混合均匀。另取一支吸管自10-1试管吸0.5ml放入10-2试管中,吸吹三次,……其余依次类推。整个稀释过程如图Ⅷ-3。
3.取样
用3支1ml无菌吸管分别精确地吸取10-4、10-5、10-6的稀释菌液0.2ml,对号放入编好号的无菌培养皿中。
4.倒平板
于上述盛有不同稀释度菌液的培养皿中,倒入溶化后冷却至45℃左右的肉膏蛋白胨琼脂培养基约10—15ml,置水平位置,迅速旋动混匀,待凝固后,倒置于37℃温室中培养。
5.计数
培养24小时后,取出培养皿,算出同一稀释度三个平皿上的菌落平均数,并按下列公式进行计算:
每毫升中总活菌数=同一稀释度三次重复的菌落平均数×稀释倍数×5
一般选择每个平板上长有30—300个菌落的稀释度计算每毫升的菌数最为合适。同一稀释度的三个重复的菌数不能相差很悬殊。由10-4、10-5、10-6三个稀释度计算出的每毫升菌液中总活菌数也不能相差悬殊,如相差较大,表示试验不精确。
平板菌落计数法,所选择倒平板的稀释度是很重要的,一般以三个稀释度中的第二稀释度倒平板所出现的平均菌落数在50个左右为最好。
平板菌蓓计数法的操作除上述的以外,还可用涂布平板的方法进行。二者操作基本相同,所不同的是涂布平板法是先将牛肉膏蛋白胨琼脂培养基溶化后倒平板,待凝固后编号,并于 37℃温室中烘烤30分钟左右,使其干燥,然后用无菌吸管吸取 0.2ml菌液对号接种于不同稀释度编号的培养皿中的培养基上,再用无菌玻璃刮棒将菌液在平板上涂布均匀,平放于实验台上20—30分钟,使菌液渗透入培养基内,然后再倒置于37℃的温室中培养。
五、实验报告
1.结果
将计数结果填入下表。
2.思考题
(1)为什么溶化后的培养基要冷却至45℃左右才能倒平板?
(2)要使平板菌落计数准确,需要掌握哪几个关键?为什么?
(3)同一种菌液用血球计数板和平板菌落计数法同时计数,所得结果是否一样?为什么?
(4)试比较平板菌落计数法和显微镜下直接计数法的优缺点
用倒平板法和涂布计数法,其平板上长出的菌落有何不同?为什么要培养较长时间(48h)后观察结果?
20##-4-19 18:06
提问者:lakersbao |悬赏分:20|浏览次数:1308次
如题,谢谢
20##-4-19 19:10
最佳答案
涂布法:(培养基时固态的)适用于好氧微生物的菌落观察。 涂布法使用较多,但有时不均匀,菌落一般在表面。
倒平板法:(培养基一般温度较高,是液态的)适用于厌氧,兼性厌氧的微生物, 稀释倒平板法操作相对麻烦,不适合好氧和对热敏感的细菌培养 。
培养较长时间(48h)后,菌落特征才明显。
