
物 理 化 学 实 验 报 告

实 验 名 称: 氨基甲酸铵分解反应标准平衡常数的测定
学 院: 化学工程学院
专 业: 化学工程与工艺
班 级: 化工12-4班
姓 名: 王佳琦
学 号: 12402010411
指 导 教 师: 付志强/赵力维
日 期: 2014年03月15日
一、 实验目的
1. 掌握测定平衡常数的一种方法;
2. 用等压法测定氨基甲酸氨的分解压力并计算分解反应的有关热力学常数。
二、 实验原理
氨基甲酸铵(NH2COONH4)是白色固体,是合成尿素的中间产物,很不稳定,NH2COONH4的分解反应式为:NH2COONH4=== 2NH3 +CO2
+CO2
该反应为复相反应,该反应正逆向都容易进行,在封闭体系中很容易达到平衡,其标准平衡常数可近似表示为:
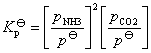 (1)
(1)
式中,PNH 3、PCO 2分别表示反应温度下NH3和CO2平衡时的分压; py为标准压。体系总压: p=pNH 3+pCO
从化学反应计量方程式可知:
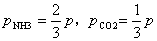 (2)
(2)
将式(2)代入式(1)得:
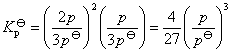 (3)
(3)
因此可知,当体系达平衡后,测定其总压力p,即可计算出平衡常数Kpy
温度对平衡常数的影响一般都很明显,其定量关系为:
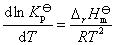 (4)
(4)
式中,T为热力学温度;ΔrH? m为标准反应热效应。氨基甲酸铵分解反应是一个热效应很大的吸热反应,温度对平衡常数的影响比较灵敏。当温度在不大的范围内变化时,ΔrH? m可视为与温度无关的常数,由(4)式积分得:
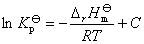 (C为积分常数) (5)
(C为积分常数) (5)
若以lnK? p对1/T作图,应为一直线,其斜率为-ΔrH? m/R。由此可求出ΔrH? m。在一个小的温度区间内,也可用此式计算出此温度区间的平均ΔrH? m。
并按下式计算T温度下反应的标准吉布斯自由能变化ΔrG? m,
ΔrG? m=-RT ln K? p (6)
利用实验温度范围内的平均等压热效应ΔrH? m及等温下的自由能变ΔrG? m,可近似地计算出该温度下的标准熵变ΔrS? m
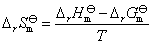 (7)
(7)
综上所述:通过测定一定温度范围内某温度的氨基甲酸铵的分解压(平衡总压),就可以利用上述公式分别求出 K? p,ΔrH? m,ΔrG? m(T),ΔrS? m(T)。
三、实验仪器、试剂
仪器:循环水泵,低真空数字侧压仪,等压计,恒温槽一套,样品管。
药品:氨基甲酸铵,液体石蜡。
四、实验步骤
1. 由特制的小漏斗将氨基甲酸铵粉末小心装入干燥的球状样品管中,与已装好液体石蜡的等压计连好。
2. 开动循环水泵,旋转活塞10与体系相通,旋转活塞11与减压瓶2相通,旋转活塞12至三个方向都通,此时观察到的测压仪数字应不断减小,至低真空测压仪示数为-90kPa以下时,关闭活塞11,检查体系的气密性。
3. 恒温槽中加水至没过样品管和等压计,调节恒温槽水温为25℃。
4. 旋转活塞11,抽吸大约1min,把样品管中的空气抽走,然后关闭活塞11。慢慢旋转活塞13,缓慢放入空气进入体系,使U型等压计液面水平。若3min内保持液面水平不变,记下低真空测压仪的读数,即为氨基甲酸铵分解的平衡压力。然后关闭活塞13,再重复一次,如果二次结果相差在0.2kPa之内,则可改变温度,继续进行实验;若二次结果偏差较大,说明第一次空气没抽净,应再重复一次。若平衡保持不住,可检查是否有漏气的地方。
5. 用同样的方法测25℃、30℃、35℃、40℃、45℃的分解压力。
6. 实验完成后,关闭活塞13,使活塞12与样品管断开,以保护剩余的氨基甲酸铵。将测压仪的NH3和CO2抽净,关闭活塞11,使活塞10放空后方可关泵。
五、数据记录与处理
室温:21.2℃大气压(实验前):101.64kPa大气压(实验后):101.55kPa
大气压(平均值):101.60kPa
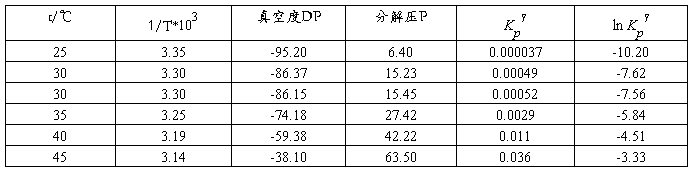
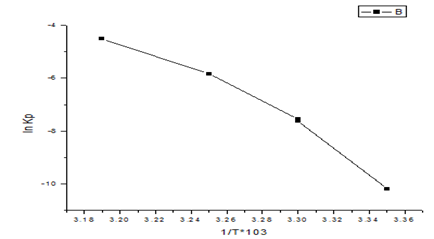
由图可知该直线的斜率为(10.20-3.33)/(3.14-3.35)*10-3 = -32.714×103
(1)-ΔrH? m/R = -32.714×103,ΔrH? m=32.714×103×8.314=271.98kJ/mol
(2)查阅资料知25℃氨基甲酸铵分解的ΔrH? m=159.32kJ/mol,
故相对误差=|159.32-271.98|/159.32×100%=70.7%
(3)25℃时:ΔrG? m=-RT ln K? p=-8.314×298.15×(-10.20)=25.284kJ/mol
(4)△rSm0=(△rHm0-△rGm0)/T=(271.98-25.284)/298.15=0.827KJ/mol· K
六、注意事项
1、体系必须达到平衡后,才能读取数字压力计的压力差。
2、恒温槽温度控制到±0.1℃。
3、玻璃等压计中的封闭液一定要选用粘度小,密度小,蒸汽压低,并且与反应体系不发生作用的液体。
4、步骤1中不能让液体石蜡进入样品管。
5、步骤4中不可使空气进入过快,避免空气进入样品管。
七、结果与讨论
1、一定要检查系统是否漏气,关闭真空泵,关闭阀门,观察平衡常数测定仪的示数是否变化。
2、判断氨基甲酸铵分解达平衡的标准:U型等压计两臂的液面无论是否等高,在1min内,液面不再变化即可认为反应体系已达平衡。
八、 思考题
1、 若体系有漏气的地方会发生什么现象?
答:若体系有漏气,等压计液面水平的平衡保持不住,无法测得NH2COONH4分解的平衡压力。
2、 当空气通入体系时,若通得过多有何现象出现?怎么办?
答:空气通的过多,空气会进入样品管,得到的蒸气压数据就会偏大,平衡常数就会偏大。
第二篇:物化-氨基甲酸铵分解反应标准平衡常数的测定
宁波工程学院
物理化学实验报告
专业班级 姓名 序号 实验日期
同组姓名 指导老师
实验名称 氨基甲酸铵分解反应标准平衡常数的测定
一、 实验目的
1、掌握测定平衡常数的一种方法;
2、用等压法测定氨基甲酸铵的分解压力并计算分解反应的有关热力学常数。
二、 实验原理
氨基甲酸铵是白色固体,是合成尿素的中间产物,它很不稳定,易分解成NH3和CO2 。
其分解反应式为:
NH2COONH4(s) 2NH3(g)+CO2(g)
2NH3(g)+CO2(g)
在常压下其平衡常数可近似表示为:
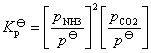
未达到平衡时体系的总压力为p,固体NH2COONH4产生的分压很小,可以忽略不计其中,又体系中的NH3和CO2全部是由氨基甲酸铵分解长生的,所以:
p=pNH3+pCO2
由反应方程式可知
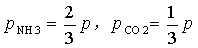
所以:
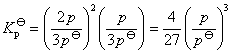
因此可知当体系达平衡后,测量其总压p,即可计算出平衡常数Kθp温度对平衡常数的影响一般都很显著的,其定量关系为:
 (C′为积分常数) (1)
(C′为积分常数) (1)
若以ln Kθp对1/T作图,应为一直线,其斜率为 -ΔrHθm/R。由此可求出ΔrHθm。在一个小的温度区间内,也可用此式计算出此温度区间的平均ΔrHθm。
因为任一温度下的平衡常数与反应的标准自由能变化值间有如下关系:
ΔrGθm =﹣RT ln Kθp (2)
可用平衡常数求出该反应的温度下的ΔrGθm 。
利用实验温度范围内反应的平均等压热效应ΔrHθm和T温度下的标准吉布斯自由能变化ΔrGθm,可近似计算出该温度下的熵变ΔrSθm 。
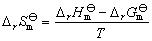 (3)
(3)
三、 实验仪器、试剂
仪器 :循环水泵,低真空数字测压仪,等压计,恒温槽一套,样品管;
试剂 :氨基甲酸铵,液体石蜡。
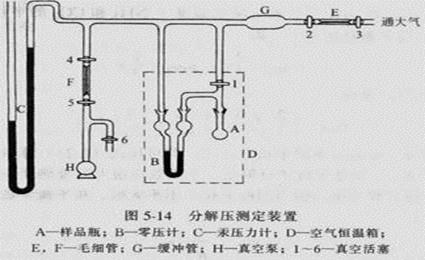
四、 实验步骤
1、由特制的小漏斗将氨基甲酸铵粉末小心装入干燥的球状样品管中,与已装好的液体石蜡的等压计连好。注意不能让液体石蜡进入样品管;
2、开动循环水泵,旋转活塞10与体系相通,旋转活塞10和减压瓶2相通,旋转活塞12至三个方向都通,此时观察到的测压仪数字应不断减小,至低真空测压仪示数为-90KPa以下时,关闭活塞11,检查体系气密性;
3、恒温槽中加水至没过样品管和等压计,调节恒温槽水温至25℃;
4、旋转活塞11,抽吸大约1分钟,把样品管中的空气抽走,然后关闭活塞11.慢慢旋转活塞13,缓慢放入空气进入体系,使U型等压计液面水平。若1分钟内保持液面水平,记下低真空测压仪的读数,即为氨基甲酸铵分解的平衡压力;
5、用同样的方法测25℃,30℃,35℃,40℃,45℃的分解压力;
6、整理实验数据,收拾实验仪器和药品。
五、 数据记录与处理
室温:17.4℃ 大气压力:101.92KPa
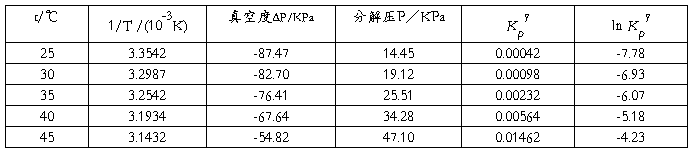

从图中测量所得的斜率为 -1.749×104 ;
ΔrHθm = ﹣(﹣1.749 )× 104 × 8.314 = 145390 J/mol = 145.390 kJ/mol ;
已知25℃时氨基甲酸铵的标准ΔrHθm = 159.32 kJ/mol ;
故相对偏差为 8.74% 。
ΔrGθm =﹣RT ln Kθp = 8.314 × 298.15 × 7.78 = 19285 J/mol = 19.285 kJ/mol ;
ΔrSθm = (ΔrHθm﹣ΔrGθm )/T = (145.390﹣19.285)/298.15 = 0.423 kJ/mol·K =423 J/mol·K
六、 注意事项
1、体系必须平衡后,才能读取数字压力计的压力差;
2、恒温槽温度控制到不相差0.1℃;
3、玻璃等压计中的封闭液一定要选用黏度小,密度小,蒸汽压低。并且与反应体系不 发生作用的液体。
七、 结果与讨论
刚开始实验的时候未能将样品球内的空气完全排尽,对实验有一定的影响;
U型等压计液面等高调节有失误,未能等到液面完全等高便读取数据。
八、 思考题
1、若体系有漏气的地方会发生什么现象?
平衡常数测定仪的示数会一直变大,稳定不下来;
关闭真空泵,关闭阀门,观察平衡常数测定仪的示数是否变化,若变化则说明系统漏气。
2、当空气通入体系时,若通得过多有何现象出现?怎么办?
得到的蒸气压数据就会偏大,平衡常数就会偏大;
开真空包将空气抽出。
