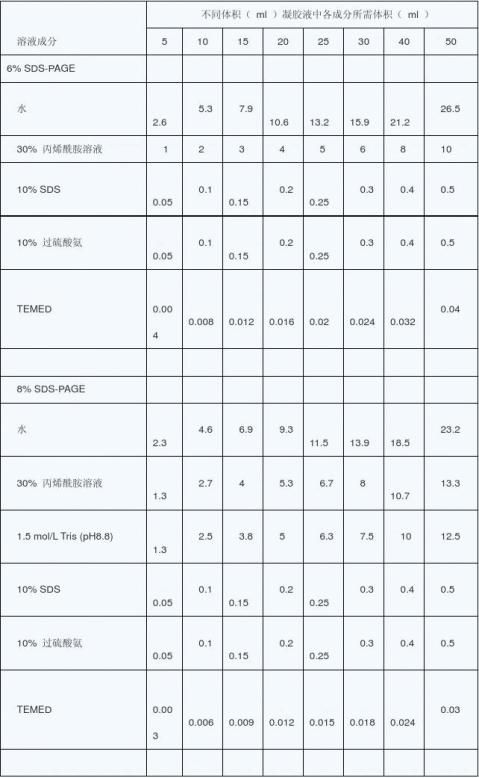
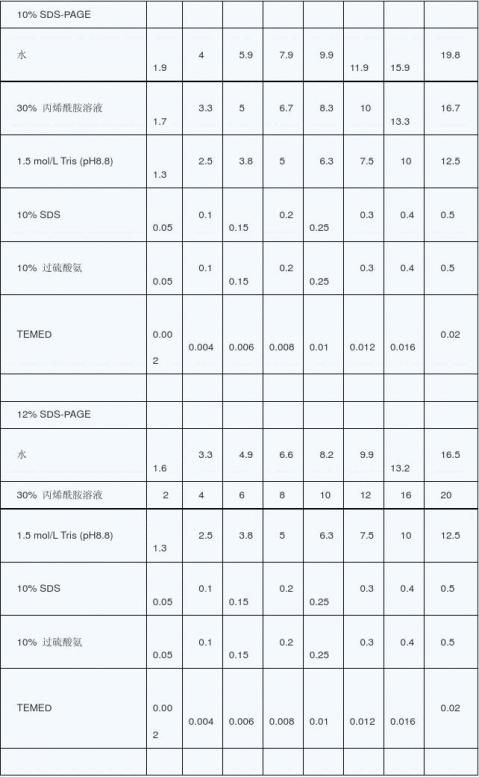
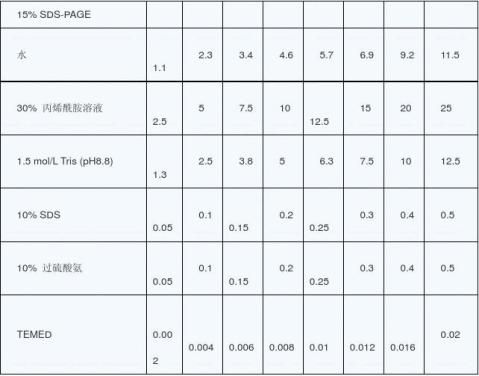
聚丙烯酰胺凝胶电泳是以聚丙烯酰胺凝胶作为支持介质的电泳方法。在这种支持介质上可根据被分离物质分子大小和分子电荷多少来分离。
聚丙烯酰胺凝胶有以下优点:
①聚丙烯酰胺凝胶是由丙烯酰胺和N,N'甲叉双丙烯酰胺聚合而成的大分子。凝胶有 格子是带有酰胺侧链的碳-碳聚合物,没有或很少带有离子的侧基,因而电渗作用比较小,不易和样品相互作用。
②由于聚丙烯酰胺凝胶是一种人工合成的物质,在聚合前可调节单体的浓度比,形成 不同程度交链结构,其空隙度可在一个较广的范围内变化,可以根据要分离物质分子 的大小,选择合适的凝胶成分,使之既有适宜的空隙度,又有比较好的机械性质。一 般说来,含丙烯酰胺7-7.5%的凝胶,机械性能适用于分离分子量范围不1万至100万物 质,1万以下的蛋白质则采用含丙烯酰胺15-30%的凝胶,而分子量特别大的可采用含 丙烯酰胺4%的凝胶,大孔胶易碎,小孔胶则难从管中取出,因此当丙烯酰胺的浓度增 加时可以减少双含丙烯酰胺,以改进凝胶的机械性能。
③在一定浓度范围聚丙烯酰胺对热稳定。凝胶无色透明,易观察,可用检测仪直接测定。
④丙烯酰胺是比较纯的化合物,可以精制,减少污染。合成聚丙烯酰胺凝胶的原料是丙烯酰胺和甲撑双丙烯酰胺。丙烯酰胺称单体,甲撑双 丙烯酰胺称交联剂,在水溶液中,单体和交联剂通过自由基引发的聚合反应形成凝 胶。
在聚丙烯酰胺凝胶形成的反应过程中,需要有催化剂参加,催化剂包括引发剂和 另速剂两部分。引发剂在凝胶形成中提供始自由基,通过自由基的传递,使丙烯酰胺 成为自由基,发动聚合反应,加速剂则可加快引发剂放自由基的速度。常用的引发剂 和加速剂的配伍如下表:
聚合反应催化剂配伍

注:(NH4)2S2O8,过硫酸胺 TEMED:N,N,N,N';四甲基乙二胺 DMAPN:β-二甲基胺基丙晴 用过硫酸铵引发的反应称化学聚合反应;用核黄素引发,需要强光照射反应液, 称光聚合反应。 聚丙烯酰胺聚合反应可受下列因素影响: 1、大气中氧能淬灭自由基,使聚合反应终止,所以在聚合过程中要使反应液与空气 隔绝。 2、某些材料如有机玻璃,能抑制聚合反应。 3、某些化学药物可以减慢反应速度,如赤血盐。 4、温度高聚合快,温度低聚合慢。 以上几点在制备凝胶时必须加以注意。 凝胶的筛孔,机械强度及透明度等很大程度上由凝胶的浓度和交联决定。每100亳升 凝胶溶液中含有单体和交联剂的总克数称凝胶浓度,常用T%表达;凝胶溶液中交联剂 占单体和交联体总量的百分数称为交联度,常用C%表示,可用下式计算:
公 式
a:丙烯酰胺克数; b:甲撑双丙烯酰胺克数;m:缓冲液体积(毫升) 凝胶浓度过高时,凝胶硬而脆,容易破碎;凝胶浓度太低时,凝胶稀软,不易操作。
交联度过高,胶不透明并缺乏弹性;交联度过低,凝胶呈糊状。 聚丙烯酰胺凝胶具有较高的粘度,它不防止对流减低扩散的能力,而且因为它具有三 度空间网状结构,某分子通过这种网孔的能力将取决于凝胶孔隙和分离物质颗粒的大 小和形状,这是凝胶的分子筛作用。由于这种分子筛作用,这里的凝胶并不仅是单纯 的支持物,因此,在电泳过程中除了注意电泳的基本原理以外,还必须注意与凝胶本 身有关的各种性质(网孔的大小和形状等)。可通过下式计算来选择适当的凝胶网 孔。
公 式
式中:P为网孔平均直径,C为多聚体浓度,d为该多聚体分子直径(若不是卷曲的分 子应为5A),K为常数,K值取决于涨胶的几何构型,假如多聚体的链是以近似于直角 交联的,则约为1.5根据此式,我们可以通过多聚体浓度C近似地计算出网孔直径,例 如已知多聚体浓度为5%,其网孔平均直径应为:
公 式
这样的计算是粗略的,与实际情况有一定距离,有人测定了总浓度(T)为20%的丙烯酰胺液,在六种不同比例的双丙烯酰胺存在 下,聚合后的网孔大小,发现孔径与总浓度有关,总浓度愈大,孔径相应变小,机械 强度增强,与总浓度不变时,甲叉双丙烯酰胺(Bis)的浓度在5%时孔径最小,高于或 低于此值时,聚合体孔径都相对变大,凝胶孔径在凝胶电泳中是一个重要的参数,它 往往决定了电泳的分离效果。经过不断的实践,得到了如表3所示的经验值,在一般情况下,大多数生物体内的蛋白质采用7.5%浓 度的凝胶,所得电泳结果往往是满意的,因此称由此浓度组成的凝胶为“标准凝 胶”。
对那些用于重要研究的凝胶,最好是通过采用10%的一系列凝胶浓度梯进行预先试验,以选出最适凝胶浓度。
表3不同分子量范围的蛋白质和核酸在凝胶电泳 中所选用的凝胶浓度百分率

聚丙烯酰胺凝胶电泳可分为连续的和不连续的两类,前者指整个电泳系统中所用缓冲 液,pH值和凝胶网孔都是相同的,后者是指在电泳系统中采用了两种或两种以上的缓 冲液,pH值和孔径,不连续电泳能使稀的样品在电泳过程中浓缩成层,从而提高分辨 能力。
蛋白质在聚丙烯酰胺凝胶中电泳时,它的迁移率取决于它所带净电荷以及分子的大小 和形状等因素。如果加入一种试剂使电荷因素消除,那电泳迁移率就取决于分子的大 小,就可以用电泳技术测定蛋白质的分子量。1967年,Shapiro等发现阴离子去污剂 十二烷基硫酸钠(SDS)具有这种作用。当向蛋白质溶液中加入足够量SDS和巯基乙 醇,SDS可使蛋白质分子中的二硫键还原。由于十二烷基硫酸根带负电,使各种蛋白 质—SDS复合物都带上相同密度的负电荷,它的量大大超过了蛋白质分子原的电荷量, 因而掩盖了不同种蛋白质间原有的电荷差别,SDS与蛋白质结合后,还可引起构象改 变,蛋白质—SDS复合物形成近似“雪茄烟”形的长椭圆棒,不同蛋白质的SDS复合物 的短轴长度都不一样,约为18A,这样的蛋白质—SDS复合物,在凝胶中的迁移率,不 再受蛋白质原的电荷和形状的影响,而取决于分子量的大小,因而SDS聚丙烯酰胺凝胶电泳可以用于测定蛋白质的分子量。
蛋白质的聚丙烯酰胺凝胶电泳
一、实验目的
1. 了解电泳实验原理
2. 掌握电泳实验操作规程
3. 用电泳方法测定蛋白分子量
二、实验原理
最广泛使用的不连续缓冲系统最早是由Ornstein(1964) 和Davis(1964) 设计的, 样品和浓缩胶中含 Tris-HCl(pH 6.8), 上下槽缓冲液含Tris-甘氨酸(pH 8.3), 分离胶中含Tris-HCl(pH 8.8)。系统中所有组分都含有0.1% 的 SDS(Laemmli, 1970)。样品和浓缩胶中的氯离子形成移动界面的先导边界而甘氨酸分子则组成尾随边界,在移动界面的两边界之间是一电导较低而电位滴度较陡的区域, 它推动样品中的蛋白质前移并在分离胶前沿积聚。此处pH值较高, 有利于甘氨酸的离子化,所形成的甘氨酸离子穿过堆集的蛋白质并紧随氯离子之后,沿分离胶泳动。从移动界面中解脱后,SDS-蛋白质复合物成一电位和pH值均匀的区带泳动穿过分离胶,并被筛分而依各自的大小得到分离。
SDS与蛋白质结合后引起蛋白质构象的改变。SDS-蛋白质复合物的流体力学和光学性质表明,它们在水溶液中的形状,近似于雪茄烟形状的长椭园棒,不同蛋白质的SDS复合物的短轴长度都一样(约为18Å,即1.8nm),而长轴则随蛋白质分子量成正比地变化。这样的SDS-蛋白质复合物,在凝胶电泳中的迁移率,不再受蛋白质原有电荷和形状的影响,而只是椭园棒的长度也就是蛋白质分子量的函数。
由于SDS和巯基乙醇的作用,蛋白质完全变性和解聚,解离成亚基或单个肽链,因此测定的结果只是亚基或单条肽链的分子量。
SDS聚丙烯酰胺凝胶的有效分离笵围取决于用于灌胶的聚丙烯酰胺的浓度和交联度。在没有交联剂的情况下聚合的丙烯酰胺形成毫无价值的粘稠溶液,而经双丙烯酰胺交联后凝胶的刚性和抗张强度都有所增加,并形成SDS蛋白质复合物必须通过的小孔。这些小孔的孔径随 “双丙烯酰胺~丙烯酰胺” 比率的增加而变小,比率接近 1:20 时孔径达到最小值。SDS聚丙烯酰胺凝胶大多按“双丙烯酰胺~丙烯酰胺”为1:29 配制,试验表明它能分离大小相差只有3% 的蛋白质。
凝胶的筛分特性取决于它的孔径,而孔径又是灌胶时所用丙烯酰胺和双丙烯酰胺绝对浓度的函数。用5~15%的丙烯酰胺所灌制凝胶的线性分离范围如下表:
SDS聚丙烯酰胺凝胶的有效分离范围

*双丙烯酰胺~丙烯酰胺摩尔比为 1:29。
三、实验材料和试剂
1. 试剂
(1)丙烯酰胺和N, N’-亚甲双丙烯酰胺。以温热(利于溶解双丙烯酰胺)的去离子水配制含有29%(w/v)丙烯酰胺和1%(w/v)N, N’-亚甲双丙烯酰胺的贮存液,丙烯酰胺和双丙烯酰胺在贮存过程中缓慢转变为丙烯酸和双丙烯酸,这一脱氨基反应是光催化或碱催化的,故应核实溶液的pH值不超过7.0。这一溶液置棕色瓶中贮存于室温,每隔几个月须重新配制。
小心:丙烯酰胺和双丙烯酰胺具有很强的神经毒性并容易吸附于皮肤。
(2) 十二烷基硫酸钠(SDS)。SDS可用去离子水配成10%(w/v)贮存液保存于室温。
(3)用于制备分离胶和积层胶的Tris缓冲液。
(4)TEMED(N,N,N’,N’-四甲基乙二胺)。TEMED通过催化过硫酸铵形成自由基而加速丙烯酰胺与双丙烯酰胺的聚合。
(5)过硫酸铵。 过硫酸铵提供驱动丙烯酰胺和双丙烯酰胺聚合所必需的自由基。须新鲜配制。
(6)1.5M Tris,pH8.8(分离胶缓冲液)
(7)1M Tris,pH6.8(浓缩胶缓冲液)
(8)Tris-甘氨酸电泳缓冲液。
25mM Tris,250mM 甘氨酸 (pH 8.3),0.1% SDS,
(9) 样品处理液 ,50mM Tris-HCl(pH 6.8),100mM DTT(or 5% 巯基乙醇),2% SDS,0.1% 溴酚蓝,10%甘油
(10)染色液:
0.1% 考马斯亮蓝 R250,40% 甲醇,10% 冰醋酸
(11)脱色液:
10% 甲醇,10% 冰醋酸
四、实验步骤
1. 配制SDS聚丙烯酰胺凝胶所需的各种试剂
2.SDS聚丙烯酰胺凝胶的灌制 (realplay)
⑴ 根据厂家说明书安装玻璃板。
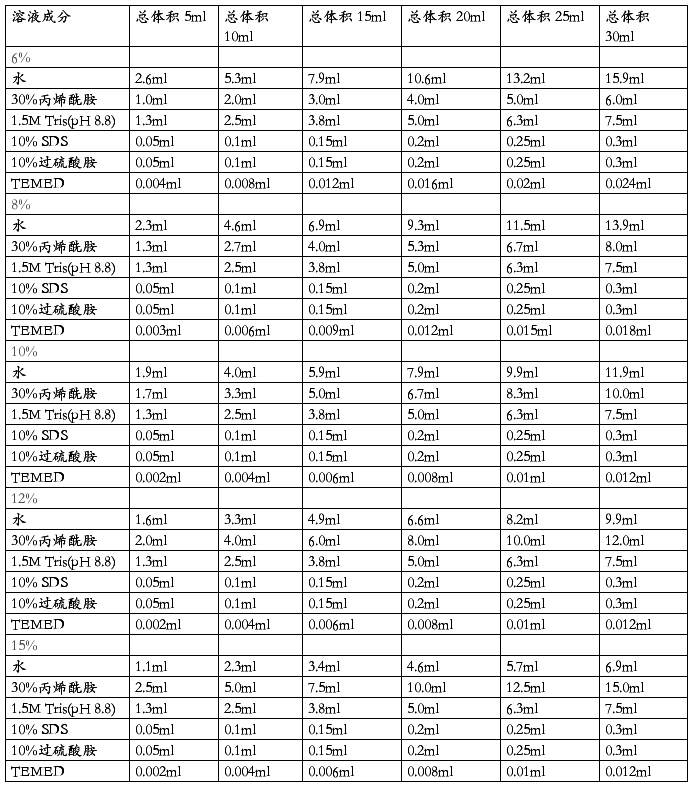
⑵ 确定所需凝胶溶液体积,按下表给出的数值在一小烧杯中按所需丙烯酰胺浓度配制一定体积的分离胶溶液。一旦加入TEMED,马上开始聚合,故应立即快速旋动混合物并进入下步操作。
配制Tris-甘氨酸SDS聚丙烯酰胺凝胶电泳分离胶溶液
⑶ 迅速在两玻璃板的间隙中灌注丙烯酰胺溶液,留出灌注浓缩胶所需空间(梳子的齿长再加0.5cm)。再在胶液面上小心注入一层水(约2~3mm高),以阻止氧气进入凝胶溶液。
⑷ 分离胶聚合完全后(约30分钟),倾出覆盖水层,再用滤纸吸净残留水。
⑸ 制备浓缩胶:按下表给出的数据,在另一小烧杯中制备一定体积及一定浓度的丙烯酰胺溶液,一旦加入TEMED,马上开始聚合,故应立即快速旋动混合物并进入下步操作。
配制Tris-甘氨酸 SDS聚丙烯酰胺凝胶电泳5% 浓缩胶溶液

⑹聚合的分离胶上直接灌注浓缩胶,立即在浓缩胶溶液中插入干净的梳子。小心避免混入气泡,再加入浓缩胶溶液以充满梳子之间的空隙,将凝胶垂直放置于室温下。
⑺在等待浓缩胶聚合时,可对样品进行处理,在样品中按1:1体积比加入样品处理液,在100℃加热3分钟以使蛋白质变性。
⑻ 浓缩胶聚合完全后(30分钟),小心移出梳子。把凝胶固定于电泳装置上,上下槽各加入Tris-甘氨酸电极缓冲液。必须设法排出凝胶底部两玻璃板之间的气泡。
⑼ 按予定顺序加样,加样量通常为10~25μl(1.5mm厚的胶)。
⑽ 将电泳装置与电源相接,凝胶上所加电压为8V/cm。当染料前沿进入分离胶后,把电压提高到15V/cm,继续电泳直至溴酚蓝到达分离胶底部上方约1cm,然后关闭电源。
⑾ 从电泳装置上卸下玻璃板,用刮勺撬开玻璃板。紧靠最左边一孔(第一槽)凝胶下部切去一角以标注凝胶的方位。
3.用考马斯亮蓝对SDS聚丙烯酰胺凝胶进行染色
经SDS聚丙烯酰胺凝胶电泳分离的蛋白质样品可用考马斯亮蓝R250染色。染色1~2小时或过夜。
4. 换脱色液脱色,需3~10小时,其间更换多次脱色液至背景清楚。
此方法检测灵敏度为0.2~1.0 mg。脱色后,可将凝胶浸于水中,长期封装在塑料袋内而不降低染色强度。为永久性记录,可对凝胶进行拍照,或将凝胶干燥成胶片。


五、结果处理
测量并计算分子量
蛋白质的分子量与它的电泳迁移有一定关系式,经37种蛋白的测定得到以下的关系式:
Mw = K (10-bm) (1)
lgMw = lg K -bm = K1-bm (2)
其中Mw是蛋白质分子量;K和K1为常数
b为斜率,m 是电泳迁移率,实际使用的是相对迁移率mR。
如果用几种标准蛋白质分子量的对数作纵坐标,用各自的相对迁移率作横坐标,即可画出一条斜率为负的标准曲线。相对迁移率为:
其中,dpr、dBPB分别为样品和BPB(溴酚兰)以分离胶表面为起点迁移的距离。
欲求未知蛋白的分子量,只需求出它的相对迁移率:
mR未= dpr未/ dBPB
然后,从标准曲线上就可求出此未知蛋白的分子量。
取出脱色后的凝胶平放在两块透明投影胶片中间,赶尽气泡,在复印机上复印。在复印的凝胶图上用直尺分别量出各条蛋白带迁移的距离dpr和dBPB(以蛋白带的上沿或中心为准),计算相对迁移率,根据方程式:
lgMw = K1-bmR
用各标准蛋白分子量的对数(纵坐标)和相对迁移率mR(横坐标)画出标准曲线,由标准曲线再求出其他各条待测和未知蛋白带的分子量,如有可能计算其误差
蛋白质聚丙烯酰胺凝胶电泳--生物秀PCR技术
【实验试剂和器材】
(一)试剂
1. 制备分离胶、浓缩胶有关试剂
(1)凝胶贮液:在通风橱中,称取丙烯酰胺29g,甲叉双丙烯酰胺1g,加重蒸水溶解后,定容到100ml。过滤后置棕色瓶中,4℃保存,一般可放置1个月。
(2)pH8.9分离胶缓冲液: Tris 36.3g ,加1mol/L HCl 48ml,加重蒸水80ml使其溶解,调pH8.9,定容至100ml, 4℃保存。
(3)pH6.7浓缩胶缓冲液: Tris 5.98g ,加1mol/L HCl 48ml,加重蒸水80ml使其溶解,调pH6.7,定容至100ml, 4℃保存。
(4) TEMED(四乙基乙二胺)原液
(5)10%过硫酸铵(用重蒸水新鲜配制)
2. pH8.3 Tris-甘氨酸电极缓冲液
称取Tris 6.0g,甘氨酸28.8g,加蒸馏水约900ml,调pH8.3后,用蒸馏水定容至1000ml。置4℃保存,临用前稀释10倍。
3. 50% (v/v)甘油
4. 1% (w/v) 溴酚蓝:称取100mg溴酚蓝,加蒸馏水10ml,搅拌直到完全溶解,过滤除去聚合的染料。
5. 5× 样品缓冲液(loading buffer):10ml
3.1ml 1mol/L Tris-HCl (pH6.7) 312.5mmol/L
5ml 50% (v/v)甘油 25%
0.5ml 1% (w/v) 溴酚蓝 0.05%
1.4ml 蒸馏水
4. 考马斯亮蓝G250染色液:称100mg考马斯亮蓝G250,溶于200ml蒸馏水中,慢慢加入7.5ml
70%的过氯酸,最后补足水到250ml,搅拌1小时,小孔滤纸过滤。
第二篇:聚丙烯酰胺凝胶电泳凝胶的配方