氧气的制备与性质
一、实验原理
1、高锰酸钾法:
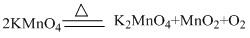 ↑
↑
2、过氧化氢法:
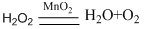 ↑
↑
3、氧气的性质:
在通常状况下,O2为无色无味的气体。在标准状况下,O2的密度比空气的平均密度大。不易溶于水。
氧气的化学性质比较活泼。它不仅可以助燃,而且在点燃或高温条件下可以和大多数金属、非金属发生反应,放出大量热。
二、实验操作过程与实验现象
1、氧气的制取与收集
(1)、过氧化氢分解制备法
1、安装实验装置如下图
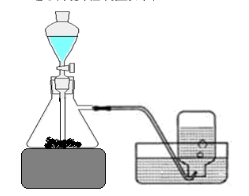
2、实验步骤:
a、检查装置气密性
b、在蒸馏烧瓶中装入0.5克MnO2,将与烧瓶口匹配的分液漏斗塞住烧瓶口,分液漏斗中加入H2O2(以体积比水:过氧化氢=1:3稀释过的过氧化氢溶液);
c、将集气瓶装满水并倒扣于水槽中,打开分液漏斗活塞,等到导管口有均匀连续气泡逸出,将导管伸入集气瓶内(此时集气瓶仍为倒置),观察到有连续的气泡从瓶口冒出,移开导管,用玻璃片毛面迅速封口,从水槽中取出集气瓶既可。收集四瓶气体。
※实验现象:
1打开分液漏斗活塞后,可以观察有大量气泡冒出.
2同时观察到烧瓶中出现烟雾.
(2)高锰酸钾加热分解制备法:
1、安装实验装置如下图

2、实验步骤:
a、检查装置气密性
b、称取3克高锰酸钾加入硬质试管中,管口塞一块蓬松的脱脂棉,塞紧单孔塞
c、点燃酒精灯后,先预热试管,然后集中在药品处加热
d、用排水法收集
※实验现象:
1高锰酸钾在加热时有强烈的迸裂
 2并伴有少量烟产生
2并伴有少量烟产生
2、氧气的性质
 (1)、硫在O2中的燃烧:
(1)、硫在O2中的燃烧:
取一洁净的燃烧匙,放入少量硫磺粉,在酒精灯上加热至燃烧,然后将燃着的硫匙由上往下缓缓伸进集有O2的集气瓶中。
※实验现象:
在酒精灯上加热会发出微弱的淡蓝色火焰,而在氧气瓶中火焰颜色为明亮的蓝色,并有刺激性气味的气体产生。
(2)、碳在O2中的燃烧:
用坩埚钳夹取一小段木炭,在酒精灯上烧至红热,再缓慢伸进盛满氧气的集气瓶中,观察现象。给此集气瓶中倒入少量澄清石灰水,振荡。
※实验现象:
木炭在O2中燃烧剧烈,并发出白色亮光,并伴有少量烟产生。加入的澄清石灰水变浑浊。
(3)、铁在O2中的燃烧:
取一小段细铁丝,将其绕在火柴上,用坩埚钳夹住两头的铁丝,点燃火柴,烧至火焰将尽时,伸入瓶底留有少许水的集气瓶中。
※实验现象:
在空气中只看到火柴燃烧,铁丝被烧红。铁丝在氧气中燃烧,火星四射,并生成黑色的熔融物。
(4)、蜡烛在O2中的燃烧:
取一小截蜡烛,点燃后伸入集气瓶中,观察现象,给此集气瓶中倒入少量澄清石灰水,振荡。
※实验现象:
蜡烛在酒精灯上只在一端燃烧,而在O2中会全部燃烧,火焰更加亮白,石灰水变浑浊。
三、实验应注意的事项
1、在加热高锰酸钾时,颗粒容易迸裂而从导气管冲进水槽,或致导气管堵塞,因此要在试管口放一团脱脂棉;而且加热前要先预热,然后集中加热。
2、使用过氧化氢时,要注意先用蒸馏水稀释,控制滴加速度;将分液漏斗中的过氧化氢完全加入到蒸馏烧瓶中后,需要将活塞关闭,以免气体从漏斗排出,影响实验的进行。
3、排水法收集气体完后,要先把导气管从水槽中取出再撤装置,防止倒吸。
4、燃烧物定要放于集气瓶中央,切勿靠近瓶壁,以防集气瓶炸裂
5、在硫的燃烧试验中,为避免污染空气,将燃烧匙取出后及时淬入盛有冷水的大烧杯中;
6、在铁丝的燃烧试验中,集气瓶底一定要铺细砂或者留有部分水,高温的熔融物会使集气瓶底炸裂。
四、相关文献与重点文献综述
1、铁丝在氧气中燃烧实验的探究
(1)、铁丝为什么要绕在一根火柴上?
点燃火柴后,放出热量,使铁丝达到一定温度才能在氧气中燃烧,即火柴起预热铁丝的作用;而且螺旋状是为了增大铁丝与氧气的接触面积。同理,我们可以只让铁丝绕成螺旋状,蘸入酒精中,也可起到此作用。
(2)、铁丝伸人集气瓶时,为什么要从瓶的正中央慢慢地往下移?
因铁丝燃烧时放出大量的热,若不在瓶的正中央伸人,会使集气瓶局部过热而炸裂,如果快速伸人,则会将瓶里中部和上部的氧气排出,铁丝就不能顺利燃烧
(3)、集气瓶里为什么要预先盛少量水或铺一薄层细沙?
防止实验时溅落的高温熔化物炸裂瓶底。
(4)“火星四射”为什么不能说成“耀眼的火焰”?
火焰是由气体或蒸气燃烧而形成的现象,而铁丝是固体,且熔点极高,不易气化,因而看不到火焰
2、氧气的化学性质“很活泼”应该为“比较活泼”:
人教社20##年3月第一版初中《化学(全一册)》,第一章第二节中对氧气化学性质的叙述为:“通过以上实验可以看出,氧气是一种化学性质比较活泼的气体”;但又在第四节这样叙述:“证明氧气性质的几个实验,不仅说明了氧气的化学性质很活泼……”表示物质化学性质时用很活泼、比较活泼、不活泼、很不活泼是有一定区别的。
通过14页习题2.(3)可知,,第四节的表述应改为:“证明氧气性质的几个实验,不仅说明了氧气的化学性质比较活泼……”氧气的化学性质“很活泼”应改为“比较活泼”。
3、本次试验的目的
(1)、首先,对比三种制取氧气方法,了解其优缺点,由于氯酸钾制取氧气反应装置复杂,操作不当容易引起试管炸裂,所以本次实验不用此方法。
(2)、教材所提供的三种制取氧气的方法其教学侧重点是不一样的: “用双氧水和二氧化锰混合制取氧气” 侧重于催化剂概念的教学; 用“氯酸钾和二氧化锰混合共热制取氧气” 侧重于基本实验方法和技能的教学; “单独加热高锰
酸钾制取氧气” 侧重于为中学化学的后续学习打下基础。
(3)、即将作为教师的我们在演示实验中不仅要引导学生从物质颜色、状态的变化、是否有气体等方面进行观察实验,还要引导学生将所观察的实验现象进行总结提升,达到以实验促进知识掌握的目的。
五、参考文献
1、胡大勇.氧气的化学性质“很活泼”应该为“比较活泼”〔J〕.实验教学与仪器,2003,2:42
2. 耿庆梅 刘金瑞. 新课程下的化学实验教学〔J〕.现代教育科学·中学教师,2001.3:25
3. 徐良水 曹向华.氧气性质实验探究〔J〕.中学生数理化,2003,25:59
第二篇:氧气的性质与制备实验报告
氧气的制备与性质实验探究报告
一 实验目的
1、熟悉实验室制取氧气的反应原理,掌握实验室制取和收集氧气的方法及其性质实验的操作技巧。
2、练习药品的取用及装置气密性检查。
二 实验原理
我们都知道,约占空气体积1/5的氧气与人类的生活、生产有着很密切的关系,是人类维持生命不可缺少的物质,动物和植物的生存也都离不开氧气。在通常情况下,O2为无色无味的气体。在标准情况下,O2比空气的密度大。不易溶于水(每升水溶解O2约30ml)
氧气的化学性质很活泼。它不仅可以助燃,而且在点燃或高温条件下可以和大多数金属(如铁、镁)、非金属(木炭、硫、磷、和石蜡等)发生反应,放出大量的热。
2KMnO4===K2MnO4 + MnO2 + O2↑

2H2O2 === 2H2O+O2↑
三 仪器、材料与药品
硬质大试管、锥形瓶、分液漏斗、单孔橡皮塞、酒精灯、火柴、垫木、水槽、集气瓶、蒸发皿、研钵、毛玻璃片、橡皮软管、铁架台、玻璃棒、钥匙、脱脂棉、托盘天平、燃烧匙、·大烧杯、坩埚钳、砂纸、试管及试管架;
KMnO4、10﹪H2O2、硫磺、木炭、铁丝、蜡烛、澄清石灰水。
四 实验内容
⑴ KMnO4加热分解法
2KMnO4===K2MnO4 + MnO2 + O2↑
实验步骤
①----按照下图组装好仪器
组装仪器的顺序是从上到下,从左到右。注意:试管口略向下倾斜约15度。

②----检查装置的气密性
用手握住试管(或用热毛巾捂住试管),若有气泡冒出则证明装置的气密性良好。

③----装药品
由于KMnO4是固体药品,所以纸槽装好KMnO4,缓缓倒入试管中。
④----把试管固定到铁架台上
注意将将试管固定在1/3处。
⑤----点燃酒精灯加热
确保酒精灯内的酒精约为1/4—2/3。先预热。注意,让试管均匀受热,否则会因冷热不均炸裂试管 。
⑥----收集气体(可以使用排水法、向上排空法)
⑦----把导气管从水槽中取出
如果使用向上排空法,此步骤基本不需要,但是最好先取出导管在盖上玻片。
⑧----熄灭酒精灯
注意事项
① 实验前先检查装置的气密性。
② .试管口要略微向下倾斜:防止生成的水回流,使试管底部破裂。
③ 导气管伸入发生装置内要稍露出橡皮塞(不要太长)有利于产生的气体排出。
④ 试管口塞一团棉花:防止高锰酸钾粉末进入导气管,污染制取的气体和水槽中的水。
⑤ 加热时先预热。
⑥ 排气法收集气体时,导气管要伸入接近集气瓶底部:有利于集气瓶内空气排出,使收集的气体更纯。
⑦ 实验结束后,先将导气管移出水面,然后熄灭酒精灯:防止水槽中的
水倒流,炸裂试管。
⑵ H2O2分解法

2H2O2 === 2H2O+O2↑
①如下图,连接实验装置,顺序为由左到右,由上到下。
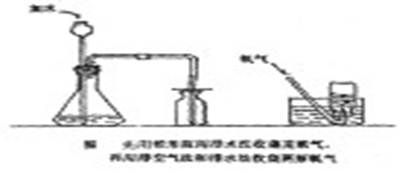
②检查装置的气密性
用手捂住锥形瓶口,若有气泡冒出,证明仪器的气密性良好。
③装药品
将固体药品二氧化锰缓缓倒入锥形瓶中;用20ml10% H2O2与40ml H2O混合配成30% H2O2缓慢加入分液漏斗中。
④收集气体(同上高锰酸钾收集法)
注意事项
①如果用长颈漏斗,应注意其颈部应在液面以下:防止气体从长颈漏斗泄露,可用分液漏斗代替(可随时控制反应的发生和停止,以及反应的速度);
②导管应稍露出橡皮塞,便于气体排出;
③由于H2O2易分解,稀释时应当用蒸馏水,并在使用前稀释。
五 氧气的性质实验
1 硫与氧气的反应
取一洁净的燃烧匙,放入少量硫粉,酒精灯上加热至燃烧,发出微弱的淡蓝色火焰。然后将燃烧着的硫匙由上往下缓缓伸进集有O2的集气瓶中,这时火焰呈现明亮的蓝紫色,并伴有刺激性气味的SO2产生。为避免污染空气,将燃烧匙取出后及时淬入盛有冷水的大烧杯中。
2 碳在O2中燃烧
用镊子夹取一小段木块碳,在酒精灯上烧至红热,再缓缓伸进盛满O2的集气瓶中,可看到木炭燃烧的更剧烈并发出白光。给集气瓶中倒入少量澄清石灰水,振荡,石灰水变浑浊。
3 铁在O2中燃烧
准备一条铁丝,砂纸擦亮后弯成螺旋状,系在火柴上。点燃火柴,伸入盛有水的集气瓶中,铁丝燃烧,火星四射,并生成 一种黑色熔融物。
4 蜡烛在O2中燃烧
用小刀截取长约1cm的蜡烛,放入燃烧匙,点燃后伸入集气瓶。蜡烛的火焰更加亮白。给集气瓶中倒入少量澄清石灰水,振荡,石灰水变浑浊。
注意事项
以上关于做O2性质的实验,燃烧物一定要放置于集气瓶中央,切勿靠近瓶壁,以防集气瓶炸裂。
六 讨论与研究
1、过氧化氢是液态,只需加入催化剂二氧化锰就可以反应,不需要加热,而且可以根据需要随开随停,并可以通过过氧化氢溶液的滴加速度来控制反应的速度和通过烧瓶内气体的冒出速度来判断反应速度,产物是水没有污染。
2、加热高锰酸钾制氧气的优点:能产生较为稳定的气流,反应速率适中,危险小。缺点:原料价格高,氧元素利用率低,反应装置复杂,操作不当容易引起试管炸裂,固体废弃物对环境有负面影响。
3、加热氯酸钾+二氧化锰 优点:氧元素利用率高,分解过程中无粉末飞扬。缺点:原料价格高,反应装置复杂,操作不当容易引起试管炸裂,固体废弃物对环境有负面影响,制取的氧气中混有较多氯气而有异味等。
