��������������Ӧ����ѧ
1.ʵ��Ŀ��
��ѧϰ�絼���ⶨ��������������Ӧ���ʳ�����ԭ���ͷ����Լ���ܵIJⶨ������
���˽������Ӧ���ص㣬ѧ����ͼ����㷨�������Ӧ�����ʳ�����
����Ϥ�絼�ǵ�ʹ�á�
2.ʵ��ԭ��
��1�����ʳ����IJⶨ
��������������Ӧʱ���͵Ķ�����Ӧ���䷴ӦʽΪ��
CH3COOC2H5��NaOH = CH3OONa��C2H5OH
t=0 C0 C0 0 0
t=t Ct Ct C0 - Ct C0 -Ct
t=�� 0 0 C0 C0
���ʷ���ʽ 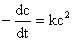 �����ֲ����������ʳ���k�ı���ʽΪ��
�����ֲ����������ʳ���k�ı���ʽΪ��
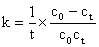
�ٶ��˷�Ӧ��ϡ��Һ�н��У���CH3COONaȫ�����롣��μӵ���������Na����OH����CH3COO��,��Na����Ӧǰ�䣬OH����Ǩ����ԶԶ����CH3COO�������ŷ�Ӧ�Ľ��У�
OH�� ���ϼ�С��CH3COO���������ӣ�������ϵ�ĵ絼�ʲ����½�������ϵ�絼�ʣ��ʣ�
���½��Ͳ���CH3COO����Ũ�ȳ����ȡ�
��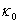 ��
��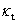 ��
��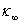 �ֱ�Ϊ0��t�͡�ʱ�̵ĵ絼�ʣ���
�ֱ�Ϊ0��t�͡�ʱ�̵ĵ絼�ʣ���
t=tʱ��C0 �CCt=K��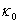 -
-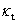 �� K��������
�� K��������
t����ʱ��C0= K��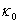 -
-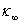 ��
��
��������ʽ�ӣ������ã�
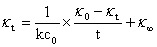
�ɼ�������֪��ʼŨ��C0���ں��������£����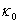 ��
��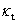 ������
������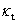 ��
��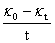 ��ͼ���ɵ�һֱ�ߣ���ֱ��б��
��ͼ���ɵ�һֱ�ߣ���ֱ��б��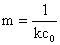 ���Ӷ���ô��¶��µķ�Ӧ���ʳ���k��
���Ӷ���ô��¶��µķ�Ӧ���ʳ���k��
��2����ܵIJⶨԭ����
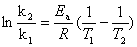
���ֻҪ���������ͬ�¶ȶ�Ӧ�����ʳ������Ϳ��������Ӧ�ı��ۻ�ܡ�
3.�������Լ�
���²� �絼����
�絼�缫 ���ε絼��
��� �ζ��ܣ���ʽ��
��Һ��10��25ml ����ƿ100��50ml
ĥ������ƿ100ml NaOH��Һ��Լ0.04 mol?dm-3��
����������A.R.��
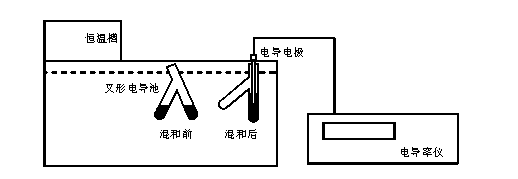
ͼC19.1 ʵ��װ��
4.ʵ�鲽��
1) ʵ��װ����ͼC19.1��ʾ�����ε絼����ͼC19.2��ʾ�������ε絼��ϴ����ɣ����ں��²���25�档
2) ����100mlŨ��Լ0.02 mol?dm-3����������ˮ��Һ��������������Է�������Ϊ88.12������100mlŨ��0.02 mol?dm-3����������ˮ��Һ��Ҫ��������0.1762g���ڽྻ��100ml����ƿ�м�������ȥ����ˮ��ʹ��0.0001g���ȵ���ƽ��ͨ������������������0.1762g���ҡ�����ȥ����ˮ���̶ȣ����ݼ����������������������������������Һ�ľ�ȷŨ�ȡ�ע���ڵμ���������֮ǰ��Ӧ������ƿ�м�������ȥ����ˮ���������������μ��ڿ�ƿ�����ӷ������������ڵμ���������ʱ����ʹ��ϸС�ĵιܣ�ʹ������������������������ӽ�0.1762g����С��0.1762gΪ�ˡ��μ���������ʱ��Ҫ�μ���ƿ���ϣ�Ҫ��ȫ�μӵ���Һ�С�

3) ����100ml��������������������ҺŨ����ͬ��NaOHˮ��Һ������ʵ�������ṩNaOH��Һ�ľ�ȷŨ�ȣ����������NaOH��Һ��������õζ��ܽ������NaOH��Һ���뵽�ྻ��100ml����ƿ�У���ȥ����ˮϡ�����̶ȡ�
4)  �IJ���������Һ��ȡ����������Ũ����ͬ��NaOH��Һ25.00ml�����뵽�ྻ��50ml����ƿ�У���ȥ����ˮϡ�����̶ȣ����ڲ���
�IJ���������Һ��ȡ����������Ũ����ͬ��NaOH��Һ25.00ml�����뵽�ྻ��50ml����ƿ�У���ȥ����ˮϡ�����̶ȣ����ڲ��� ��ȡ����Һһ���ַ��뵽�ྻ����IJ��ε絼��ֱ֧���У��ò�����Һ��ϴ�絼�缫�����絼�缫���뵽���ε絼��ֱ֧���У���ҺӦ�ܽ����缫��ȫ��û�������ε絼�ط��뵽���²��к��¡�10min�Ժ�ȡ��¼�絼��ֵ�������˲��ε絼���е���Һ�������������ں���35��ʱ����
��ȡ����Һһ���ַ��뵽�ྻ����IJ��ε絼��ֱ֧���У��ò�����Һ��ϴ�絼�缫�����絼�缫���뵽���ε絼��ֱ֧���У���ҺӦ�ܽ����缫��ȫ��û�������ε絼�ط��뵽���²��к��¡�10min�Ժ�ȡ��¼�絼��ֵ�������˲��ε絼���е���Һ�������������ں���35��ʱ���� ��
��
5) 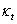 �IJ���������Һ��ȡ�����Ƶ�����������Һ10ml�����뵽�ྻ����IJ��ε絼��ֱ֧���У�ȡŨ����ͬ��NaOH��Һ10ml�����뵽ͬһ���ε絼�ز�֧���У�ע���ʱ������Һ��Ҫ������Ⱦ�����ྻ�ĵ絼�缫���뵽���ε絼��ֱ֧���У������ε絼�ط��뵽���²��к��¡�10min�Ժ��ں��²��н���֧���е���Һ��;��ȣ���ҺӦ�ܽ����缫��ȫ��û�������Һ��ͬʱ���������ʼ��ʱ��ע�����һ���������м䲻Ҫ��ͣ���ڵ�3minʱ��ȡ��Һ�絼��ֵ���Ժ�ÿ��3min��ȡһ�ε絼��ֵ����������30min��
�IJ���������Һ��ȡ�����Ƶ�����������Һ10ml�����뵽�ྻ����IJ��ε絼��ֱ֧���У�ȡŨ����ͬ��NaOH��Һ10ml�����뵽ͬһ���ε絼�ز�֧���У�ע���ʱ������Һ��Ҫ������Ⱦ�����ྻ�ĵ絼�缫���뵽���ε絼��ֱ֧���У������ε絼�ط��뵽���²��к��¡�10min�Ժ��ں��²��н���֧���е���Һ��;��ȣ���ҺӦ�ܽ����缫��ȫ��û�������Һ��ͬʱ���������ʼ��ʱ��ע�����һ���������м䲻Ҫ��ͣ���ڵ�3minʱ��ȡ��Һ�絼��ֵ���Ժ�ÿ��3min��ȡһ�ε絼��ֵ����������30min��
6) ���ں��²���35�档
7) ����35��ʱ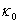 ���ڷ���絼�缫�����ε絼��ʱ��ע��絼�缫�Ľྻ�������ô�����Һ��ϴ�絼�缫��
���ڷ���絼�缫�����ε絼��ʱ��ע��絼�缫�Ľྻ�������ô�����Һ��ϴ�絼�缫��
8) ���ղ���5)����35��ʱ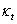 ��
��
9) ������ϣ�ϴ���������������缫��ȥ����ˮϴ��������ȥ����ˮ�б��档
5 ���ݼ�¼������
1) ���������ݼ�����ֵ�����±���
T=25��ʱ 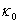 =2020us T=35��ʱ
=2020us T=35��ʱ 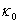 =1834us a=0.01955 mol?dm-3
=1834us a=0.01955 mol?dm-3

2) ��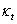 ��
��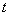 ͼ��
ͼ��
T=25��ʱ��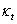 ��
��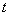 ͼ
ͼ
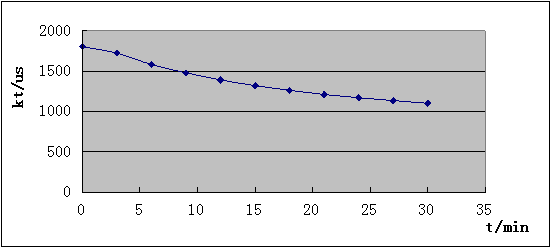
T=35��ʱ��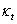 ��
��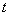 ͼ
ͼ
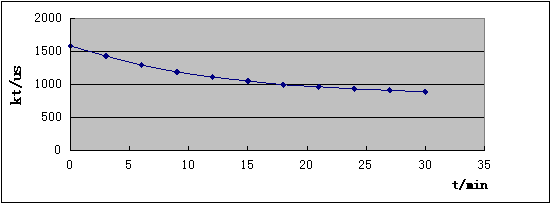
3) ��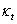 ��
��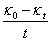 ��ͼ����һֱ�ߣ���б�ʼ�����¶���
��ͼ����һֱ�ߣ���б�ʼ�����¶���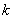 ��
��
T=25��

ֱ�߷���Ϊ��Y=9.4712x+856.80 б��K=9.4712 ��ʼŨ��a=0.01955
K1=1/(0.01955*9.4712)=5.4007 L/(min*mol)
T=35��ʱ
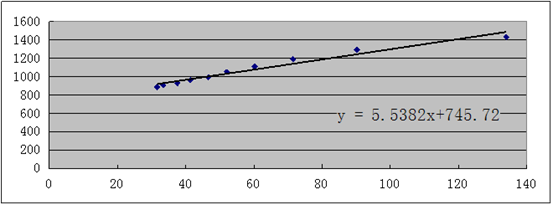
ֱ�߷���Ϊ��Y=5.5382x+745.72 б��K=5.5382 ��ʼŨ��a=0.01955
K2=1/(0.01955*5.5382)=9.2360 L/(min*mol) Y=5.253x+727.8
4) �����¶�T1��T2�µ�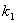 ��
��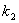 ��������
��������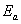 ��
��
Ea=R*ln(K1/K2)/(1/T2-1/T1)
={8.314*ln(5.4007/9.2360)/(1/308.15-1/298.15)} J/mol
=40.99kJ/mol
6.˼����
1) �ڱ�ʵ���У�ʹ��DDSJ-308�͵絼���Dz�����Һ�ĵ絼�ʣ����Բ����е缫������У����Ϊʲô��
��ʵ�ʼ���ʱ����ֻ����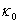 -
-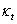 ����������������Ե�������ʱ��ƫ������ˡ�
����������������Ե�������ʱ��ƫ������ˡ�
2��Ϊʲô��ҺŨ��Ҫ�㹻С��
��ֻ����ϡ��Һ�У�ǿ����ʵ絼�ʲ���Ũ�ȳ����ȣ��Ӷ�����ͨ����絼�ʼ���ƽ�ⳣ����
3�����÷�Ӧ������ij�������ʼ�Ӳ���Ũ�Ƚ��ж���ѧ�о���Ӧ������Щ������
��Ũ�����Ӳ�����������֮���мĶ�Ӧ��ϵ�������������ڲ�����
�ڶ�ƪ��10.��������������Ӧ����ѧ�о�
ʵ��ʮ ��������������Ӧ����ѧ�о�
һ��ʵ��Ŀ����Ҫ��
�� 1�����ջ�ѧ����ѧ��ijЩ���
�� 2���ⶨ��������������Ӧ���ٶȳ�����
3�� ��Ϥ�絼���ǵ�ʹ�÷�����
����ԤϰҪ��
1�� �˽�絼���ⶨ��ѧ��Ӧ�ٶȳ�����ԭ����
2�� �˽�DDS-�͵絼���ǵ�ʹ�÷�����
����ʵ��ԭ����
�� ��������������Ӧ����ʽΪ��
�� CH3COOC2H5��Na����OH�� �T�T CH3COO����Na����C2H5OH
�� �ڷ�Ӧ�����У������ʵ�Ũ����ʱ����ı䣨ע��Na�������ڷ�Ӧǰ��Ũ�Ȳ��䣩�������������ij�ʼŨ��Ϊa���������Ƶij�ʼŨ��Ϊb����ʱ��Ϊtʱ�����������Ũ�Ⱦ�Ϊx����ʱ�̵ķ�Ӧ�ٶ�Ϊ��
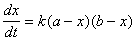 (10��1)
(10��1)
��ʽ�У�kΪ��Ӧ�����ʳ���������ʽ���ֿɵã�
 (10��2)
(10��2)
����ʼŨ��a=b��9��(1)ʽ��Ϊ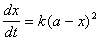 �����ֵã�
�����ֵã�
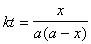 (10��3)
(10��3)
��ͬʱ�̸����ʵ�Ũ�ȿ��û�ѧ��������������������Ӧ�е�OH��Ũ�ȣ�Ҳ����������������Һ�ĵ絼����á��ڱ�ʵ�������Dz��ú�һ�ַ��������õ絼�����ⶨ��
�絼�ǵ��嵼�����������ȣ������ĵ������������ɵ����ڵ糡���˶���ʵ�ֵģ����������Һ�ĵ���������������������������Ǩ�ƵĽ�����絼L�ǵ���R�ĵ�����
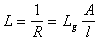
ʽ��AΪ����Ľ������lΪ����ij��ȣ�Lg�Ƶ絼�ʡ��������������ǣ���l=1m��A=1m2ʱ�ĵ絼����һ�ֽ�������һ���¶��£�Lg��һ���ġ��Ե������Һ��Lg�������¶��йأ���������Һ�е�����Ũ���йء����ж������Ӵ��ڵ���Һ�У�Lg�Ǹ�������Ǩ�����õ��ܺͣ�������Һ�����ӵ���Ŀ��������������Լ�����Ǩ�����йء��ڱ�ʵ���У����ڷ�Ӧ���ڽ�ϡ��ˮ��Һ�н��еģ����ǿ��Լٶ�CH3COONaȫ�����룬��Ӧǰ����Һ��������Ŀ������������ɲ��䣬������CH3COO����Ǩ���ʱ�OH����Ǩ����С�����ŷ�Ӧ�Ľ��У�OH�����ϼ��٣�CH3COO����Ũ�Ȳ������ӣ�����ϵ�絼��ֵ����½�����һ����Χ�ڣ�������Ϊ��ϵ�ĵ絼�ʵļ�������CH3COO����Ũ��x�����������ȣ���t=tʱ
 (10��4)
(10��4)
ʽ��L0Ϊ��ʼʱ�ĵ絼�ʣ�LtΪtʱ�ĵ絼�ʡ���t=t¥ʱ��Ӧ����CH3COO����Ũ��Ϊa������
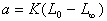 (10��5)
(10��5)
ʽ��L¥����Ӧ����ʱ�ĵ絼�ʣ�KΪ��������������4������5�����루3��ʽ�ã�
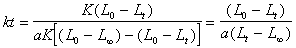
��д�ɣ�
 (10��6)
(10��6)
�� 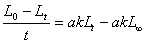 (10��7)
(10��7)
��ֱ�߷��̣�6����֪��ֻҪ�ⶨ��L0��L¥�Լ�һ��Ltֵ������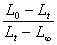 ��t��ͼ��Ӧ��һֱ�ߣ�ֱ�ߵ�б�ʾ��Ƿ�Ӧ�ٶȺͳ�ʼŨ��a�ij˻���k�ĵ�λΪdm3·mol-1·min-1��
��t��ͼ��Ӧ��һֱ�ߣ�ֱ�ߵ�б�ʾ��Ƿ�Ӧ�ٶȺͳ�ʼŨ��a�ij˻���k�ĵ�λΪdm3·mol-1·min-1��
��Ӧ�Ļ�ܿɸ��ݰ�������˹��ʽ���㣺
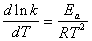 (10��8)
(10��8)
���ֵã� 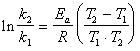 (10��9)
(10��9)
ʽ��k1��k2�ֱ��Ӧ���¶�T1��T2�ķ�Ӧ���ʳ�����RΪ���峣����EaΪ��Ӧ�Ļ�ܡ�
�ġ�������ҩƷ��
�� DDS���͵絼���� 1̨ �絼�� 1ֻ
���²� 1�� 100mL���¼���Ӧ�� 1��
0.5mL��Һ�� 1֧ 100mL��Һ�� 1֧
50mL���ձ� 1�� 50mL�ζ��� 1֧
250mL��ƿ 3�� ��� 1��
������ 1ֻ CH3COOC2H5�Լ�����������
NaOH���������� ��ָ̪ʾ����Һ
�塢ʵ�鲽�裺
1�����²�ʹ�������25��±0.2�档
2���絼���ǡ����ݸ�¼���絼���ǵ�ʹ�á��Ե絼���ǽ���0�㼰���̶�У���������������õ絼�缫�ij�����������ť���������λ�á�
3��NaOH��Һ�����ƣ��������£�
��һ��С�ձ�����������ŨNaOH��Һ����1000ml�Ĺ��ƿװ��Լ900ml������ˮ������ѡ��ʵ�������IJ����缫����ˮ�У�
��1�����ѡ�õ絼���Dz�������Ž��������£���μ���ŨŨNaOH��Һ��L=1300��1400��S/cm
��2�����ѡ�����ӷ����Dz�������Ž��������£���μ���ŨŨNaOH��Һ��PH=12.00���ҡ�
4��NaOH��Һ�ĵζ����������£�
�����ƺõ�NaOH��Һ���˹��ֶ��ζ��ܺͷ�ָ̪ʾ���������½���Ũ�Ȳⶨ���ظ��������ϣ�ȡƽ��ֵ��
5��L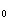 ����PH
����PH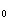 ���IJⶨ��������25.00�������30.00�棩
���IJⶨ��������25.00�������30.00�棩
ȡ100ml�����ҵζ��õ�NaOH��Һ���ں��¼���Ӧ���У�����ϴ��������ˮ�IJ����缫������10���ӣ��ȵ絼���ϵĶ����ȶ���ÿ��1���Ӷ�ȡһ�����ݣ��ⶨ����ƽ�е����ݡ�
6��L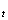 ����PH
����PH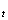 ���IJⶨ��������25.00�������30.00�棩
���IJⶨ��������25.00�������30.00�棩
���L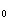 ����PH
����PH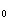 ���IJⶨ��ʹ��С��������Һ����ȡ��������������������������ڲ����ף�����������ȫ��������Һ�У���Ҫ�����ڲ������ڱ��ϣ�����Ũ�Ȳ����ŵ�һ��ʱ�������ʱ������ƽ�ȱ仯���������һ�����ݣ��Ժ�ÿ��1���Ӷ�һ������15���Ӻ�ÿ��2���Ӷ�һ���������е�35���Ӻ������
���IJⶨ��ʹ��С��������Һ����ȡ��������������������������ڲ����ף�����������ȫ��������Һ�У���Ҫ�����ڲ������ڱ��ϣ�����Ũ�Ȳ����ŵ�һ��ʱ�������ʱ������ƽ�ȱ仯���������һ�����ݣ��Ժ�ÿ��1���Ӷ�һ������15���Ӻ�ÿ��2���Ӷ�һ���������е�35���Ӻ������
7��������Ҫ������������
8��������5��6��7�ڵڶ����¶��½��в�����������30.00�������35.00�棩
����ʵ��ע�����
1�� NaOH��Һ�������������ǰӦԤ�Ⱥ��¡�
2�� ��ϴ���缫ʱ��������ֽ���õ缫�ϵIJ��ڡ�
�������ݼ�¼��������
1��NaOH��Һ�ĵζ����ݣ�
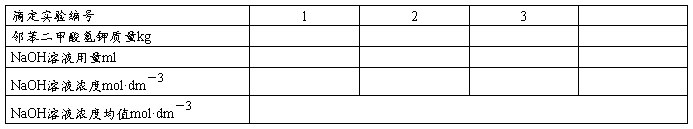
2��L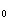 ����PH
����PH ����L
����L ����PH
����PH ���IJⶨ�� ʵ���¶ȣ� ��
���IJⶨ�� ʵ���¶ȣ� ��
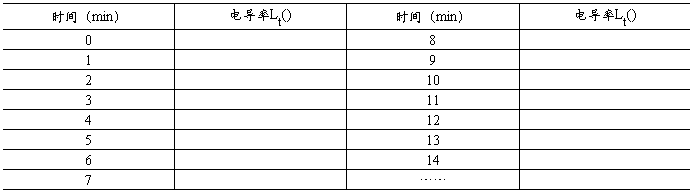
3������ǡ���Ĺ�ϵʽ��ͼ��һֱ�ߣ�������б����Ӧ���ʳ���k��
4����k25��k30�����ݰ�������˹��ʽ
�� 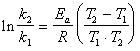
�����Ӧ�Ļ��Ea��
�ˡ�˼���⣺
1. ��ѧ��Ӧ����ѧ�о����������棬�ֱ�Ϊ��
��
2. ��ѧ��Ӧ����ѧ��������Ҫ������ʲô��һ���������һ������Ӧ���ȱ�ʵ��ȷ����
��
3. ��Һ���ѧ��Ӧʵ���о�����Ҫ��������ǣ�
��
4. ��ѧ��Ӧ�п�������Ϊ����ȷ���������ϱ仯������Ũ�Ȼ�������������ѧ������Ӧ�ù�ע��������Ҫʱ�������:
��.
5. ���ڶ���ѧ�о��У��������������������ѡ������Щ����Ŀ��ǣ�
�𣺣�1����Ӧǰ����ϵ���������ı仯�dz�������
��2���������Ũ�ȳ����Թ�ϵ������������Ϊ��ѣ�
��3���������Ũ�Ȳ������Թ�ϵ�ķ�����������Ϊ��
6. ���ݾ��м�Ӧ�����Ļ�ѧ��Ӧ����ѧ�������������ļ���ȷ����Ӧ���������ݴ���������
���ַ������ַ�����˥�ڷ����ı��ʼ����Ũ�ȷ���
7. ����ѧʵ�飬һ�������ΪʲôҪ�ں��������½��У�
�𣺲�ͬ�¶��µķ�Ӧ�ٶȲ�һ������Ӧ���ʳ������¶��йأ��絼�ʵ���ֵ���¶�Ҳ�йأ�����Ҫȷ���ж���ѧ�����������ں��������½��С�
8. 1999�꣬������A.H.Zewail��ŵ�������Ļɾ��ǣ�
��: ���뼤�⼼���о����컯ѧ��Ӧ���̺���̬��
����
����Һ����ѧ��Ӧ����ѧʵ���о�
�����������ɲο������еĽ���ժҪ��������ƴ�Ӷ��ɣ����ο�����ϸ�����뿴�й����ϣ�
��ѧ��Ӧ����ѧ�о����������棺
��1����ѧ��Ӧ�����о�����2����ѧ��Ӧ�����������̣��о���
��ѧ��Ӧ�����о�����㣺
���Dz���һ������Ũ����ʱ��ı仯����������Ũ������ȷ��ϵ����������ʱ��ı仯���ߡ�
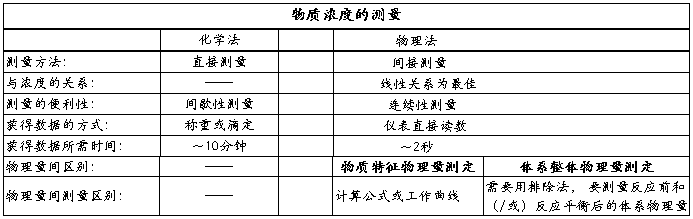
������Ҫ��ʱ����
��ѧ��Ӧ�п��������еļ��죬Ҳ�еļ�������Բ�ͬ�����������Ҫʹ�ò�ͬ��ʵ�鷽���Ͳ��������������ѡ��ʵ�鷽���Ͳ�������ʱ����Ҫ���ǵ�����Һ�෴Ӧ����ѧʵ���о���������Ҫע�����Ҫʱ����
1�� ��ѧ��Ӧ�յ�ʱ��t(i)
t(i)���������������
��1�� �����������ʻ�Ϻ�ѧ��Ӧ���ܽ��У��ӻ�Ͽ�ʼ����ϵ��Ͼ���һ������Ҫ��ʱ�䣻
��2�� ��ѧ��Ӧ�������������⡢�硢�š��������ߵ��ⳡ��������У���������������ѧ��Ӧ��ʼ����Ҫ��ʱ�䡣
2�� ���ݲ���ʱ��t(m)
t(m)���������������
��1�� ʵ�������������Ӧʱ�䣺�����Ĵ�����������Ԫ�����ܼ�ת�Ƶ���������Ũ�Ƚϴ����Һ��ʱ�����������ȶ��ɿ���������Ҫ��ʱ�䣻
��2�� �����ڽ��еĻ�ѧ��Ӧ��ϵ��ȡ��һ���֣������еĻ�ѧ��Ӧֹͣ���Ӳ�����ʼ����ѧ��Ӧ��ȫֹͣ������Ũ�Ȳ�����ʱ��仯������Ҫ��ʱ�䡣
3�� ��ѧ��Ӧʱ�䣨ͨ��ȡ����Ũ�ȵİ�˥��t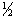 ��
��
���ջ�ѧ����ʽ�����ʺ���������ٵ����������ڷ�Ӧ�����ĵ�һ������Ҫ��ʱ�䡣
Ϊ���ܹ���ʵ���в������ɿ���ȷ�����С�Ķ���ѧ���ݣ���������ʱ��֮������������µ�������
t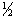 ��t(i) �� t
��t(i) �� t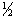 ��t(m)
��t(m)
���t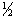 ��С���ͱ�������Ӧ�����ʻ�Ϸ������ԥ����ͬʱ�и�ʱ��ֱ��ʵ�ʵ�������������ʹ���������ڲ�ͬ��ѧ��Ӧ���ʲⶨ�Ķ���ʵ�鷽����
��С���ͱ�������Ӧ�����ʻ�Ϸ������ԥ����ͬʱ�и�ʱ��ֱ��ʵ�ʵ�������������ʹ���������ڲ�ͬ��ѧ��Ӧ���ʲⶨ�Ķ���ʵ�鷽����
��1�� �����ʵ���������
����Ӧ��t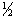 �������ӣ������ϣ���ͨ����������
�������ӣ������ϣ���ͨ����������
��2�� ���ٻ�Ϸ�
1923����Hartridge��Roughton��չ�����ġ�
t(i)=0.5��1ms ���������� t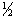 =101��103ms��
=101��103ms��
��3�� ��ԥ�����ɳڷ���Ծ�䷨
��������Manfred ��Eigen ����ͬ�����ڸ�͢���о���չ�����ġ�
�ڸ�ʵ�鷽���У��������ʻ��ʱ�䣬�ڷ�Ӧ��ϵ���ﻯѧƽ����̵�ʱ�����ڣ��������⡢�硢�š����ߵȶ������������ı�ԭ��ѧƽ����ϵ��������ʹ��ƫ�뻯ѧƽ�⣬�þ�ƽ��״̬����ƽ��״̬�仯����Ҫ��ʱ������ʾ��ѧ��Ӧ���ʡ�
t(i)��1��s
��4�� ���巨
���巨���������о��ķ�Ӧ��ϵ�б���ŷ��䣨�⡢�����ߡ�X���ߡ����⣩��������ӣ�ͨ���ǵ��ӣ��ɵ��Ӽ��������������������»������ʣ��缤���ĵ���̬�����ɻ����������ӵȣ���������ѧ��Ӧ�����ڹ⻯ѧ�ͷ��仯ѧ�о���Χ��
���ʹ��ǿ�Ŀɼ���������߷��䣬ʹ��Ӧ��ϵ���������ɻ�����Ӽ���̬���÷���ͨ����Ϊ������ֽ⡱����1949����Norrish ��Porter �ڽ��Ŵ�ѧ�о������ġ�
��������ƣ� t(i)=10-6s
���ڼ��⣺ t(i)=10-9s
�������⼼�����⣺ t(i)=10-12s
���ʹ�õ�������X�������䷴Ӧ��ϵ��ʹ��ϵ�ڵ����ʷ��ӵ��룬����Ϊ��������⡱���������о����ӻ����ʵķ�Ӧ�������Բ����ܼ������ӣ���ˮ�����ӣ�
��5�� �����ڷ�������������
�����ڷ�ʵ�����û�ѧ��ӦӰ�����ߵ���״��Ƶ�ʵķ�������H. Gutowsky����ͬ������1953��ͺ˴Ź�����������ģ����ַ�������ں˴Ź����������ߣ���ʱҲ���ڵ������������ף�������ԭ���Ͽ��������κ����ߣ��ؼ�Ҫ�������㹻�ߵķֱ��ʡ�
���µĻ�ѧ�仯��
����ת�ƣ�Cu+ +Cu2+ ���� Cu2+ + Cu+ 63Cu�˴Ź���
����ת�ƣ�H2O +OH�C ���� HO�C + H2O H�˴Ź���
CH3OH + OH�C ����CH3O�C+ H2O H�˴Ź���
����仯�������� �ţ�����ʽ������ʽ H�˴Ź���
����������ϵ�ͷ�����t(i)= 0(s)��t(m)��������������������������ͨ���ı���ϵ���¶����ı�t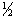 ��
��
�����ϵ�¶Ƚϸߣ�t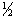 ��t(m)���������ڲ���ʱ���ڸ��ٿ��ٱ仯������״̬����ȷ����̬������Ƶ�ʷ壬��t(m)ʱ����õ�����������̬��ƽ���������ֻ��һ�������ˣ�
��t(m)���������ڲ���ʱ���ڸ��ٿ��ٱ仯������״̬����ȷ����̬������Ƶ�ʷ壬��t(m)ʱ����õ�����������̬��ƽ���������ֻ��һ�������ˣ�
�����ϵ�¶����ͣ�t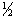 ���������̬���ȶ�����ʱ��䳤�������ͻ�Ӳ��ֱܷ�������̬��Ϊ���Էֱ�������̬��
���������̬���ȶ�����ʱ��䳤�������ͻ�Ӳ��ֱܷ�������̬��Ϊ���Էֱ�������̬��
�����ϵ�¶��㹻��ʱ��t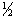 ��t(m)�������ܹ��ڲ���ʱ���ڷֱ���������״̬����ȷ����̬������Ƶ�ʷ壬�ͻ�õ��������շ��ˡ�
��t(m)�������ܹ��ڲ���ʱ���ڷֱ���������״̬����ȷ����̬������Ƶ�ʷ壬�ͻ�õ��������շ��ˡ�
��ͬ����ϵ�õ�������̬����Ƶ�ʷ�ʱ����Ҫ���͵��¶Ȳ�ͬ�����ɱ���Ϊ�仯���ʵIJ�ͬ��
��6�� ������µĽ���������������������μ��йط��ӷ�Ӧ��̬ѧ���鼮��
��ѧ��Ӧ����ϵ��������Ӧ����
��ѧ��Ӧ����ϵ���뷴Ӧ����֮����ȫ��������ͬ�ĸ����ѧ��Ӧ����ϵ���������ʽṹ�йأ���Ӧ����������ϵ������Ӧ����������Ũ�ȶԷ�Ӧ����Ӱ��̶ȵ�����ָ�ꡣ���ھ��������ۻ�ѧ��Ӧ��˵�������ѧ��Ӧ����ϵ���������뷴Ӧ������������ȣ�Ҳ�Ǽ���żȻ���ɺϣ�û�б�Ȼ����ϵ��
�������۵Ļ�Ԫ��Ӧ����ѧ��Ӧ����ϵ���뵥��Ӧ�ķ�Ӧ����֮�䱻��Ϊ�ж�Ӧ��ϵ��
��Ԫ��Ӧ�����������ö��ɡ����ۿ�����ԭ��
��Ԫ��Ӧ A+B 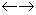 C+D
C+D
�������ö��� r+=k+CACB
r��=k��CCCD
�ۿ�����ԭ�� r= r+�Dr��= k+CACB�Dk��CCCD
ֻ�л�ѧ��Ӧ�տ�ʼ���õ�һС��ʱ���ڣ�����C��D��Ũ�Ⱥ�С������Ӧ�����ʼ������Ժ��Բ���ʱ
r(t®0)�� r+�� k+CACB
�ɴ˿ɼ������м�Ӧ�����Ļ�ѧ��Ӧ����ѧ���������ʹ�ǻ�Ԫ��Ӧ��Ӧ��Ҳ�ǽ��ƵĽ������
���м�Ӧ�����Ļ�ѧ��Ӧ�Ķ���ѧ����
�μ���������ѧ�����²ᣩ���ײʵȣ��ߵȽ��������磬P700��734
����Һ����ද��ѧʵ���о�������Ҫ����
1�� ��������ʹ�õĻ�ѧ��Һ����������Ҫ�ⶨ��ȷŨ�ȣ�
2�� ���е���ϵ��Ҫ������ѧ��Ӧ��ʼǰij����Һ����ʼ������Z(t=0)��
3�� ������ѧ��Ӧ��ʼ������Ũ��C��ʱ��t�ı仯����������Ũ���йص�������
Z��C����ʱ��t�ı仯����
4�� ���е���ϵ��Ҫ������ѧ��Ӧ����ƽ���Ժ����Һ��������Z(t=��)��
5�� ���ݾ��м�Ӧ�����Ļ�ѧ��Ӧ�Ķ���ѧ��������2��3��4���������Ľ�������Ӧ�Ĺ�ʽ�̣�ȷ����Ӧ����n��
6�� ����ijȷ���¶��µĻ�ѧ��Ӧ���ʳ���k��
7�� �仯��ͬ���¶��������вⶨ����k��T�Ĺ�ϵ���㻯ѧ��Ӧ���Ea��
�뻯ѧ��Ӧ����ѧ�����йص�ŵ������
�ο����ϣ�
1����������ѧ�����²ᣩ���ײʵȣ��ߵȽ���������
2����������ѧ��(��)V.����µ��� �ߵȽ��������磬 1983��7��
3����չ��21���͵Ļ�ѧ�������ɵ����࣬��ѧ��ҵ�����磬20##��5��
