
1、欲要比较各种电解质的导电能力的大小,更为合理应为 ( )
A、 电解质的电导率值
B、 电解质的摩尔电导率值
C、 电解质的电导值
D、 电解质的极限摩尔电导率值
2、在一般情况下,电位梯度只影响 ( )
A、离子的电迁移率 B、离子迁移速率 C、电导率 D、离子的电流分数
3、在CuSO4溶液中用铂电极以0.1 A的电流通电10 min,在阴极上沉积的铜的质量是: ( )
A、19.9 mg B、 29.0 mg C、 39.8 mg D、 60.0 mg
4、在饱和 AgCl 溶液中加入 NaNO3,AgCl 的饱和浓度如何变化 ? ( )
A、 变大
B、 变小
C、 不变
D、 无法判定
5、当一定的直流电通过一含有金属离子的电解质溶液时,在阴极上析出金属的量正比于: ( )
A、阴极的表面积 B、电解质溶液的浓度 C、通过的电量 D、电解质溶液的温度
6、在298 K的无限稀的水溶液中,下列离子摩尔电导率最大的是: ( )
A、 CH3COO - B、 Br – C、 Cl - D、 OH -
7、按物质导电方式的不同而提出的第二类导体,下述对它特点的描述,哪一点是不正确的?( )
A、其电阻随温度的升高而增大 B、其电阻随温度的升高而减小
C、其导电的原因是离子的存在 D、当电流通过时在电极上有化学反应发生
8、用同一电导池分别测定浓度为 0.01 mol·kg-1和 0.1 mol·kg-1的两个电解质溶液,其电阻分别为 1000 W 和 500 W,则它们依次的摩尔电导率之比为 ( )
A、 1 : 5
B、 5 : 1
C、 10 : 5
D、 5 : 10
9、室温下无限稀释的水溶液中,离子摩尔电导率最大的是: ( )
A、 ?La3+ B、½Ca2+ C、NH4+ D、 OH -
10、浓度为 1.0 mol·dm-3 的强电解质溶液,它的摩尔电导率数值近似于: ( )
A、 与电导率相等 B、是电导率的 103倍
C、是电导率的 10-3倍 D、 是电导率的 102倍
11、Al2(SO4)3的化学势 m 与Al3+ 和 SO 离子的化学势 m + ,m-- 的关系为: ( )
离子的化学势 m + ,m-- 的关系为: ( )
A、 m = m + + m-- B、 m = 3m + + 2m--
C、 m = 2m ++ 3m--- D、 m = m +·m---
12、对于0.002 mol·kg-1 的Na2SO4溶液,其平均质量摩尔浓度m±是: ( )
A、3.175×10-3 mol·kg-1 B、2.828×10-3 mol·kg-1 C、1.789×10-4 mol·kg-1 D、4.0×10-3 mol·kg-1
13、水溶液中氢和氢氧根离子的电淌度特别大,究其原因,下述分析哪个对? ( )
A、 发生电子传导
B、 发生质子传导
C、 离子荷质比大
D、 离子水化半径小
14、用0.1 A的电流,从200 ml 浓度为0.1 mol·dm-3的AgNO3溶液中分离Ag,从溶液中分离出一半银所需时间为:( ) A、10 min B、 16 min C、 100 min D、 160 min
15、对于德拜-休克尔理论,下述哪一点说法是正确的?( )
A、认为离子严格讲不是独立单元 B、只适用于饱和溶液 C、只适用于过渡元素的离子 D、只适用于水溶液
16、电解质溶液中离子迁移数 (ti) 与离子淌度 (Ui) 成正比。当温度与溶液浓度一定时,离子淌度是一定的,则 25℃时,0.1 mol·dm-3 NaOH 中 Na+的迁移数 t1 与 0.1mol·dm-3 NaCl 溶液中 Na+ 的迁移数 t2,两者之间的关系为 ( )
A、 相等 B、 t1> t2 C、 t1< t2 D、 大小无法比较
17、在10 cm3 浓度为 1 mol·dm-3 的KOH溶液中加入10 cm3水,其电导率将: ( )
A、 增加
B、 减小
C、 不变
D、 不能确定
其摩尔电导率将 ( )
A、 增加
B、 减小
C、 不变
D、 不能确定
18、在HAc解离常数测定的实验中,总是应用惠斯顿电桥。作为电桥平衡点的指零仪器,结合本实验,不能选用的是:( )
A、 耳机 B、 电导率仪 C、阴极射线示波器 D、直流桥流计
19、0.3 mol·kg-1 Na2HPO4水溶液的离子强度是: ( )
A、 0.9 mol·kg-1 B、 1.8 mol·kg-1 C、 0.3 mol·kg-1 D、1.2 mol·kg-1
20、对于给定离子B,应当满足下列条件中的哪几个,才能使离子的摩尔电导率lm,B和离子淌度UB为常数。(a)强电解质溶液;(b)无限稀释溶液;(c)一定温度下;(d)一定溶剂下;(e)一定的共存离子。 ( )
A、a, b, c, d B、a, b, c, d, e C、b, c, d D、 b, c, d, e
21、下列物理量除哪一个外,均与粒子的阿伏加德罗数有关: ( )
A、法拉第 B、标准状态下22.4 dm3气体
C、 摩尔 D、库仑
22、有一ZnCl2水溶液,m=0.002 mol·kg-1 ,g±=0.83,则a±为: ( )
A、 1.66×10-3 B、 2.35×10-3 C、 2.64×10-3 D、 2.09×10-4
23、在浓度为 c1的 HCl 与浓度 c2的 BaCl2混合溶液中,离子迁移数可表示成: ( )
A、 lm(H+)/[lm(H+) + lm(Ba2+) + 2lm(Cl-)] B、 c1lm(H+)/[c1lm(H+)+ 2c2lm(½ Ba2+)+ (c1+ 2c2)lm(Cl-)] C、 c1lm(H+)/[c1lm(H+) + c2lm(Ba2+) + lm(Cl-)] D、 c1lm(H+)/[c1lm(H+) + 2c2lm(Ba2+) + 2c2lm(Cl-)]
24、下面哪一个公式表示了离子独立移动定律 ( ) 、
A、 a = Lm/ L B、l
B、l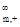 = t
= t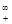 L
L C、l
C、l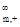 ,+= L
,+= L -l
-l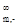 D、 Lm= k / c
D、 Lm= k / c
25、在其它条件不变时,电解质溶液的摩尔电导率随溶液浓度的增加而 ( )
A、 增大
B、 减小
C、 先增后减
D、 不变
26、18℃时,纯水的 4.89×10-2
4.89×10-2  ,此时水中m(H+)= m(OH-)=7.8×10-8 mol·kg-1,则18℃时纯水的电导率k为: ( )
,此时水中m(H+)= m(OH-)=7.8×10-8 mol·kg-1,则18℃时纯水的电导率k为: ( )
A、3.81×10-6 S·m-1 B、3.81×10-8 S·m-1 C、3.81×10-7 S·m-1 D、3.81×10-5 S·m-1
27、不同浓度醋酸溶液的电导率k、摩尔电导率Lm和无限稀释时的摩尔电导率数据如下:
m/(mol·kg-1) k Lm 
1 k1 Lm,1 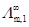
0.5 k2 Lm,2 
0.1 k3 Lm,3 
0.05 k4 Lm,4 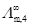
下列关系中正确的是: ( )
A、 B、
B、
C、 D、
D、
28、在无限稀释的电解质溶液中,正离子淌度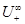 ,正离子的摩尔电导率
,正离子的摩尔电导率 和法拉第常数F之间的关系是: ( ) A、 z+
和法拉第常数F之间的关系是: ( ) A、 z+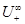 /
/ =F B、 z+
=F B、 z+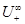
 =F C、 z+
=F C、 z+
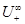 F = 1 D、
F = 1 D、  / z+
/ z+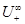 =F
=F
29、 zB、rB及 cB分别是混合电解质溶液中 B 种离子的电荷数、迁移速率及浓度,对影响 B 离子迁移数 (tB) 的下述说法哪个对? ( )
A、 │zB│ 愈大, tB愈大
B、 │zB│、rB愈大,tB愈大
C、 │zB│、rB、cB愈大 ,tB愈大
D、 A、B、C 均未说完全
30、1 mol·kg-1 K4Fe(CN)6 溶液的离子强度为 : ( )
A、 10 mol·kg-1 B、 7 mol·kg-1
C、 4 mol·kg-1 D、 15 mol·kg-1
31、测定溶液的电导是以溶液中通过电流时所表现的电阻大小来进行换算的。实验测定时所用的电源是: ( )
A、普通家用交流电 B、低压直流电 C、超高频交流电 D、中频交流电
32、0.1 mol·kg-1 CaCl2水溶液,其平均活度系数g±=0.219,则离子平均活度a±为: ( )
A、 3.476×10-4 B、 3.476×10-2 C、 6.964×10-2 D、 1.385×10-2
33、电导测定应用广泛,但下列问题中哪个是不能用电导测定来解决的?( )
A、求难溶盐的溶解度 B、求弱电解质的解离度 C、求平均活度系数 D、测电解质溶液的浓度
34、浓度均为 m 的不同价型电解质,设 1-3 价型电解质的离子强度为 I1,2-2 价型电解质的离子强度为 I2,则 ( ) A、 I1 < I2 B、 I1 = I2
C、 I1 = 1.5I2 D、 无法比较 I1和 I2大小
35、 NaCl 稀溶液的摩尔电导率 Lm与 Na+、 Cl-离子的淌度(Ui)之间的关系为 : ( )
A、 Lm = U+ + U- B、Lm = U+/F + U-/F
C、Lm = U+F + U-F D、 Lm= 2 (U+ + U-)
36、离子电迁移率的单位可以表示成 ( )
A、 m·s-1
B、 m·s-1·V-1
C、 m2·s-1·V-1
D、 s-1
37、25℃时,Lm(LiI)、lm(H+)、Lm(LiCl) 的值分别为 1.17×10-2,3.50×10-2 和 1.15×10-2 S·m2·mol-1。 LiCl 中的 t+为 0.34,当假设其中的电解质完全电离时, HI 中的 t+为 : ( )
A、 0.18
B、 0.82
C、 0.34
D、 0.66
38、德拜-休克尔理论及其导出的关系式是考虑了诸多因素的,但下列因素中哪点是它不曾包括的?( )
A、强电解质在稀溶液中完全解离 B、每一个离子都是溶剂化的
C、每一个离子都被电荷符号相反的离子所包围 D、溶液与理想行为的偏差主要是由离子间静电引力所致
39、Ostwald稀释定律表示为: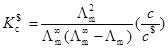 ,它适用于: ( )
,它适用于: ( )
A、非电解质溶液 B、强电解质溶液 C、解离度很小的弱电解质 D、无限稀释的电解质溶液
40、298 K时,无限稀释的 NH4Cl 水溶液中正离子迁移数 t+= 0.491。已知L (NH4Cl) = 0.0150 S·m2·mol-1 ,则: ( )
(NH4Cl) = 0.0150 S·m2·mol-1 ,则: ( )
A、 l (Cl-) = 0.00764 S·m2·mol-1 B、 l
(Cl-) = 0.00764 S·m2·mol-1 B、 l (NH
(NH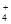 ) = 0.00764 S·m2·mol-1
) = 0.00764 S·m2·mol-1
C、 淌度 U = 737 m2·s-1·V-1 D、 淌度 U
= 737 m2·s-1·V-1 D、 淌度 U = 7.92×10-8 m2·s-1·V-1
= 7.92×10-8 m2·s-1·V-1

1、测定电解质溶液电导时必须采用________电源,以防止________。
2、现有不同浓度的KCl溶液,若c1>c2,则摩尔电导率较小的是___________浓度的溶液。
3、1 mol·kg-1 K4[Fe(CN)6]溶液的离子强度为:______________________。
4、某溶液含 LaCl3和 NaCl 均为 0.025 mol·kg-1,则其离子强度为___________ mol·kg-1。
5、浓度分别为0.001,0.01,0.1和1.0 mol·dm-3的四种NaCl溶液,其中___________mol·dm-3溶液的电导率最大。
6、Al2(SO4)3的化学势m 与Al3+ 和SO42- 离子的化学势m+,m - 的关系为:__________________________。
7、在25℃时,0.1 mol·dm-3 KOH溶液中,K+ 的迁移数 t1 与0.1 mol·dm-3 KCl溶液中K+的迁移数t2,比较两者之间的大小为______________。
8、YHSO4的摩尔电导率 与Y2SO4和H2SO4的摩尔电导率
与Y2SO4和H2SO4的摩尔电导率 和
和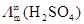 的关系为:________________________________________。
的关系为:________________________________________。
9、有下述电解质溶液: A、 0.01 mol·kg-1 KCl B、0.01 mol·kg-1 CaCl2 C、0.01 mol·kg-1 LaCl3 D、 0.001 mol·kg-1 KCl
其中平均活度系数最大的是:( ); 最小的是:( )。
10、在其他条件不变时,电解质溶液的摩尔电导率随溶液浓度的增加而__________________(填入增大、减小、先增后减)。
11、离子迁移率的单位是____________________。
12、水溶液中氢和氢氧根离子的电迁移率特别大,是因为通过____________传导。
13、AgCl在: ⑴ 0.1 mol·dm-3 NaNO3;⑵ 0.1 mol·dm-3 NaCl;⑶ H2O;⑷ 0.1 mol·dm-3 Ca(NO3)2;⑸ 0.1 mol·dm-3 NaBr中,溶解度递增次序为____________________________________。
14、在希托夫法测定迁移数的实验中,用Ag电极电解AgNO3溶液,测出在阳极部AgNO3的浓度增加了x mol,而串联在电路中的Ag库仑计上有y mol的Ag析出,则Ag+的迁移数为___________________。
15、在HCl浓度为c1与BaCl2浓度为c2的混合溶液中,若已知 (H+)、
(H+)、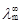 (K+)、
(K+)、 (Cl - ),则氢离子迁移数可表示成: ______________________________________。
(Cl - ),则氢离子迁移数可表示成: ______________________________________。
16、298 K时,无限稀释的NH4Cl水溶液中,正离子迁移数t+=0.491。已知 0.0150
0.0150  ,则Cl-离子的电迁移率
,则Cl-离子的电迁移率 ________________________。
________________________。
17、试完成下列原电池与电解池电极名称比较

18、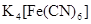 的摩尔电导率与其离子的摩尔电导率的关系是:________________________________。
的摩尔电导率与其离子的摩尔电导率的关系是:________________________________。
19、(1) 定温下,比较 H+,? La3+,OH -,½ SO 这四种离子在无限稀释水溶液条件下的摩尔电导率,哪个最大?
这四种离子在无限稀释水溶液条件下的摩尔电导率,哪个最大?
(2) 相同温度下,各种不同钠盐的水溶液中,钠离子的迁移数是否相等?
20、同样浓度的NaCl,CaCl2,LaCl3,CuSO4四种不同的电解质溶液,其中离子平均活度系数g±最大的是____________溶液。

1、AgCl 在 25℃的水溶液中的溶度积 Ksp = 1.83×10-10,在含有 0.01 mol·kg-1KNO3的水溶液中的饱和溶液的质量摩尔浓度为多少? 已知: A = 0.509 (mol·kg-1) -1/2
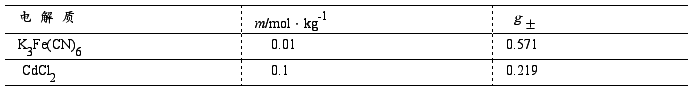
2、分别计算下列两个溶液的平均质量摩尔浓度 m± ,离子的平均活度 a± 以及电解质的活度aB
3、25℃时,KCl 和 NaNO3溶液的无限稀释摩尔电导率及离子的无限稀释迁移数如下:
L /( S·m2·mol-1) t¥,+
/( S·m2·mol-1) t¥,+
KCl 1.4985 × 10-2 0.4906
NaNO3 1.2159 × 10-2 0.4124
计算: (1) 氯化钠溶液的无限稀释摩尔电导率L (NaCl)
(NaCl)
(2) 氯化钠溶液中 Na+ 的无限稀释迁移数 t¥(Na+)和无限稀释淌度U¥(Na+)。
4、298 K 时,某溶液含 CaCl2的浓度为 0.002 mol·kg-1,含 ZnSO4的浓度亦为0.002 mol·kg-1,试用德拜-休格尔极限公式求 ZnSO4的离子平均活度系数。
已知: A = 0.509(mol·kg-1) -1/2

1、在一定温度下稀释电解质溶液,摩尔电导率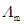 肯定会增大,而电导率k值的变化则不一定。这种说法对吗?为什么?
肯定会增大,而电导率k值的变化则不一定。这种说法对吗?为什么?
2、画出下列电导滴定的示意图
(1) 用 NaOH 滴定 C6H5OH
(2) 用 NaOH 滴定 HCl
(3) 用 AgNO3滴定 K2CrO4
(4) 用 BaCl2滴定 Tl2SO4
3、试写出在一定温度下,Al2(SO4)3溶液中Al2(SO4)3的整体活度a{Al2(SO4)3},a±,g±与Al2(SO4)3的质量摩尔浓度m之间的关系式。
4、在迁移数测定装置中,电解在100 g水里含有0.650 g NaCl的溶液。利用银作阳极,把放电的Cl - 去掉而变为AgCl固体。电解后,在阳极部的80.09 g溶液中含有NaCl 0.372 g,并且在串联连接的银量计上析出的银为0.692 g,试从这些结果求在NaCl溶液中Na+ 及Cl- 的迁移数。
5、当温度和浓度为定值时,在 KNO3和 K4Fe(CN)6水溶液中,K+离子的迁移数是否相同 ?
6、已知在0.01 mol·dm -3的KNO3溶液(1)中,平均离子活度系数g±(1)=0.916,在0.01 mol·dm -3的KCl溶液(2)中,平均离子活度系数g±(2)=0.922,假设g (K+)= g (Cl -),求在0.01 mol·dm -3的KNO3溶液中的g (NO3 -)。
7、一定温度下,给定离子B在一定溶剂的无限稀溶液中的摩尔电导率 与电迁移率
与电迁移率 都是常数,对吗?为什么?
都是常数,对吗?为什么?
8、在电解质溶液中,存在下述关系: ,说明电解质的化学势为电解后正负离子化学势的加和值。但化学势为强度性质,应不具有加和性质,如何解释上述关系式?
,说明电解质的化学势为电解后正负离子化学势的加和值。但化学势为强度性质,应不具有加和性质,如何解释上述关系式?
9、含有0.01 mol·dm-3 KCl及0.02 mol·dm-3 ACl(强电解质)的水溶液的电导率是38.2 S·m-1,如果K+及Cl-的离子摩尔电导率分别是74×10-4和76×10-4 S·m2·mol-1,试问离子A+的摩尔电导率Lm(A+)是多少?
10、今有一种酸的水溶液 A 和一种碱的水溶液 B,用 A 滴定 B ,知道两者的浓度相等 , 而测定电导则 B 大。将 A 和 B 都稀释 100 倍后发现kA、>kB、,据此推断他们是什么样的酸碱 ? 并作简要说明?
