临床荧光PCR结果分析及常见问题
中国人民解放军三零二医院 王海滨
一、荧光 PCR 技术在临床诊、疗中的应用
PCR 技术是于 1983 年由 Mullis 发明,后来传到我国,但是由于实验污染的问题, 1998 年卫生部取缔 PCR 实验方法在临床诊断中的应用。荧光 PCR 出现后,污染减少很多,但近几年由于磁珠的应用,污染又再起。 20## 年, PCR 在 SARS 的早期诊断中非常有效,当时使用的是电泳法。 H1N1 甲型流感( 20## ):荧光 PCR 技术作为确诊指标( 755 份 / 天)。疾病易感基因的研究( SNP ): CR1/ 丙型肝炎 IL-28B 。疾病(肿瘤)易感基因的鉴定。
二、影响临床荧光 PCR 检测结果的因素
(一)影响临床荧光 PCR 检测结果的常见因素
1. 检验因素:
实验室硬件、仪器、试剂、人员素质、技术水平、管理水平。
2. 非检验因素:
标本采集、质量、部位、标本保存、条件、时间、标本中的干扰物质、样本丢失!
(二) 加强检测前标本的质量管理——避免问题重复发生
规范标本前处理流程、制度化的重要性,建立不合格标本记录和定期总结制度、制定解决措施与可行路径(编号和项目错误等),查找标本丢失可能的环节。加强本室新进工作人员流程培训,经常性进行临床医护的交流与培训。
(三) 实验室分区
分为:试剂配制、核酸提取、 PCR 扩增以及开放产物分析等区域。
分区目的:通过物理分割达到标本、试剂或使用器具等被沾染或掺入污染,标本间的交叉污染等。
分区要求:至少要有清洁的试剂配制和核酸制备区
三、试剂配制
(一)试剂配制室的设置与维护
以空间内无核酸气溶胶为准!
1 .正压、清洁进风 ( 壁挂式空调 ) 。
试剂冰箱内勿存放病原或核酸相关物品!定期清洁除霜!
2 .有效氯消毒液清洁实验室台面、地面。
3 .移液器:使用前的清洁。
4 .离心机等:每周定期木浆纸巾擦拭,方法。“一次性物品的使用 - 从 COBAS 的“浪费”中找到均衡!
(二)试剂配制注意事项
试剂配制实际是简单的问题,但是也是非常复杂的环节。
1. 何时配制?如何配制!
在核酸制备好后再进行试剂配制,注意反复冻溶对试剂质量的影响,以及久配不用试剂对检测的影响 ( 如 hot-TaqE) 。
2. 如何避免荧光淬灭?
避免在强光下配制,采用有效氯消毒液后应进行通风或清水擦拭,勿在紫外灯下配制。
3. 交叉污染的避免
试剂与核酸何者先加更合理?
试剂分配中的问题:过吸、残滴(第一孔)。
热盖不能完全阻止蒸发,石蜡油,盖、膜、离心。
(三)试剂配制环境对检测的影响
PPT8 显示的是试剂配制环境对检测的影响,左边的图,是实验室在装修的时候用了一些油漆,在那个环境里面配制的试剂。右边的图,是在无油漆环境下配制的。可以看到左边的图结果很差。
(四)核酸制备
冻存标本使用前要混匀离心后使用;不同类型标本:血清、血浆、细胞、组织、乳汁、痰液、尿液等;标本核酸提取前后的保存;提取后核酸的保存(稳定性);核酸提取标本加入量与核酸得率的关系! 1+1 与 2 的关系;指示剂的引入,可以降低差错率。
PPT10 显示的是指示剂在一管法的应用,可以看到上面蓝色的是核酸提取液,非常清楚,降低了差错。
四、 荧光 PCR 扩增
(一)实验室怎么建?
独立区域、负压通风、物品专用:
1. 实验室清洁用品的专用的重要性。
2. 扩增产物的处理( PCR 管加盖、封膜、石蜡油),用两层封口袋包装后焚烧(如 PPT12 图)。产物的处理必须由专业工作人员或经过培训的工作人员处理。禁止未经培训的研究生、实习生和进修生进入区域对扩增产物进行操作。
3. 仪器清洁处理程序:载板区先用 70% 乙醇清洁。该区所有垃圾需封闭运输并销毁。
4. 地面和空气处理原则。
(二) 荧光 PCR 仪器如何选择?
PCR 实验室的仪器非常多有几十种,应按照实验的要求不同来进行选择。
(三)荧光 PCR 仪器如何维护?
荧光 PCR 仪器的功能模块分为三个:
1. 温度模块
包含最基本的升降温。要保证温度模块的均一性,既不能有边缘效应,也不能有局部温度的影响。
2. 光学模块
即测光系统, PCR 反应的过程中每一个循环都要测一次光,测光不论是照相还是扫描,都有一定的差别,光学模块的敏感性要高。
3. 软件模块
荧光信号采集以后,要用软件模块来进行分析。分析不但要人性化,而且还要准确,不能有故障。
(四)荧光 PCR 扩增循环数量的选择( 60:50:40cycles )
COBASTAQMAN 用的是 60 个循环,早期是 40 个循环,近几年的荧光 PCR 试剂,循环数有所增加,如丙肝增加到 45 个循环,乙肝 42 个循环。
PPT16 显示的是实验室的图,扩增的循环数量是 40 个。
(五)质控品的设立 - 没有质控就没有质量保证
对一个完整的实验,一定要注意有空白对照,阴性对照与临界对照,临界对照是对精密度的考核。另外,有平行定量标准品。如果试验测的是血清,质控标准品也应该是血清,而不是人造核酸。
质控品在结果报告中的应用非常重要:
1. 空白对照
一般放在第一孔的位置,监控扩增试剂及环境污染。
2. 阴性对照
第二孔位置,监控核酸提取,试剂是否污染,可自行制备。
3. 临界对照
实验室自行制作,是实验精确度需求。
4. 等效定量标准品
中间位置或最后,实验准确性前提,参与核酸提取,标准范围宽。
(六)质控品的制作
HBVDNA :介质的选择、临界质控的制作: 400IU/ML-50IU/ML ; HCVRNA :介质的选择、临界质控的制作: 3000IU/ML-100IU/ML ; EBVDNA/CMVDNA/H1N1/HPV 等定性试剂盒的质控,阳性标本,稳定性实验;质控品的朔源: WHO 标准或 COBAS 等;自建质控品:建立数据记录(稳定性等);室间质控与室内质控的有机结合!
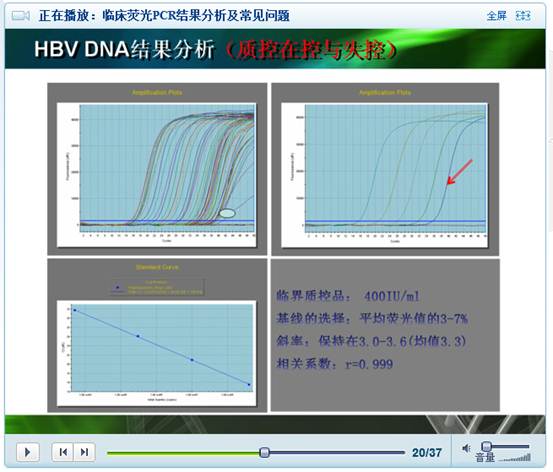
(七) HBVDNA 结果分析(质控在控与失控)
HBVDNA 结果分析,就是荧光曲线的分析,要尽可能保证报告的数值,低限值和高于低限值的线要平行,尽可能不要失控。
临界质控品: 400IU/ml ;基线的选择:平均荧光值的 3-7% ;斜率:保持在 3.0-3.6( 均值 3.3) ;相关系数: r=0.999 。
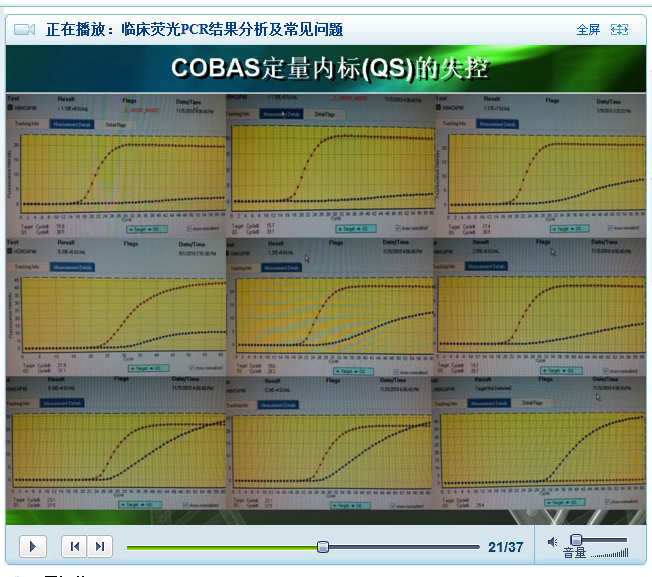
1.COBAS 定量内标 (QS) 的失控
PPT21 显示的是 COBAS 定量内标失控的情况。
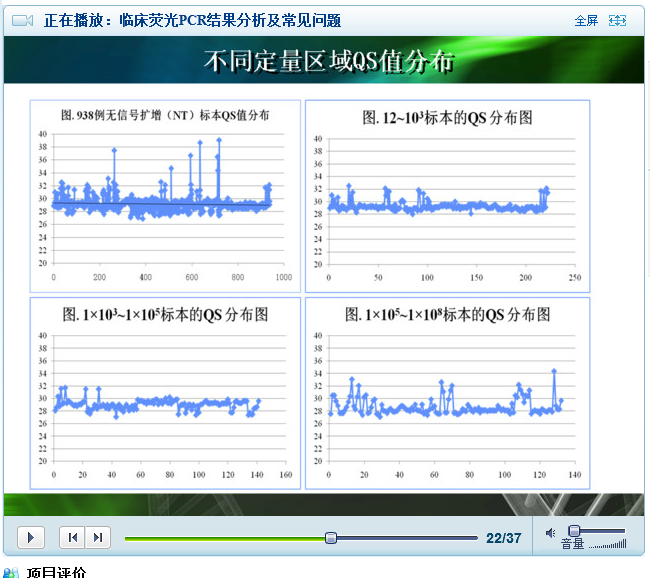
2. 不同定量区域 QS 值分布
PPT22 显示的是不同定量区域 QS 的分布,例数是 900 多例。如果内标出现了失控,定量值就无法参考了。
3. 假阴性曲线的识别
在荧光 PCR 曲线里面,如果有荧光曲线是阴性、不规则的,要考虑是不是有干扰物质,在试剂配制或者标本里边有干扰物质。此时需要复检。
五、实验室人员(与职称和学历无关)
(一)实验室人员分类
1. 实习型:
按照操作说明进行操作,但环节控制、环节间衔接和防污染意识差!
2. 工作型:
能够再现说明书操作要求,具有质量环节控制意识,具有一定的防污染常识,但发现问题和解决问题能力稍差。
3. 示教型:
明晰试验操作的关键环节,并能够对下级工作人员进行演示和示教,具有完整的防污染意识、质量实现和一定的发现问题解决问题能力。
4. 专家型:
能对商品试剂盒存在的问题进行改进,具有提前预知的质量意识。
(二)移液器的使用
移液器的使用,是小问题,大学问。
1. 移液器加吸头的要点,需慢慢压,不能用力压。
2. 不同量程移液器的应用要点(液体性质)。
3. 移液器连续分液挂滴对实验的影响。
4. 如何避免移液器连续分液导致的污染。
5. 移液器吹打混匀带来的污染!
6. 移液器的清洗,需要高压吗?
7. 移液器的校准,很多单位无法实现。
(三)质量环节意识的培养(轮流当主任)
1. 环节控制能力
质量环节的认知:明晰实验操作环节的组成和目的!
关键环节的实现:细节的严谨性与准确性!
环节的连贯性与细节实现:实现完整实验!
2. 防污染素质
实验室环境防污染意识:具备科学防污染清洁意识和实现能力,如标本外溢的处理、实验室环境(空气、桌面、地面、移液器等)清洁,实验废物的管理和处理,离心机的清洁和维护等。标本间交叉污染的预防意识和实现能力:避免移液过程中的隐形迸溅污染(移液器);试剂加样过程中的沾染污染;标准品的携带污染等。扩增产物的外露污染:产物回流预防能力;产物处理流程。
(四)人员的培养与专业技能比对
不同职务、职称和学历人员同时进行;环节操作与结果同时计分;比对结果记录在案并作为评聘指标。
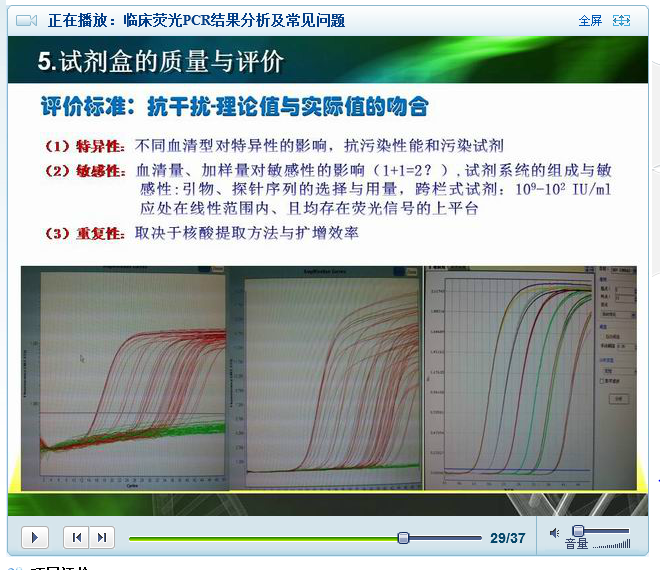
六、试剂盒的质量与评价
(一)评价标准:抗干扰 - 理论值与实际值的吻合。
1. 特异性:不同血清型对特异性的影响,抗污染性能和污染试剂
2. 敏感性:血清量、加样量对敏感性的影响( 1+1=2 ?) , 试剂系统的组成与敏感性 : 引物、探针序列的选择与用量,跨栏式试剂: 10 9 -10 2 IU/ml 应处在线性范围内、且均存在荧光信号的上平台。
3. 重复性:取决于核酸提取方法与扩增效率。
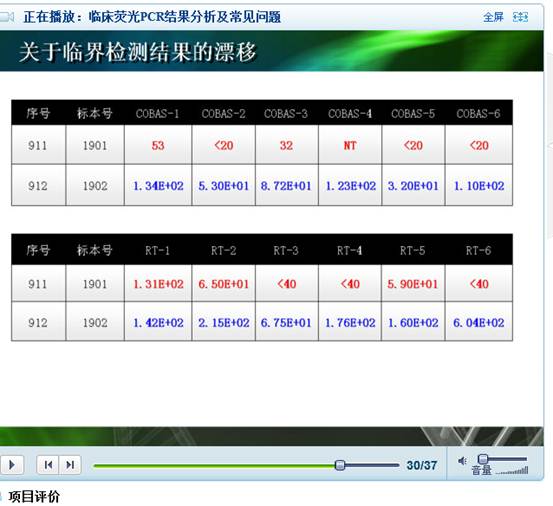
(二)关于临界检测结果的漂移
例如,本场检测的时候,一个病人,一次检测是 53IU ,一次是 <20IU ,这都是漂移,这个技术方法性能本身,是正常的和合理的。但这种漂移的原因,是试剂盒核酸提取的稳定性问题。
七、关于内标
(一)实时荧光定量 PCR 无需内标
实时荧光定量 PCR 技术有效地解决了传统定量只能终点检测的局限,实现了每一轮循环均检测一次荧光信号的强度,并记录在软件之中,通过对每个样品 Ct 值的计算,根据标准曲线获得定量结果。
1.Ct 值的重现性:
PCR 循环在到达 Ct 值所在的循环数时,刚刚进入真正的指数扩增期(对数期),此时微小误差尚未放大,因此 Ct 值的重现性极好,即同一模板不同时间扩增或同一时间不同管内扩增,得到的 Ct 值是恒定的。
2.Ct 值与起始模板的线性关系:
由于 Ct 值与起始模板的对数存在线性关系,可利用标准曲线对未知样品进行定量测定,因此,实时荧光定量 PCR 是一种采用外标准与标本同步进行核酸提取的曲线定量方法。
(二)内标对实时荧光定量 PCR 的影响
若在待测样品中加入已知起始拷贝数的内标,则 PCR 反应变为双重 PCR ,双重 PCR 反应中存在两种模板之间的干扰和竞争,尤其当两种模板的起始拷贝数相差比较大时,这种竞争会表现得更为显著。但由于待测样品的起始拷贝数是未知的,所以无法加入合适数量的已知模板作为内标。正因如此,定量方法虽然加入内标,仍为一种半定量方法。
美国 Texas 大学的科研人员进行了外标法定量和内标法定量的方法学比较,得出的结论是:内标法作为定量或半定量的手段是不可靠的,而外标准曲线的定量方法是一种准确的、值得信赖的科学方法。
AppliedBiosystems 公司的 7700 型实时荧光定量 PCR 仪是全球公认的荧光定量 PCR 的金标准,可实现多色荧光同时检测,但定量检测仍然采用外标准曲线的方法,而不用内标进行定量。
(三)内标对 PCR 扩增的影响
PPT34 显示的是内标对 PCR 扩增的影响。
左图,可以看到加入内标后线性范围变窄,无内标线性范围较宽。
右图,无内标时是直线,有内标后,变成曲线。
个人建议:试剂盒在报批时,或使用单位对试剂盒质量进行评估时,使用内标对试剂盒性能进行评价!检定:正如 ELISA 试剂盒的批批检!
八、如何就分子诊断结果与临床和患者沟通?
医生和患者,都会对检验结果提出一些质疑。质量、速度应该还是个硬道理,应该权威的结果加虚心的请教。




第二篇:荧光定量PCR常见问题-Good

1. 定量PCR仪的开关机顺序是怎样的?
按照正确的开关机顺序操作,有助于延长仪器的使用寿命,减少仪器出故障的频率。开机顺序:先开电脑,待电脑完全启动后再开启定量PCR仪主机,等主机面板上的绿灯亮后即可打开定量PCR的收集软件,进行实验。关机顺序:确认实验已经结束后,首先关闭信号收集软件,然后关掉定量PCR仪主机的电源,最后关闭电脑。
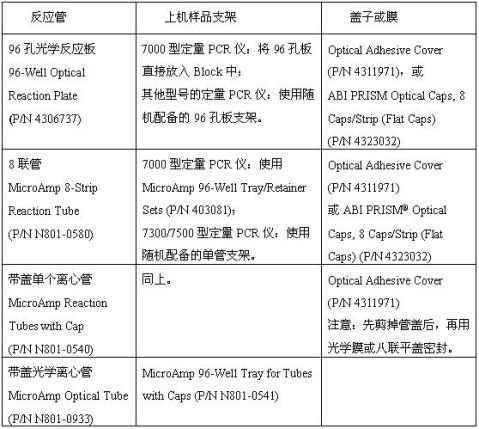
2. 哪些种类的反应管和盖子适合定量PCR实验使用?有何需要注意的地方? 定量PCR实验可以使用以下耗材:96孔光学反应板配合光学膜,0.2 ml光学八联反应管配合光学膜,0.2 ml光学八联反应管配合平盖的光学八联管盖。ABI公司生产的定量PCR耗材的具体使用方法和货号见下表:
3. 为什么要定期对电脑进行磁盘碎片整理?怎样整理?
当运行实时定量PCR仪及使用软件分析实验结果时,计算机会删除并创建若干文件,计算机硬盘的空闲空间会被分割成越来越多的小块。当硬盘驱动器上文件以分解的碎片存储时,程序需要更长的时间才能存取文件,因为必须多次寻找文件碎片以存取不同的片断。碎片整理实用程序将一个文件分解开的多个碎片合并在一起,并存储到硬盘的同一个位置,从而清除文件碎片,进而优化系统性能。
碎片整理的方法如下:
? 在Windows桌面上,选择开始(start),我的电脑(My computer)。
? 在(我的电脑)窗口中,用鼠标右键单击硬盘驱动器,并选择(属性)property。
? 在(属性)对话框中选择工具(Tools)选项卡,单击开始整理(Defragment now)。
? 单击碎片整理(Defragment)。
? 当显示“碎片整理完毕”对话框时,单击(确定)。
? 在“本地磁盘属性”对话框中,单击(确定)。
为计算机机中剩余的驱动器重复如上步骤。
4. 何时执行windows service pack更新?
不要执行该操作。除非美国应用生物系统公司代表通知您更新操作系统,否则请不要更新控制定量 PCR 仪的计算机的操作系统。新版本的 Microsoft Windows 操作系统有可能与SDS 软件存在冲突,并导致仪器不能正常运行。如果您希望安装 service pack(更新包)以更新操作系统,应查看随 SDS 软件提供的版本说明,避免兼容性问题。
5. 应该备份哪些数据?
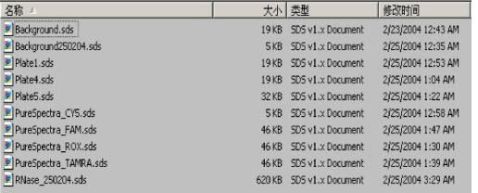
应该定期备份您的实验数据,备份频率推荐每周一次,用光盘刻录。同时您也应该备份定量PCR仪的各种纯荧光光谱校正文件、背景文件和安装验证实验数据,这些文件所在的目录是C:/Appliedbiosystems/SDS Document。下图是校正文件的样本。
6. 怎么样的实验室环境才能保证仪器设备正常运行?
良好的实验室环境有助于延长仪器的使用寿命,减少仪器出故障的频率。推荐做到以下几个方面:
电源:推荐配备合适的UPS或稳压器。
通风:仪器的通风应该没有阻挡。
温度:推荐实验室配备空调,温度应该控制在10-30°C之间。
湿度:20-80%;对于潮湿的省份,推荐实验室配备除湿机。
空间:易于操作,安全。
7. 怎样判断定量PCR仪的样本加热块是否被污染?怎样清除污染?
一个办法是运行背景校正反应板,当一个或多个反应孔连续显示出不正常的高信号,则表明该孔可能被荧光污染物。另外一种办法是在不放任何物品到样本块上的前提下,执行ROI的校正,当某个孔的信号明显高出其他孔时,则表明该孔被污染。
清除样本加热块污染的步骤如下:
用移液器吸取少量乙醇并滴入每个污染的反应孔中。
吹打数次。
将废液吸入废液杯中。
重复以上步骤:乙醇三次,去离子水三次。
确认反应孔中的残留液体蒸发完
8. 什么是背景校正?多长时间执行一次背景校正?
背景校正程序测量定量PCR仪所使用的反应管和水的空白荧光强度。在运行校正程序期间,定量PCR仪在10分钟内连续读取背景校正板的荧光强度,信号收集的温度为60 °C。随后,SDS软件计算所收集到的荧光强度的平均值,提取结果并保存到校正文件中。软件在今后的分析中将自动调用此校正文件,从实验数据中扣除背景信号。
因为背景荧光的信号强度随着许多外界因素(比如外来的污染、反应板/反应管的生产厂商不同、水的纯度等)而变化,所以推荐定期进行背景校正,一般每三个月到半年校正一次。
9. 什么是纯荧光校正?多长时间校正一次?
纯荧光校正是测定各种纯荧光染料标准品的波长和信号强度,通俗地说是让仪器“认识”各种荧光染料。软件收集并储存各种纯荧光染料标准品的荧光信息。以后每次定量实验运行过程中,SDS软件收集样品的原始光谱信号,并将此原始光谱与纯荧光文件中的数据进行比较,精确扣除不同染料的信号重叠部分,从而确定样品中的荧光染料种类和信号强度。
推荐每隔半年进行一次纯荧光校正。在运行光谱校正之前,请先进行背景校正和ROI校正。
10. 96孔板怎样封膜?
当使用96孔板做实验的时候,推荐使用光学膜代替盖子来密封反应孔。正确的封膜方法是:先沿着96孔板的纵向压膜,然后横向,最后沿着板的边缘按压使之密封。具体手法见下面图示:

11. 使用单管或8连管做实验时,在样品加热块上应该怎样安排放置?
使用单管或8连管做实验,并且样本数量不多的时候,建议在样品加热块(TRAY)上对称地安放样品,最好是纵向放置,并且优先放在第6列或第7列,然后逐渐向两边放置。这样做的好处是热盖压下来的时候不至于发生倾斜,各个反应管的受力和受热都比较均匀,提高孔与孔之间的数据精密性。
12. 绝对定量与相对定量有什么区别?
绝对定量的目的是测定目的基因在样本中的分子数目,即通常所说的拷贝数。相对定量的目的是测定目的基因在两个或多个样本中的含量的相对比例,而不需要知道它们在每个样本中的拷贝数。举例来说,如果研究项目中包括处理过的和未经处理的对照样本,通常可以将未经处理的样本指定为基准,规定其目的基因浓度为100%,将经处理的样本的定量结果除以对照样品的定量结果,就可以计算各个处理样本的基因含量相对于未处理样品的百分比。
绝对定量实验必须使用已知拷贝数的绝对标准品,必须做标准曲线。相对定量可以做标准曲线,也可以不做标准曲线。
相对定量实验有两种方法:标准曲线法和CT值比较法。如果使用标准曲线法,可以使用绝对标准品,也可以使用相对标准品,而且相对标准品在实验操作上更为简便易行。相对标准品是只知道样品中DNA或RNA的稀释比例而不需要知道其分子数目的标准品,典型的做法是将一个已知pg数的样品做一系列梯度稀释。
CT值比较法是利用CT值与起始DNA浓度的对数成反比的数学关系,来计算不同样本之间的相对百分比,其计算公式是
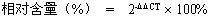
绝对定量的数据易于理解,但是绝对标准品的制备和测定其DNA含量比较困难。有许多商业性的标准品试剂盒供选购,可以解决这种困难。相对定量的标准品容易在实验室里自己制备,但是数据处理比较麻烦,对实验数据的解释有一定难度。
13. 定量PCR基因表达的实验数据应该如何处理?
总的来说,有三个层次的校正是必须要做的。
首先,参比信号校正。试剂中必须包含固定浓度的ROX,这样由于反应总体积的差异、所在孔的位置不同、试管壁的厚度差异、管盖透光性能的差异等所引起的荧光信号波动都能够被扣除,使数据真正反映PCR进程。ROX校正能够极大地改进定量的精确度,提高重复管之间的数据重现性。
其次,内对照校正。实验中加入样品基本上都是以体积为单位的,但是同样体积的不同样品很可能来自不同数目的细胞,所以将实验结果校正到每个细胞的含量是必要的。方法是在定量目的基因(如IL-2)的同时定量一个内对照基因(如18S RNA基因),然后IL-2/18S。内对照校正使不同样品的实验数据可以相互比较。
第三,计算相对于基准样品(Calibrator)的相对基因含量。比如研究处理和未处理的、0小时和6小时的、正常和患病的之间的基因表达的差别,则需要计算处理/未处理、6小时/0小时、患病/正常。
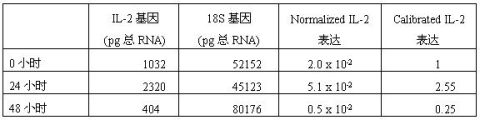
14. 标准曲线法相对定量的数据应该怎么处理?
假设实验的目标是研究药物处理后0、24、48小时IL-2基因在某种组织中的表达量的变化,所用的内对照是18S RNA基因。IL-2和18S RNA的测定结果都是总RNA的pg数,数据的处理方法见下表:
15. 什么是CT值比较法?数据怎么处理?
CT值与起始DNA浓度的对数成反比:
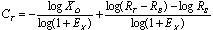
如果(1)不同管之间的PCR反应效率相同;(2)这些PCR的反应效率接近100%,可以从上面的公式推出相对含量(X01/X02) = 2 -ΔΔCT
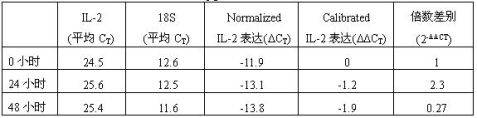
假设实验的目标是研究药物处理后0、24、48小时IL-2基因在某种组织中的表达量的变化,所用内对照是18S RNA基因。IL-2和18S RNA的测定结果都是CT值,而没有通过标准曲线测定总RNA的pg数。数据的处理方法见下表:
16. 每个反应管中可以加入多少种探针?
每个反应管中可以加入的探针数目,取决于仪器、软件、试剂和实验设计等几个方面。
首先是仪器的硬件构成和软件的解析能力。在软件解析能力足够的前提下,全波长检测的定量PCR仪如激光管-CCD类型对于探针的数量实际上是没有限制的。如果信号的采集要通过滤色片,那么探针的数量取决于滤色片的数目,增加探针需要增加或改变滤色片。改动仪器的结构通常很困难。以AB公司的仪器为例,7900和7700是激光-全波长检测的,7000、7300是4色滤色片的,7500是5色滤色片的。
其次是化学上的可能性。不同的荧光基团要组合到一起,在同一反应管内使用,必须其激发波长既相对靠近又不能靠得太近,既保证信号激发的效率又保证信号不重叠干扰,能够区分清楚。现已发现的荧光基团种类有限,满足这样条件的分子组合更少。目前的最佳组合只能达到每组4到5种荧光的水平。
第三是实验方案的设计和选用的探针类型。定量PCR实验必须使用ROX校正荧光,占去一种荧光;TaqMan探针的淬灭基团(TAMRA)也要占用一种荧光,对于4色检测的仪器来说,只剩下2种荧光可以标记探针,对于5色检测的仪器还有3种荧光可以使用。如果将探针改用TaqMan MGB探针,由于它的淬灭基团是不发荧光的,比之TaqMan探针就可以多1种荧光用于标记探针。如果实验要求不高,不做ROX校正(AB公司不推荐这样做),还可以再多一种荧光用于标记探针。
第四是研究应用本身的要求。如果研究SNP和基因突变,因为绝大多数人类基因是2态的,只存在两种等位基因,2条探针已经足够。如果研究基因表达,通常是两两比较居多,比如处理比未处理,正常比异常等,加上一个内对照,3色也就足够了。
最后是成本控制方面的要求。多重定量的目的一是提高数据精确度,二是节省反应成本。同时测定的基因越多,成本也越低。但是加入4-5种探针,就要同时加入8-10条引物。在引物设计的时候要考虑到尽量减少这些引物之间的竞争和抑制等多种干扰,平衡各对引物之间的PCR效率。虽然这是可以做到的,但是要花费大量时间、人力和物力来筛选最佳引物组合、优化反应条件。如果实验规模不大,在总体上可能反而不合算。
在实际应用中,不是单纯追求加入的探针越多越好,而是追求总体效益的最优化。比较切合实际的是2到3重反应,引物和探针的设计不太困难,反应条件的优化也不太麻烦,同时降低了成本。
17. 等位基因鉴定实验(比如SNP分型)是定性的研究,是否可以不进行ROX荧光校正?
不,等位基因鉴定实验也要进行ROX荧光归一,以保证实验结果的精密可靠。
由于试剂加样操作的误差、离心管热量传递的误差、离心管盖透光性能的误差等偶然因素是不可避免的,必然导致荧光激发效率的差异,因此仪器收集到的原始信号必须进行归一化校正,相互之间才可以比较并保证重现性。
这种校正是通过在反应缓冲液中添加ROX校正荧光来实现的。ROX在反应缓冲液中的浓度是固定的,因此其信号的高低变化只与上述物理方面变化的总体效应有关。将报告荧光的信号除以ROX荧光的信号,就能够消除所有这些物理因素所引起的数据波动。
18. 内标法和外标法哪种数据更精密?
是同样可靠的。内标的优点在于目标基因与管家基因的反应条件最接近一致,缺点在于目标基因与管家基因的引物和探针相互之间会发生竞争与抑制,导致它们的PCR效率有差异。外标的优点在于目标基因与管家基因的引物和探针之间没有发生竞争与抑制的机会,但是不同管之间的反应条件差异比同管的要大,也会导致它们的PCR效率有差异。两相比较,内标法与外标法的数据精确度是一样的。
