吉林化工学院
食品分析实验报告
实验名称 蛋白质含量的测定
指导教师 陈 萍
班 级 食 品 0901
学 号 09340136
姓 名 黄 锡 红
日 期 2012.11.28
蛋白质含量的测定
一、目的与要求:
掌握微量凯氏法测定蛋白质总氮量的原理及操作技术。包括样品的消
化,蒸馏吸收及滴定与含氮量的计算。
二、原理:
凯氏定氮法:食品经加硫酸消化使蛋白质分解,其中氮素与硫酸化合成硫酸铵。然后加碱蒸馏使氨游离,用硼酸液吸收后,再用盐酸或硫酸滴定根据盐酸消耗量,再乘以一定的数值即为蛋白含量,其化学反应式如下。
( 1 ) 2NH2(CH2)2COOH+13H2S04 (NH4)2S04+6C02+12S02+ 16H2
(2)(NH4)2SO4+2NAOH-----2NH2+2H2O+NA2SO4
(3)2NH3+4H3BO3----(NH4)2B4O7+5H2O
(4) (NH4)2B407+H2S04+5H20-(NH4)9SO4+4H2BO2
三、试剂与仪器:
1、硫酸钾
2、硫酸铜
3、硫酸
4、2%硼酸溶液
5、40%氢氧化钠溶液
6、混合指示剂:把溶解于95%乙醇的0.l%溴甲酚绿溶液10毫升和溶于95%乙醇的0.l%甲基红溶液2毫升混合而成.
7、约0.01mol/L硫酸标准溶液.
8、KDN-08A(04A)定氮仪
9、三角瓶250ml 3只。
10、量筒50ml、l0ml、l00ml。
11、吸量管10ml只。
12、酸式滴定管1支。
13、容量瓶100毫升1只。
14、小漏斗1只。
四、实验步骤
1.样品处理: 移取5ml牛奶,移入干燥的500ml定氮瓶中,加入0.2g硫酸铜,3g硫酸钾及20毫升硫酸,将消化管分别放入消化架各个孔呢,然后置于消化炉上,然后开启抽气三通上自来水龙头,使抽气三通处于吸气状态,接通电源,在加热初始阶段防止样品飞溅(选用电压型控温的消化炉起先控制在150伏左右,1h左右后可满电压工作)。待内容物全部炭化,泡沫完全停止后,加强火力,并保持瓶内液体微沸,至液体呈蓝绿色澄清透明后,再继续加热0.5小时。取下放冷,放冷后,移入100ml容量瓶中,并用少量水洗定氮瓶,洗液并入容量瓶中,再加水至刻度,混匀备用。
取与处理样品相同量的硫酸铜、硫酸钾、硫酸铵同一方法做试剂空白试验。
2.蒸馏: (KDN-08A为例)蒸馏器中,碱液及蒸馏水采用电磁泵加入,NaOH ,H2O注入接口用橡胶管套入后分别置入自备的容器中,加液时按面板上相应开关,液体由泵吸入消化管内,注入毫升数视标尺所注位置而定。
向接收瓶内加入50ml 2%硼酸溶液及混合指示剂1滴,并使冷凝管的下端插入液面下,吸取10.0ml样品消化液于定氮瓶中,加入10ml 40%氢氧化钠溶液,开始蒸馏,在接收瓶内接收液达150ml左右时移下接收瓶,用蒸馏水冲洗滴管口,继续蒸馏半分钟,然后取下接收瓶,待滴定用。
3.滴定: 取下接收瓶,以0.01N硫酸或0.01N盐酸标准溶液定至灰色或蓝紫色为终点。
同时吸取10.0ml试剂空白消化液按3操作。
4.硫酸标准溶液的标定: 称取固体碳酸钠0.2232g于烧杯中加少量水溶解,溶解后移入250ml容量瓶中,定容,摇匀。再分别移取25ml碳酸钠溶液三分于100ml锥形瓶中,各加入两滴指示剂。用标准硫酸溶液滴定到颜色由淡红色变成灰色即为滴定终点,记录硫酸溶液消耗的体积。
四、数据记录
实验数据表1-1

五、计算
1.标准硫酸溶液浓度计算
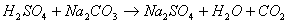
1 1
CV m/M
由表1-1数据可算出硫酸浓度(由于称量时,碳酸钠质量扩大了10倍,所以计算时需缩小10倍,所以下列式中“10”表示10倍)
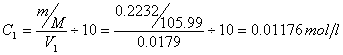
同理: 为0.01172 mol/l,
为0.01172 mol/l,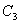 为0.01170 mol/l
为0.01170 mol/l
 mol/l(1mol/l=1N)
mol/l(1mol/l=1N)
2. 样品中蛋白质的含量计算
公式: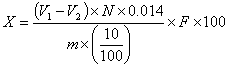
X:样品中蛋白质的含量,g;
V1:样品消耗硫酸或盐酸标准液的体积,ml;
V2:试剂空白消耗硫酸或盐酸标准溶液的体积,ml;
N:硫酸或盐酸标准溶液的当量浓度;
0.014:1N硫酸或盐酸标准溶液1ml相当于氮克数;
m:样品的质量(体积),g(ml);
F:氮换算为蛋白质的系数。

即每毫升样品中蛋白质含量为1.91g
六、结果讨论
相对于其他的蛋白质含量测定法,凯氏定氮法虽然比较复杂,但较准确,往往以订单发测定的蛋白质作为其他方法的标准蛋白质。从实验结果测得的实际数据和包装盒上厂家所给数据,可以清晰知道,蒙牛和光明纯牛奶的蛋白质含量是没有虚假上报的,而伊利纯牛奶的蛋白质含量没有包装盒上所给的高。可能是测定的时候有一些实验操作过程所造成的误差。所以可以通过别的测定蛋白质的含量的方法进行进一步鉴定。或者再次使用凯氏定氮法测一次伊利牛奶的蛋白质含量。以得到更加准确可靠的结果。
七、注意事项
(1)样品应是均匀的,固体样品应预先研细混匀,液体样品应振摇或搅拌均匀。
(2)样 品放入定氮瓶内时,不要沾附颈上,万一沾附可用少量水冲下,以免被检样消化不完全,结果偏低。
(3)消化时如不容易呈透明溶液,可将定氮瓶放冷后,慢慢加入30%过氧化氢2-3ml,促使氧化。
(4)在整个消化过程中,不要用强火,保持和缓的沸腾,使火力集中在凯氏瓶底部,以免附在壁上的蛋白质在无硫酸存在的情况下。使氮有损失。
(5)如硫酸缺少,过多的硫酸钾会引起氨的损失,这样会形成硫酸氢钾,而不与氨作用,因此当硫酸过多的被消耗或样品中脂肪含量过高时,要增加硫酸的量。
(6)加入硫酸钾的作用为增加溶液的沸点,硫酸铜为催化剂,硫酸铜在蒸馏时作碱性反应的指示剂。
(7)混合指示剂在碱性溶液中呈绿色,在中性溶液中呈灰色,在酸性溶液中呈红色。如果没有溴甲酚绿,可单独使用0.1%甲基红乙醇溶液。
(8)氨是否完全蒸馏出来,可用PH试纸试馏出液是否为碱性。
(9)吸收叶也可以用0.01当量的酸代表硼酸,过剩的酸液用0.01N碱液滴定,计算时,A为试剂空白消耗碱液数,B为样品消耗碱液数,N为碱液浓度,其余均相同。
(10)以硼酸为氨的吸收液,可省去标定碱液的操作,且硼酸的体积要求并不严格,亦可免去用移液管,操作比较简便。
(11)向蒸馏瓶中加入浓碱时,往往出现褐色沉淀物,这是由于分解促进碱与加入的硫酸铜反应,生成氢氧化铜,经加热后又分解生成氧化铜的沉淀。有时铜离子与氨作用,生成深兰色的结合物[Cu(NH3)4]++
八、思考题
1.本实验的误差来源有哪些?
答: 凯氏定氮仪测定蛋白质含量的误差来源可能是样品、催化剂种类和用量、消化的时间、加碱液后的操作、蒸馏加热、清洗凯氏定氮仪的过程、凯氏定氮仪的气密性、氨气是否完全蒸馏出来;硼酸是否封住蒸馏管口、试剂的准确性、滴定终点的判断、滴定盐酸的浓度准确性等。
2. 试验中加入硫酸钾和硫酸铜混合物的作用是什么?
在硫酸消解液中,硫酸钾的作用是提高硫酸的沸点以提高消解温度;硫酸铜是催化剂,其作用是加快消解速度,二者的共同作用是缩短消解时间,减少消解过程中氨的逸失
九、评语和成绩
成绩: 指导教师:
第二篇:Lowry氏法测定蛋白质含量







