分析化学实验要求
1. 进入实验室: a. 提前10min;b. 着白大褂;c. 不能穿拖鞋;d.带预习报告。
2. 实验过程中: a. 台面整洁,仪器摆放合理整齐;b. 站立操作,规范认真;
c. 原始数据及时记录在实验报告上,实事求是,规范正确。
3. 实验结束后:a. 仪器洗净,归架回柜;b. 台面整理,公用试剂归架摆放整齐。
4. 值日生职责: a. 水、电、门、窗、地面、垃圾; b. 实验台整理,清洁。
实验一、电子天平称量及滴定基本操作练习(4学时)
一、目的要求:
1. 熟悉和掌握分析天平的使用方法;
2. 学会正确使用称量瓶和用各种称量法称量试样;
3. 学习掌握定量分析常用仪器的洗涤和使用方法;
4. 初步练习滴定分析操作,学会正确判断滴定终点。
二.方法原理:
电子天平依据电磁力平衡原理,可进行直接称量。速度快、精度高。
酸碱互滴:HCl + NaOH = NaCl + H2O pHsp=7.0
三.实验内容:
(一).分析天平称量练习
1. 检查天平:a. 是否水平,b. 秤盘是否清洁,c. 干燥剂是否失效。
2. 开启天平,预热半小时后:a. 调节零点(TARE),b. 用标准砝码校准
(TARE → CAL → 放上砝码 → CC → 200.0000 ± 0.2 mg)。
3. 称量练习
a. 直接称量法:称两坩埚及称量瓶质量。
b. 递减称量法(差减法或减量法):
称0.3-0.4g粗K2Cr2O7两份于坩埚中,并验证(?≤±0.4mg)。
c. 固定质量称量法(指定质量称量法或增量法):
称0.5000g粗K2Cr2O7一份于坩埚中(?≤±0.2mg)。
4. 使用登记、天平复原(关机、加罩)、台面整理
(二).滴定分析基本操作练习
1. 仪器洗涤:(干净——内壁不挂水珠)
去污粉刷洗 → 自来水冲洗 → 蒸馏水润洗(少量多次原则)
2. 操作液的装入:
滴定管检漏→ 洗涤→ 润洗→ 装液→ 排除气泡→ 调节零点→ 悬滴挂除
3. 酸碱互滴基本操作练习:
a. HCl滴定NaOH 甲基橙(MO) 1D 黄色→橙色
b. NaOH滴定HCl 酚酞(PP) 2-3D 无色→微红色
四.数据记录与结果处理
1. 要求:规范、正确、清晰、实事求是
准确质量—— 0.0001g; 准确体积—— 0.01mL
2. 称量结果记录格式
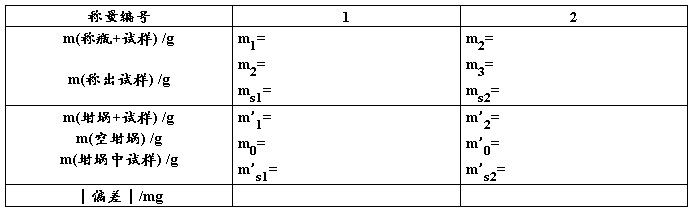
3. 实验报告的书写:
——思路清晰、认真规范
六.思考题
P156:1、4、5
第二篇:实验1 滴定分析基本操作练习
实验1 滴定分析基本操作练习
一、实验目的
1.学习、掌握滴定分析常用仪器的洗涤和正确使用方法。
2.通过练习滴定操作,初步掌握甲基橙、酚酞指示剂终点的确定。
二、实验原理
0.1mol·L—1 HCl溶液(强酸)和0.1mol·l—1 NaOH(强碱)相互滴定时,化学计量点时的pH为7.0,滴定的pH突跃范围为4.3~9.7,选用在突跃范围内变色的指示剂,可保证测定有足够的准确度。甲基橙(简写为MO)的pH变色区域是3.1(红)~4.4(黄),酚酞(简写为PP)的pH变色区域是8.0(无色)~9.6(红)。
在指示剂不变的情况下,一定浓度的HCl溶液和NaOH溶液相互滴定时,所消耗的体积之比值VHCl/VNaOH应是一定的,改变被滴定溶液的体积,此体积之比应基本不变。借此,可以检验滴定操作技术和判断终点的能力。
三、主要试剂和仪器
1.HCl溶液 6mol·L—1。
2.固体NaOH。
3.甲基橙溶液 1 g·L—1。
4.酚酞溶液 2 g·L—1 乙醇溶液。
四、实验步骤
1.溶液配制
(1)0.1 mol·L—1 HCl溶液
用洁净量杯量取约17 mL 6mol·L—1 HCl溶液,倒人装有约980 mL水的1 L试剂瓶中,加水稀释至1 L,盖上玻璃塞,摇匀。
(2)0.1mol·L—1 NaOH溶液
称取固体NaOH 4g (如何算得的?), 置于250mL烧杯中,马上加入蒸馏水使之溶解,稍冷却后转入试剂瓶中①,加水稀释至1 L,用橡皮塞塞好瓶口,充分摇匀
2.酸碱溶液的相互滴定
(1)用0.1 mol·L-1 NaOH溶液润洗碱式滴定管2,3次,每次用5~10mL溶液润洗。然后将滴定剂倒人碱式滴定管中,滴定管液面调节至0.00刻度。
(2)用0.1 mol·L-1盐酸溶液润洗酸式滴定管2~3次,每次用5~10mL溶液,然后将盐酸溶液倒人滴定管中,调节液面到0.00刻度。
(3)在250mL锥瓶中加入约20mL NaOH溶液,2滴甲基橙指示剂,用酸管中的HCl溶液进行滴定操作练习。
务必熟练掌握操作。练习过程中,可以不断补充NaOH和HCl溶液,反复进行,直至操作熟练后,再进行(4)、(5)、(6)的实验步骤。
(4)由碱管中放出NaOH溶液20~25 mL于锥形瓶中,放出时以每分钟约10mL的速度,即每秒滴入3~4滴溶液,加入2滴甲基橙指示剂,用0.1 mol·l—1 HCl溶液滴定至黄色转变为橙色③。记下读数。平行滴定三份。数据按下列表格记录。计算体积比VHCl/VNa0H,要求相对偏差在±0.3%以内。
(5)用移液管吸取25.00 mL 0.1 mol·L—1 HCl溶液于250mL锥瓶中,加2~3滴酚酞指示剂,用0.1 mol·L—1 NaOH溶液滴定溶液呈微红色,此红色保持30s不褪色即为终点。如此平行测定三份,要求三次之间所消耗Na0H溶液的体积的最大差值不超过±0.04 mL。
(6)同(5)操作,改变指示剂,选用百里酚蓝—甲酚红混合指示剂。平行测定三份,所消耗Na0H溶液的体积,三次之间的最大差值要求≤±0.04mL。
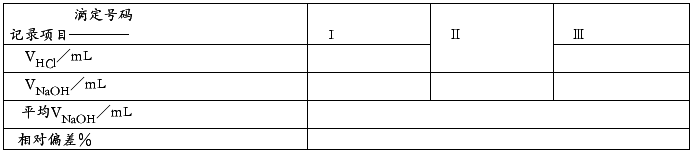
3.滴定记录表格
(1)HCl溶液滴定Na0H溶液(指示剂:甲基橙)

(2)NaOH溶液滴定HCl溶液(指示剂:酚酞)
五、思考题
1.配制NaOH溶液时,应选用何种天平称取试剂?为什么?
2.HCl和NaOH溶液能直接配制准确浓度吗?为什么?
3.在滴定分析实验中,滴定管、移液管为何需要用滴定剂和要移取的溶液润洗几次?滴定中使用的锥形瓶是否也要用滴定剂润洗?为什么?
4.HCl溶液与NaOH溶液定量反应完全后,生成NaCl和水,为什么用HCl滴定NaOH时采用甲基橙作为指示剂,而用NaOH滴定HCl溶液时使用酚酞(或其它适当的指示剂)?
