实验七十八 溶液电导的测定——测HAc的电离平衡常数
预习提问
1、电导法测醋酸的电离平衡常数的测量原理 ?
2、用不同的电导电极测定同一溶液的电导率时所得结果应该怎样?为什么?
3、什么是电导水?测醋酸的电离平衡常数时为何要测电导水的电导率?水越纯,电导率是越大还是越小?
4、实验中影响准确测定结果的因素有那些?
5、我们不知道溶液的大概电导率时首先应如何测量?
6、实验中用移液管移弃溶液时能否先用该溶液润洗?为什么?
思考题
1. 简述电导法测醋酸的电离平衡常数的测量原理。
2. 在电导法测醋酸的电离平衡常数实验中,影响准确测定结果的因素有那些?
3. 用不同的电导电极测定同一溶液的电导率时所得结果应该怎样?为什么?
4. 测溶液的电导时,为了消除极化作用,实验中采取了什么措施?
5. 测定溶液的电导率时为何要用交流电?能否用直流电?
6. 什么是电导水?测醋酸的电离平衡常数时为何要测电导水的电导率?水越纯,电导率是越大还是越小?
7. 我们不知道溶液的大概电导率时首先应如何测量?
8. 在测HAc的电离平衡常数实验中,用移液管移弃溶液时能否先用该溶液润洗?为什么?
9. 在电导法测醋酸的电离平衡常数实验中,为什么要测电导池常数?如何得到该常数?
10. 在电导法测醋酸的电离平衡常数实验中,测电导率时为什么要恒温?实验中测电导池常数和溶液电导率,温度是否要一致?
11. 设计一个实验,用电导法测定难溶盐PbSO4的溶解度,并写出实验方案。
书后思考题
(1)为什么要测电导池常数?如何得到该常数?
(2)测电导时为什么要恒温?实验中测电导池常数和溶液电导率,温度是否要一致?
(3)设计一个实验,用电导法测定难溶盐PbSO4的溶解度,并写出实验方案。
第二篇:电导法测乙酸电离平衡常数
实验六 电导法测定乙酸电离平衡常数
姓名:李昭骏 班级:工艺五班 学号:10031010507
室温:14.5℃ 大气压:100kpa 实验日期: 20##年3月5日
实验仪器:DDBJ-350便携式电导率仪,电导电极,恒温槽,烧杯,锥形瓶,25ml移液管,KCl标液,0.1779mol/LHAc标准溶液。
一、 实验目的
1,掌握电导、电导率、摩尔电导率的概念以及它们之间的相互关系。
2,掌握电导法测定弱电解质电离平衡常数的原理。
二、 实验原理
1, 电离平衡常数Kc的测定原理:CH3COOH—>CH3COO—+H+
α=λm/λ∞; Cλm=λ∞2 Kc /λm﹣λ∞Kc
由上式可测定系列浓度下的λm,将Cλm对1/λm作图,求斜率。
2, 摩尔电导率λm的测定原理:(电导率即电阻率的倒数,用k表示,单位:S.m-1) 定义摩尔电导率:λm=k/c (k为电导率) 对于固定的电导池,电导常数一定,所以可用仪器测出醋酸溶液的电导率,然后用λm=k/c算出摩尔电导率。 (注:λ∞在一定温度下为常数)
三、 实验步骤
1,调节恒温水槽水浴温度为25℃。 2,校准便携式电导率仪的电导池常数:打开电导率仪,在标准KCl溶液中校准;按下校准按键,待温度达恒定,显示屏上数值稳定,即校准完毕。 3,测量醋酸溶液的电导率:标定好电导池常数,将电极清洗干净。将电极插入50mL 0.1779mol/L醋酸溶液中测量电导率;取出25mL溶液,再加入25mL电导水稀释再次测量;如此每次稀释一半的浓度,逐次递减测量五组数据(每组测三次)填入数据记录表格。
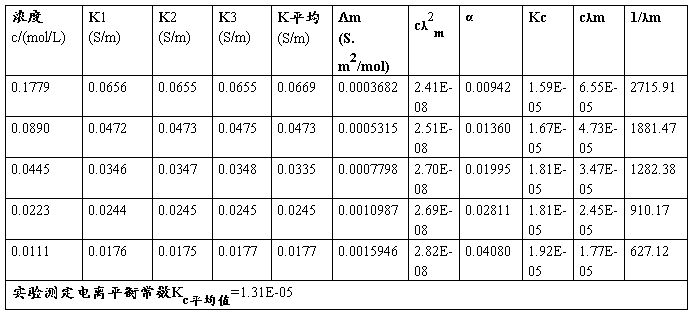
四、 数据处理
实验温度:T=25℃
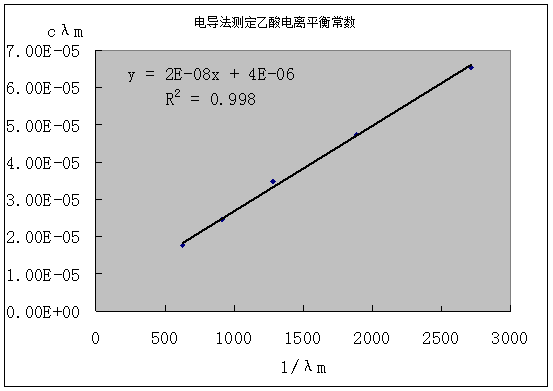
由图知,直线斜率为2×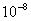 ,又因为斜率表示为
,又因为斜率表示为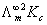 所以可得:
所以可得: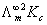 =2×
=2×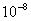 ,得
,得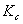 =1.31×
=1.31×
五、注意事项
1.计算∧m和kc时,需注意浓度c单位的区别,详见原理部分。
2.温度对溶液的电导影响较大,因此测量时应保持恒温。
六、思考题:
1.电导池常数是否可用测量几何尺寸的方法确定?
答:不能。测定电导池常数可以用标准溶液测定法,用氯化钾为标准物质;还可以用与标准电极比较法测定。
2.实际过程中,若电导池常数发生改变,对平衡常数测定有何影响?
答:溶液电导一经测定,则?正比于Kcell。即电导池常数测值偏大,则算得的溶液的溶解度、电离常数都偏大,反之,电导池常数测值偏小,则电离常数偏小。
