实验十六 电导法测定氯化银的溶度积和溶解度思考题
1、电导、电导率和摩尔电导率是如何定义的?三者分别以何符号表示?三者之间有何联系和区别?
2、电导池常数K的物理意义是什么?其数值如何测得?
3、在运用公式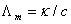 进行有关计算时,
进行有关计算时, 的单位是什么?
的单位是什么?
4、极限摩尔电导率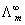 的物理意义和用途分别是什么?
的物理意义和用途分别是什么?
5、对于强、弱电解质,获得其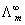 分别有哪几种方法?
分别有哪几种方法?
6、对于强电解质难溶盐,如何理论计算其 ?为什么?
?为什么?
7、难溶盐饱和溶液的电导率就是难溶盐的电导率吗?为什么?
8、简述难溶盐溶解度和溶度积的区别?
9、温度对电解质溶液的电导、电导率和摩尔电导率是否有影响?有何影响?
10、科尔劳施公式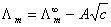 成立的条件是什么?
成立的条件是什么?
11、电导率的测定为何用交流电而不用直流电?
12、简述用DDS-11A型电导率仪测定溶液电导率的步骤?
13、简述用DDS-11A型电导率仪测定AgCl溶解度和溶度积的步骤?
答案:
1、电导G为电阻R的倒数,表示导体的导电能力大小。电导率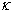 为单位体积导体的电导。摩尔电导率
为单位体积导体的电导。摩尔电导率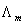 为单位浓度电解质溶液的电导率。三者均反映导体的导电能力,对第二类导体电解质溶液而言,电导对电解质溶液的体积和浓度均没有限制,而电导率和摩尔电导率则分别对电解质溶液有体积限制和浓度限制,分别为单位体积电解质溶液和单位浓度电解质溶液的电导。
为单位浓度电解质溶液的电导率。三者均反映导体的导电能力,对第二类导体电解质溶液而言,电导对电解质溶液的体积和浓度均没有限制,而电导率和摩尔电导率则分别对电解质溶液有体积限制和浓度限制,分别为单位体积电解质溶液和单位浓度电解质溶液的电导。
2、电导池常数K为电导池两极之间距离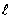 与极板面积A之比值,对于指定的电导池,K为常数。K值可通过测定已知电导率
与极板面积A之比值,对于指定的电导池,K为常数。K值可通过测定已知电导率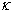 的电解质溶液的电阻R,利用公式K=
的电解质溶液的电阻R,利用公式K=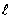 /A=
/A=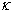 R求得。
R求得。
3、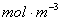 。
。
4、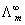 为无限稀电解质溶液的摩尔电导率,由
为无限稀电解质溶液的摩尔电导率,由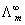 和
和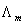 可计算弱电解质稀溶液的电离度
可计算弱电解质稀溶液的电离度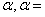
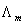 /
/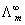 。
。
5、对于强电解质,获得其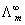 有实验测定和理论计算两种方法,前者为以
有实验测定和理论计算两种方法,前者为以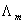 对
对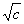 作图,在低浓度下直线在纵轴(即横坐标
作图,在低浓度下直线在纵轴(即横坐标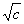 =0时)上的截距,后者为
=0时)上的截距,后者为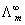 =
=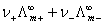 。对于弱电解质则只有如上后者理论计算一种方法。
。对于弱电解质则只有如上后者理论计算一种方法。
6、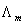 ≈
≈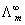 =
=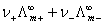 。
。
7、不是,因为难溶盐饱和溶液的电导率为难溶盐的电导率和溶剂水的电导率两部分贡献之和。
8、难溶盐溶解度为一定温度下难溶盐饱和溶液的浓度,而溶度积为难溶盐所电离出来的各种离子浓度之乘积,且各种离子浓度之幂次为一个难溶盐分子所电离出来的相应离子的个数。
9、有影响,三者均随温度升高而增大。
10、强电解质、稀溶液。
11、直流电会引起电解反应发生,甚至还会在电极上析出气体。电解反应发生导致溶液的组成发生改变,因而引起电导率的改变,而气体的析出则加剧电极极化,从而增大溶液电阻,降低其电导率。因此,用直流电测定溶液的电导率时难以获得准确的结果。
12、调零→预热→校正→测量。
13、同上步骤首先测出AgCl饱和溶液的电导率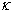 ,然后再进行如下计算:
,然后再进行如下计算:
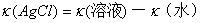
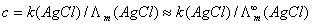
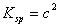 。
。
第二篇:电导法测定难溶盐的溶解度
电导法测定难溶盐的溶解度
一、目的
1. 掌握惠斯顿电桥测定电导的原理和方法
2. 学会电导法测定难溶盐的溶解度
二、基本原理 导体导电能力的大小,常以电阻的倒数1 表示,即: R
1G= (1) R
式中G称为电导,单位是西门子S。
导体的电阻与其长度成正比,与其截面积成反比,即:
?l?R=ρ?? (2) ?A?
ρ是比例常数,称为电阻率或比电阻。根据电导与电阻的关系,则有:
?A?G=k?? (3) ?l?
k称为电导率或比电导k=1
ρ,它相当于长为1m,截面积为1m2导体的电导,其单位是S m-1。
对于电解质溶液,若浓度不同,则其电导也不同。如取1mol电解质溶液来量度,即可在给定条件下就不同电解质溶液来进行比较。1mol电解质溶液全部置于相距为1m的两个平行电极之间,溶液的电导称之为摩尔电导,以λ表示。如溶液的摩尔浓度以c表示,则摩尔电导可表示为:
λ=k (4) 1000c
式中λ的单位是S·m2·mol-1;c的单位是mol·dm-3。λ的数值常通过溶液的电导率k,经(4)式计算得到。而k与电导G(或电阻R)有直接关系,由(3)式可知
k=ll1G 或 k=? AAR
对于确定的电导池来说,l/A是常数,称为电导池常数。电导池常数可通过测定已知电导率的电解质溶液的电导(或电阻)来确定。

图1
溶液的电导通常利用惠斯顿电桥来测定。线路如图所示。其中S为音频信号发生器(本实验使用
;R1、R2和R3是三个可变电阻箱的阻值。RX为待测溶液的阻值;H为示波器。的信号频率为1000Hz)
C1是与电阻R1并联的一个可变电容,用以平衡电导电极的电容。
测定时调节R1、R2、R3和C1,使H无电流通过。此时,表明B、D两点电位相等,电桥达到了平衡。即有
R=R1R3 R2
Rx的倒数即为该溶液电导。
本实验是测定PbSO4的溶解度。首先测定PbSO4饱和溶液的电导,代入(3)式求其电导率(k溶液)。因溶液极稀,必须从k溶液中减去水的电导率(k水)即
kPbSO4=k溶液-k水
因为 λ=k 1000c
则 λ硫酸铅=k硫酸铅1000c
k硫酸铅 式中:c是难溶盐饱和溶液的浓度。由于溶液极稀,λ可视为λ0。因此, c=1000λ0,硫酸铅
与l 相加而得。因温度PbSO4的极限摩尔电导λ0硫酸铅 可以根据离子独立移动定律将l10,Pb2+
212+0,SO42
对溶液的电导有影响,本实验应在恒温下测定。
BaSO4等难溶盐的溶解度,还可以测定弱电解质的电离度和电导的测定不仅可以用来测定PbSO4、
电离常数、盐的水解度等。
(为消除由交流电所引起的极化效应,使用镀铂黑电极,增加电极面积)
三、仪器和试剂
音频讯号发生器 1台 恒温槽 1套
示波器或耳机 1个 可变电阻箱 3个
电导电极(镀铂黑) 1支 锥形瓶(200ml) 4个
0.02 mol·L-1氯化钾溶液 PbSO4(A.R.)
四、操作步骤
1.按图接好线路。调节恒温槽温度至25℃。
2.测定电导池常数
用少量0.02mol/L KCl溶液浸洗电导电极两次,将电极插入盛有适量0.02mol/L KCl溶液的锥形瓶中,液面应高于电极铂片2mm以上。将锥形瓶放入恒温槽内,十分钟后测定电导,然后换溶液再测定两次,求平均值。
3.测定PbSO4溶液的电导率
将约1g固体PbSO4放入200mL锥形瓶中,加入约100mL重蒸馏水,摇动并加热至沸腾。倒掉清液,以除去可溶性杂质。按同样方法重复两次。再加入约100mL重蒸馏水,加热至沸腾,使之充分溶解。然后放在恒温槽中,恒温20分钟使固体沉淀,将上层溶液倒入一干燥的锥形瓶中(溶液中不能含有
,恒温后测其电导,然后换溶液再测两次,求平均值。 任何悬浮物,否则将影响实验结果,为什么?)
4.测定重蒸馏水的电导率
取约100mL重蒸馏水放入一干燥的锥形瓶中,待恒温后,测电导三次,求平均值。
五、数据记录和处理
实验温度:25℃
1.电导池常数的测定
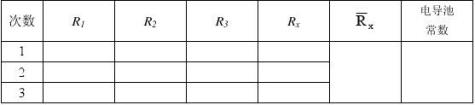
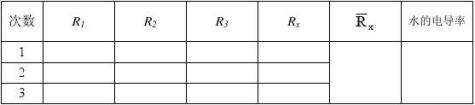
2
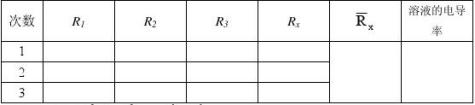
3λ0硫酸铅k硫酸铅=2.87×10-3 S·m-1
文献值:c=1.49×10-4 mol/L
实验关键:
1.硫酸铅要充分煮沸,除去其中可溶性杂质,否则硫酸铅溶解度的测定值将大于其真实值。
2.电解质溶液电导的温度系数较大,温度变化1℃,温度系数改变约2%。所以,测量时应注意保持恒温条件。
