电导法测定难溶盐的溶解度
一、实验目的
1.掌握惠斯顿电桥测定电导的原理及方法
2.掌握电导测定的原理和电导仪的使用方法。
3.学会用电导法测定难溶盐的溶解度
二、基本原理
1、电导法原理
导体导电能力的大小常以电阻的倒数去表示,即有
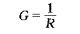
式中G称为电导,单位是西门子S。
导体的电阻与其长度成正比与其截面积成反比即:
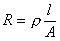
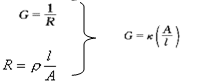 ρ是比例常数,称为电阻率或比电阻。根据电导与电阻的关系则有:
ρ是比例常数,称为电阻率或比电阻。根据电导与电阻的关系则有:
κ称为电导率或比电导,单位:S·m-1
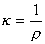
对于电解质溶液,浓度不同则其电导亦不同。如取1mol电解质溶液来量度,即可在给定条件下就不同电解质溶液来进行比较。lmol电解质溶液全部置于相距为1m的两个平行电极之间溶液的电导称之为摩尔电导,以λ表示之。如溶液的摩尔浓度以c表示。则摩尔电导可表示为
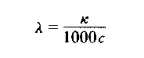
式中λ的单位是S.m2.mol-1,c的单位是mol.L-1。λ的数值常通过溶液的电导率k式计算得到。
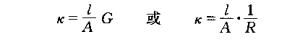
对于确定的电导池来说l/A是常数,称为电导池常数。电导池常数可通过测定已知电导率的电解质溶液的电导(或电阻)来确定。
本实验测定PbSO4的溶解度,首先测定PbSO4饱和溶液的电导率,因溶液极稀,必须从k溶液中减去水的电导率(kH20):
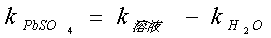
因为: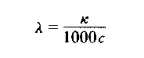
则: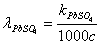
C 是难溶盐的饱和溶解度,由于溶液极稀,λ可视为λ0 ,因此:
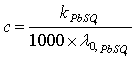
PbSO4的极限摩尔电导λ0可以根据离子独立移动定律得:
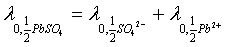
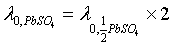
其中25℃时的 可查表得到。
可查表得到。
2、惠斯顿电桥测电阻的原理
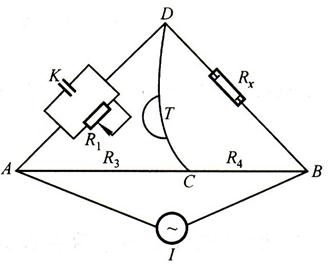
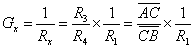
三、仪器和试剂
DDS—307型电导仪1台; 玻璃恒温水浴 1台;
电导电极(铂黑) 1支; 锥形瓶100ml 3个
PbSO4饱和溶液 重蒸水
四、实验步骤
1、连接好电路
2、测定重蒸水的电导率
取少量重蒸水,浸洗电导电极两次中,将电极插入盛有适量重蒸水的锥形瓶中,液面应高于电极铂片2mm以上。将锥形瓶放入恒温水槽中,十分钟后测定电导,然后换溶液再测两次,求平均值。
3、测定PbSO4溶液的电导率
取少量配制好的饱和PbSO4溶液,浸洗电导电极两次中,将电极插入盛有适量饱和PbSO4溶液的锥形瓶中,液面应高于电极铂片2mm以上。将锥形瓶放入恒温水槽中,十分钟后测定电导,然后换溶液再测两次,求平均值。
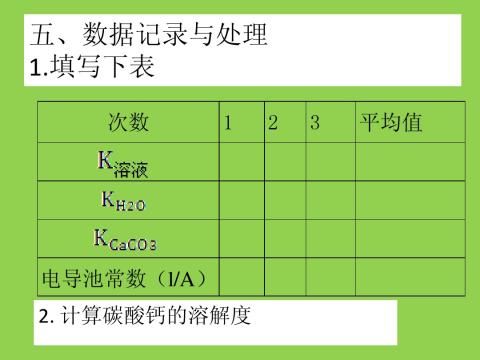
五、数据处理
电极常数: 0.969 气压: 729.50 mmHg 室温: 22 ℃ 实验温度: 25 ℃
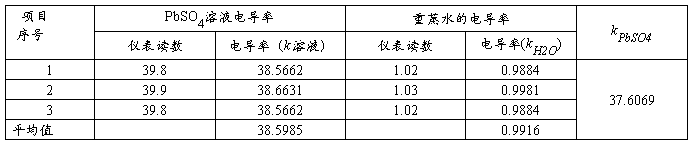
查表,得25℃时: 80.0 S·cm2·mol-1
80.0 S·cm2·mol-1
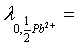 70.3 S·cm2·mol-1
70.3 S·cm2·mol-1
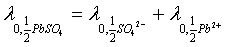 =70.3+80.0=150.3 ×10-4 S·m2·mol-1
=70.3+80.0=150.3 ×10-4 S·m2·mol-1
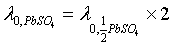 =150.3×2=300.6×10-4 S·m2·mol-1
=150.3×2=300.6×10-4 S·m2·mol-1
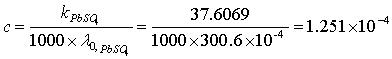 mol/L
mol/L
文献值为:1.591×10-4 mol/L
相对误差=(1.251×10-4-1.591×10-4)/ (1.591×10-4)=-23.44%
第二篇:电导法测难溶盐的溶解度