实验 酶促反应动力学
————蔗糖酶米氏常数的测
【目的要求】
1.了解酶促动力学研究的范围。
2.以蔗糖酶为例,掌握测定米氏常数(Km)
【实验原理】
在酶促反应中,当反应体系的温度、pH和酶浓度恒定时,反应初速度(v)则随底物
浓度[S]的增加而加速,最后达到极限,称为最大反应速度(v)。Michaelis和Menten
根据反应速度与底物浓度的这种关系,推导出如下方程:
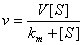
此式称为米氏方程,式中Km称为米氏常数,按此方程,可用作图法求出Km。方法有:
1.以v[S]作图
由米氏方程可知,v=V/2时,Km=[S]即米氏常数值等于反应速度达到最大反应速度一半时所需底物浓度。因此,可测定一系列不同底物浓度的反应速度v,以v对[S]作图。当v=V/2时,其相应底物浓度即为Km。
2.以1/v对1/[S]作图
取米氏方程的倒数式:


以1/v对1/[S]作图可得一直线,其斜率为Km/V,截距为1/V。若将直线延长与横轴相交,则该交点在数值上等于—l/Km。

本实验以蔗糖为底物.利用一定量蔗糖酶水解不同浓度蔗糖所形成的产物(葡萄糖和果糖)的量来计算蔗糖酶的Km值。葡萄糖和果糖能与3,5—二硝基水杨酸试剂反应,生成桔红色化合物,可于520nm处比色测定之。
【试验材料】
1.试剂
(1)标准葡萄糖溶液:准确称取100mg葡萄糖溶于少量饱和的苯甲酸溶液(0.3%),再转移到100ml容量瓶中,用饱和苯甲酸溶液稀释到刻度,混匀,即得浓度为1mg/m1的标准葡萄糖溶液。冰箱贮藏可长期保存;
(2)pH4.5的0.1mol/L醋酸缓冲液:取lmol/L醋酸钠溶液43m1及lmol/L醋酸溶液57m1,稀释至1000m1即得;
(3)pH4.5的10%蔗糖溶液:准确取l0g蔗糖溶于少量pH4.5的0.1mol/L醋酸缓冲液,转移到100ml容量瓶中,用同样缓冲液稀释到刻度备用;
(4)3,5—二硝基水杨酸试剂:溶液I:4.5%NaOH溶液300m1,1%3,5一二硝基水杨酸溶液880m1及酒石酸钾钠(KNaC4O6·4H20)255g三者一起混合均匀。
溶液Ⅱ:取结晶酚10g及lo%NaOH溶液22m1,加蒸馏水稀释成100ml,混匀。
溶液Ⅲ:取6.9gNaHSO3溶于64ml溶液n中。
将溶液皿和溶液I混合,激烈振摇混匀,即得3,5—二硝基水杨酸溶液,放置一周后备用。
(5)酵母蔗糖酶溶液:称取鲜酵母l0g于研钵中,加少量细砂及10一15ml蒸馏水研磨。磨细后置冰箱中,过滤,滤液加2—3倍体积冷丙酮,搅拌均匀后离心,沉淀用丙酮洗两次,真空干燥得固体粉末状酶,再溶于100ml蒸馏水,即得酶溶液。若有不溶物可用离心法除去。
该酶液活力以6—12单位为佳。蔗糖酶活力单位的定义为:在一定条件下反应5min,每产生lmg葡萄糖所需要的酶量。备用。
2.器材
(1)100m1三角烧瓶2只;
(2)研钵1只;
(3)50m1及100m1容量瓶各1只;
(4)离心机1台(4000rpm);
(5)糖管8支;
(6)恒温水浴1台;
(7)吸量管:1.0ml×2支;
(8)秒表1只;
(9)72l型分光光度计1台。
【实验方法】
1.标准曲线的绘制
取干净糖管6支,如下表所示添加试剂。

加毕混匀.于沸水中准确煮5min,取出用自来水冷却3min,稀释至25ml,混匀后以零号管调零点,于520nm处测定吸光度。以葡萄糖含量为横坐标,以吸光度为纵坐标作图。
2.根据活力选择酶浓度
将10%蔗糖溶液稀释成pH4.5的6.5%的溶液,取此溶液5m1于试管中,共加两管。
将两管同时置于25℃水浴中保温5min,然后向管中加入蔗糖酶溶液1.0ml,立即混匀,
同时用秒表计时,准确反应5min后,立即加入5ml0.1mol/LNaOH溶液终止酶反应。另
一管先加入5.0ml0.11mol/LNaOH溶液,再加入蔗糖酶溶液1.0ml(此为对照管)。
取干净糖管3支,第l、2管分别加入上述反应液各1.0ml及水各1.0m1,第3管加蒸馏水2.0ml,然后各管均加3.0ml二硝基水杨酸溶液。置沸水浴中煮5min,取出后经自来水冷却3min,加水至25m1,混匀,以第3管调零点,于520nm处测吸光度值。以测定管的吸光度值减去对照管吸光度值,求得的差值从标准曲线上查得相应的葡萄糖含量,并乘以ll,即为每1ml酶溶液的活力。
测定管中因酶催化水解而产生的葡萄糖含量以在0.4—1.6mg之间为佳,过高或过低均应适当改变蔗糖酶溶液的浓度或反应液用量后再测。
3.底物浓度对酶促反应速度的影响——米氏常数购测定
取试管7支,按下表所示加入试剂。
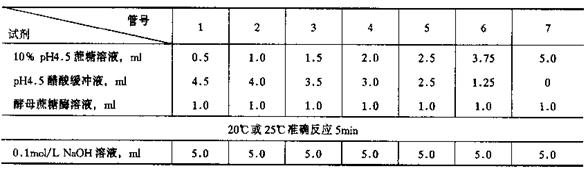
当加完蔗糖溶液及pH4.5醋酸缓冲液后,均放置室温或恒温水浴(20℃或25℃)保
温5min,再分别依次向各管加入蔗糖酶溶液1.0ml,立即摇匀.记录时间。准确反应
5min,再准时加入0.1mol/L的NaOH溶液,立即摇匀,以终止反应。
测定管反应完成后,取8支洁净糖管,前7支分别加入相应的上述反应液各1.0ml及
蒸馏水各1.0ml,第8支糖管加入2.0ml蒸馏水作空白,然后各管均加入3.0ml二硝基水
杨酸溶液,沸水浴5min。取出用自来水冷却3min,稀释到25m1,混匀,于520nm处比色
测定并记录吸光度值。
对照管的测定与测定管的操作相同。
【结果处理】
根据各测定管的吸光度值(需减去相应对照管的吸光度值),从标准曲线上查出相应的还原糖毫克数(以在0.4一1.6mg范围内为佳,否则应调整反应液用量后重新测定),再乘以11,即得各管的产物量,然后分别计算各反应管相应的[S]、l/[S]、v及1/v,并作出v—[S]及1/v—1/[S]曲线。再根据所作的两种动力学曲线,分别求出酵母蔗糖酶的Km值,并加以比较。
上述数据可记录在下表中。
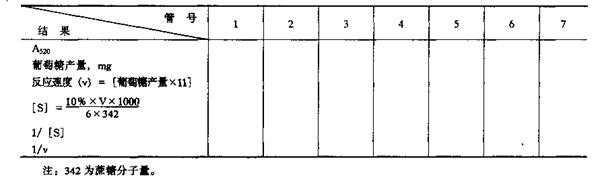
酵母蔗糖酶的提取
实验原理:
蔗糖酶主要存在于酵母中,但工业上通常从酵母中制取。酵母蔗糖酶系胞内酶,提取时细胞破碎或菌体自溶。常用的提纯方法有盐析、有机溶剂沉淀、离子交换和凝胶柱层析。以此可得到较高纯度的酶。
细胞破壁的几种方法
1、高速组织捣碎:将材料配成稀糊状液,放置于筒内约1/3体积,盖紧筒盖,将调速器先拨至最慢处,开动开关后,逐步加速至所需速度。
2、玻璃匀浆器匀浆:先将剪碎的组织置于管中,再套入研杆来回研磨,上下移动,即可将细胞研碎,此法细胞破碎程度比高速组织捣碎机为高,适用于量少和动物脏器组织。
3、反复冻融法:将细胞在-20度以下冰冻,室温融解,反复几次,由于细胞内冰粒形成和剩余细胞液的盐浓度增高引起溶胀,使细胞结构破碎。
4、超声波处理法:用一定功率的超声波处理细胞悬液,使细胞急剧震荡破裂,此法多适用于微生物材料。
5、化学处理法:有些动物细胞,例如肿瘤细胞可采用十二烷基磺酸钠(SDS)、去氧胆酸钠等细胞膜破坏,细菌细胞壁较厚,可采用溶菌酶处理效果更好。
有机溶剂沉淀法即向水溶液中加入一定量的亲水性的有机溶剂可降低溶质的溶解度使其沉淀被析出。
三、试剂:
啤酒酵母 、 二氧化硅 、甲苯(使用前预冷到0℃以下)、去离子水(使用前冷至4℃左右)、1mol / L 醋酸 、95%乙醇
四、仪器:
研钵1个、离心管3个 、 3. 滴管3个、量筒50ml 1个、水浴锅1个、恒温水浴、烧杯100ml 2个、广泛pH试纸、高速冷冻离心机
四、操作步骤:
1. 提取
(1)准备一个冰浴,将研钵稳妥放入冰浴中。预先在冰箱中冷却20g干酵
母和10g二氧化硅。
(2)将20g干酵母粉和10g二氧化硅,放入研钵中。量取预冷的甲苯30ml缓慢加入酵母中,边加边研磨成糊状,约需60分钟。研磨时用显微镜检查研磨的效果,至酵母细胞大部分研碎。
(3)缓慢加入预冷的40ml去离子水,每次加2ml左右,边加边研磨,至少用30分钟。以便将蔗糖酶充分转入水相。
(4)将混合物转入两个离心管中,平衡后,用高速冷离心机离心,4℃,10000rpm,10min。如果中间白色的脂肪层厚,说明研磨效果良好。用滴管吸出上层有机相。
(5)用滴管小心地取出脂肪层下面的水相,转入另一个清洁的离心管中,4℃,10000rpm,离心10min。
(6)将清液转入量筒,量出体积,留出1.5ml测定酶活力及蛋白含量。剩余部分转入清洁离心管中。
(7)用pH试纸检查清液pH,用1mol / L 醋酸将pH调至5.0,称为“粗级分I”。
第二篇:实验五 酶促反应动力学实验
实验五 酶促反应动力学实验
——温度和离子对酶活性的影响
【实验目的】
1、了解温度对酶活性及酶促反应速度的影响,加深对酶特性的认识。
2、了解离子对酶活性及酶促反应速度的影响,加深对酶特性的认识。
【实验原理】
1、每种酶都有其最适温度,高于或低于此温度酶的活性都降低。一般而言,若酶处于过高的温度环境中,会使酶活性永久丧失;而若处于极低温度的环境中只会使酶活性受到抑制,一旦温度适宜,酶又会全部或部分的恢复其活性。
2、酶的活性常常受某些物质的影响,有些物质能使酶的活性增加,称为酶的激活剂;有些物质能使酶的活性降低,称为酶的抑制剂。Cl-是唾液淀粉酶的激活剂。其它的阴离子,如Br-、NO3-和I- 对该酶也有激活作用,但较微弱。而Cu2+对唾液淀粉酶具有抑制作用。激活剂和抑制剂影响酶活性的剂量是很少的,并且常具有特异性。
就本实验,低浓度CI-可以增加酶活性,高浓度的CI-或者低浓度的Cu2+则会抑制酶活性,同时低浓度的Na+、SO42-等对酶活性没有影响。激活剂的作用机制是多种多样的,可能是作为辅酶或辅基的一个组成部分,也可以直接作为酶活性中心的构成部分。
【实验用品】
1、仪器和器材:冰箱、恒温水浴锅、紫外分光光度计、试管和试管架、移液枪及枪头、胶头滴管、烧杯
2、试剂:1)PH6.8的缓冲液:量取15.45ml的0.2M磷酸氢二钠和4.55ml的柠檬酸混合摇匀即可。
2)0.5%淀粉的0.5%氯化钠溶液:0.5g可溶性淀粉和0.5g氯化钠,溶于100ml蒸馏水(需加热)。
3)碘液
4)1M HCl溶液
5)1M NaOH溶液
6)稀释100倍的唾液
7)冰水浴
8) 1%NaCI溶液
9) 0.1%CuSO4溶液
10)0.1%淀粉液
【实验内容】
(一)温度对酶活性的影响
1.制管和预温:
由于本实验对恒温反应要求较高,故每个温度梯度使用两支试管,分别标记为A管和B管,同时欲温底物与酶。A管加入PH6.8的缓冲液和0.5%淀粉液;B管使用移液枪加入稀释100倍的唾液,相对应的两支试管置于设定的温度下预温5min。
取12支洁净试管,参照下表加入试剂:
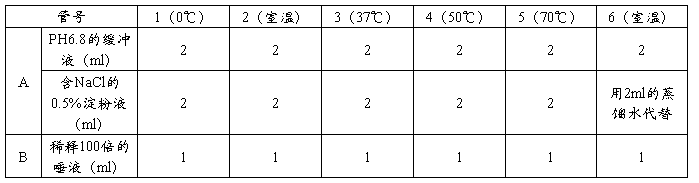
*6号管为对照组(比色时作为0号管),置于室温,且淀粉液用蒸馏水代替
2.混合A、B管:
将1号A管试剂迅速加入温度对应的B管中(为了最大限度保证酶的量),此时为计时的起点(使用秒表),摇匀后放回对应温度继续水浴。注意:转移A管试剂前需将其摇匀。
3.时间控制
然后每隔1min或2min(时间自定)按上步操作依次把2、3、4、5、6号的A、B管混合 ,严格控制好时间。
4.中止反应
准确反应13min,向1号管加入2滴1M HCl溶液,立即混匀,中止反应,按上一步的顺序和时间间隔依次对各管进行操作,并移至试管架。后再各用2滴1M NaOH溶液中和每管。
5.显色
在每管中各加入2ml 0.03175g/L碘液并混匀,观察现象。
6.比色
若不同温度梯度间现象差别不明显,则进行比色,通过光密度值来比较。
(二)离子对酶活性的影响
取3支洁净的试管,编号后按下表操作:

【结果处理】
记录现象(或比较吸光度值),做出合理分析。
【注意事项】
严格注意时间的控制及各物质的添加量。
【思考题】
1、如果某同学(没有严格按照教案步骤)做出的实验结果为唾液淀粉酶的最适温度为70度,请分析他得出这样的结果的可能原因。
2、为什么加入淀粉后有试管内颜色显现为红色?
