关于硫酸亚铁铵制备过程中亚铁离子被氧化问题的讨论
完成日期:2015/11/29
一、 摘要
本文从加料、控制反应时间两大角度总结了制备硫酸亚铁铵实验中防止亚铁离子被氧化的措施,并就哪一环节亚铁离子最容易被氧化进行了讨论。加料包括通过使酸过量调节体系pH、使用去离子水减少溶解氧两方面;控制反应时间包括制备硫酸亚铁时加热至无大量气泡产生即进行减压过滤、配制近饱和硫酸铵溶液缩短蒸发时间两方面。关于Fe2+最容易被氧化的环节,本文将从是否有氧气或铁粉、反应温度和时间等角度进行探讨。
二、 前言
Fe(II)即使处于固态也容易被空气氧化,在配制硫酸亚铁铵的水溶液时,必须通过除氧加酸等措施降低其被氧化程度。防止Fe2+被氧化的措施都有哪些?这些措施有什么意义?哪一环节Fe2+最容易被氧化?本文对此进行了讨论。
三、 内容
1. 对防止Fe2+被氧化措施的总结
(1) 加料
A. 使酸过量调节体系pH
制备硫酸亚铁时,加入4g铁粉、15mL去离子水和15mL6mol·L-1硫酸,初始c(H+)=15×6×2/(15+15)=6 mol·L-1;
加热至无大量气泡产生时(停止加热进行减压过滤),剩余铁粉约为0.1g,
参与反应的硫酸量=反应的铁量=(4-0.1)/56=0.070mol
 若忽略溶液中水的蒸发和酸气(SO2和SO3)的产生,此时c(H+)=(15×10-3×6-0.070) ×2/(30×10-3)=1.3mol·L-1;
若忽略溶液中水的蒸发和酸气(SO2和SO3)的产生,此时c(H+)=(15×10-3×6-0.070) ×2/(30×10-3)=1.3mol·L-1;
加入近饱和硫酸铵溶液时,设室温为20℃,硫酸铵的溶解度为75.4g/100g水,按n(FeSO4):n((NH4)2SO4)=1:1的比例,
应加入的硫酸铵质量为:(4-0.1)×132/56=9.2g;
加入的近饱和溶液体积为9.2×100/75.4=12.2mL;
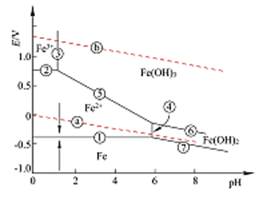
加入后溶液的c(H+)=1.3×30/(30+12.2)=0.92mol·L-1; Fe-H2O体系的E-pH图
蒸发浓缩至溶液表面出现少量晶体时,目测溶液量约为30mL,加入约10mL去离子水后,溶液中的c(H+)约为1.0mol·L-1 ;
由以上计算可知,在整个制备硫酸亚铁铵的过程中,溶液的酸性始终较强,
由上图可知,酸性条件下Fe(II)与氧气反应的E较小,故使酸过量可有效防止Fe(II)被氧化。
B.使用去离子水减少溶解氧
在配制硫酸铵溶液及最后加入10mL左右去离子水时,选用除氧去离子水减少溶解氧,防止Fe(II)被氧化。
(2) 控制反应时间
A. 制备硫酸亚铁时加热至无大量气泡产生即进行减压过滤
此时,溶液中仍有铁粉残余,Fe+Fe3+==Fe2+,E=E(Fe3+/Fe2+)-E(Fe2+/Fe)=0.771-(-0.44)=1.211V,该反应较容易进行,可有效防止Fe(II)被氧化。
B. 配制近饱和硫酸铵溶液
硫酸铵虽然溶解度较大,但是溶解很慢。本实验采取根据溶解度计算后配制近饱和溶液的方法,主要目的是减少蒸发浓缩时的溶液量,从而减少蒸发时间,降低Fe(II)被氧化的可能。
2. 关于Fe2+最容易被氧化的环节的讨论


制备硫酸亚铁后用KSCN检测Fe3+浓度 蒸发浓缩后用KSCN检测Fe3+浓度
根据实验中各环节后KSCN的检测结果,我们认为蒸发结晶环节中Fe3+最容易被氧化。原因如下:

由此可以看出,蒸发浓缩过程温度最高,反应时间最长,与氧气接触,且没有铁粉的还原作用。在整个过程均呈强酸性的条件下,Fe2+在该过程中最容易被氧化。
四、 结论
经过讨论,我们得出结论,本实验中防止Fe2+被氧化的措施分加料(酸过量和使用去离子水)和控制反应时间(控制铁和硫酸反应时间、配制近饱和硫酸铵溶液)两大方面,且Fe2+在蒸发浓缩过程中最容易被氧化。
五、 小组讨论分工
第二篇:北大物理化学实验室开设实验报告
陕西师范大学化学与化工学院
物理化学实验报告
班级
姓名
学号
目 录
实验一
燃烧热的测定 2
实验二
黏度法测定水溶性高聚物相对分子质量 4
实验三
旋光法测定蔗糖转化反应的速率常数 6
实验四
丙酮碘化反应速率常数及活化能的测定 8
实验五
凝固点降低法测定萘的摩尔质量 10
实验六
二组分固—液相图的测绘 12
年 月 日 评定:
姓名: 学号:
年级: 专业:
室温: 大气压:
一、实验名称:燃烧热的测定
二、实验目的
三、实验原理
四、实验数据及处理:
(一)热量计的水当量的测定
相关数据:
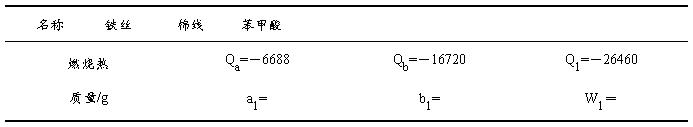
1. 作出苯甲酸燃烧的雷诺校正图,由图中得出燃烧前后温度升高
DT1=
2. 求热量计的水当量C计:(r=1g/cm3,C水=4.184J /g ×℃)
C计=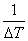 (-Q1W1-Qa× a1-Qb× b1)-3000r C水
(-Q1W1-Qa× a1-Qb× b1)-3000r C水
(二) 萘的燃烧热的测定
相关数据:

1. 萘燃烧的雷诺校正图,由图中得出燃烧前后温度升高
DT2=
2. 求萘的恒容燃烧热Qv(kJ× mol-1)
Qv=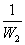 [-Qa× a2-Qb× b2-(3000r C水+C计) ×DT2]
[-Qa× a2-Qb× b2-(3000r C水+C计) ×DT2]
五、讨论思考
1. 如何由萘的恒容燃烧热Qv(kJ× mol-1),求萘的恒压燃烧热Qp(kJ× mol-1),Qv与Qp的关系式中Dn是何含义,Dn =?
2. 该实验成败的关键是什么?从结果看,你做得如何?
年 月 日 评定:
姓名: 学号:
年级: 专业:
室温: 大气压:
一、实验名称:黏度法测定水溶性高聚物相对分子质量
二、实验目的
三、实验原理
四、实验数据及处理:
1. 由实验测得的溶剂流出时间t0和不同浓度溶液流出时间t计算hr,hsp,hsp/c和(lnhr)/c
溶剂流出时间t0=
hr=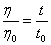 , hsp=hr-1
, hsp=hr-1
表1 聚乙二醇溶液的各种粘度

2. 以ln hr/c及hsp/c分别对c作图,并作线性外推至c=0处,求出[h],并附图。
由图得[h]=
3. 计算聚乙二醇的黏均分子量
250C时聚乙二醇的常数:K=156×10-6m3·kg-1,α=0.50,
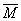 h=0.019~0.1×104
h=0.019~0.1×104
求算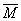
五、讨论思考
1. 高聚物溶液的hr,hsp,hsp/c和[h]的物理意义是什么?
2. 分析hsp/c~ c及(lnhr)/c~ c作图缺乏线性的原因。
年 月 日 评定:
姓名: 学号:
年级: 专业:
室温: 大气压:
一、实验名称:旋光法测定蔗糖转化反应的速率常数
二、实验目的
三、实验原理
四、实验数据及处理:
1. 蔗糖浓度: HCl浓度:
2. 完成下表: =
=
表1 蔗糖转化反应旋光度的测定结果

五、作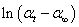 ~ t图,求出反应速率常数k及半衰期t1/2
~ t图,求出反应速率常数k及半衰期t1/2
求算过程:
六、讨论思考:
1. 配制蔗糖溶液时称量不够准确,对测量结果有否影响?
2. 混合蔗糖溶液和盐酸溶液时,可否将蔗糖溶液加到盐酸溶液中去?为什么?
年 月 日 评定:
姓名: 学号:
年级: 专业:
室温: 大气压:
一、实验名称:丙酮碘化反应速率常数及活化能的测定
二、实验目的
三、实验原理
四、实验数据及处理:
根据计算机记录的实验数据,作图并求得反应速率常数k:
五、讨论思考:
1. 本实验中,丙酮碘化反应按几级反应处理,为什么?
2. 分析影响本实验结果的误差有哪些?
年 月 日 评定:
姓名: 学号:
年级: 专业:
室温: 大气压:
一、实验名称:凝固点降低法测定萘的摩尔质量
二、实验目的
三、实验原理
四、实验数据及处理:
1. 由实验得凝固点的测定结果
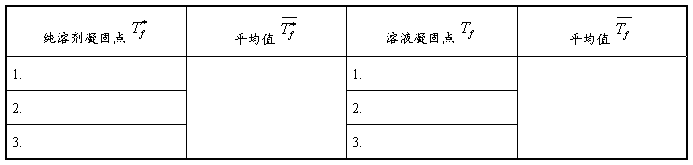
2. 其他相关物理量的测定:
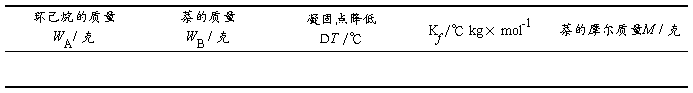
计算过程:萘的摩尔质量M及其相对误差DM的计算过程
五、讨论思考:
1. 加入溶剂中的溶质质量应如何确定?加入量过多或太少会有何影响?
2. 根据你的测定结果,分析实验误差的主要原因?
年 月 日 评定:
姓名: 学号:
年级: 专业:
室温: 大气压:
一、实验名称:二组分固—液相图的测绘
二、实验目的
三、实验原理
四、实验数据及处理:
1. 根据计算机记录各组分温度数据绘制步冷曲线
2. 根据步冷曲线绘制Sn—Bi相图
四、讨论思考
1. 对于不同组分混合物的步冷曲线,其步冷曲线都有什么不同,试解释之。
2.对于含有粗略相等的二组分混合物,步冷曲线上的第一个拐点不易确定,而其低共熔点温度却可以准确测定。相反,对于其中一个组分含量很少的样品,第一个拐点可以准确测定,而第二个拐点则较难测定,试从相率的角度及相关原因解释之。
