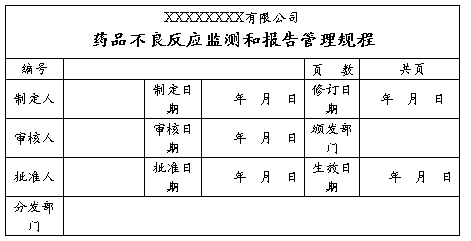
1.主题内容与适用范围
1.1本标准规定了药品不良反应监测报告管理,规范药品不良反应监测、调查、处理、上报程序的管理内容与要求,
1.2本标准适用于药品不良反应监测报告的管理。
2.职责
2.1销售部、质保部对本标准的执行负责。
3.1.1应质保部经理指定专门机构或人员负责管理。
2.2质保部经理负责对本标准的执行情况进行检查、监督与管理。
3.管理内容与要求
3.1药品不良反应的定义
3.1.1 药品不良反应主要是指:合格药品在正常用法用量下,出现的与用药目的无关的或意外的有害反应。包括副作用、毒性作用、后遗效应、继发反应、特异遗传素质等。
3.1.2 新的药品不良反应是指:药品使用说明书或有关文献资料上未收载的不良反应。
3.1.3 可疑不良反应是指:怀疑而未确定的不良反应
3.2药品不良反应基本要求:
3.2.1对用户的药品质量投诉和药品不良反应应有详细记录并及时调查处理。对药品不良反应应及时向当地药品监督管理部门报告。
3.2.2药品不良反应监测和报告应严格执行《药品不良反应报告和监测管理办法》。
3.3药品不良反应监测报告范围
3.3.1上市五年以内的药品(包括进口不到5年的药品)和列为国家重点监测的药品,报告该药品引起的所有可疑不良反应,即所有的不良反应和不良事件或不良经历(ADE)(即较轻微的反应)及药物治疗期间所发生的任何意外事件或非正常的现象。
3.3.2 上市五年以上的药品,主要报告该药品引起的严重、罕见的不良反应。对已知的比较轻微的副作用不列入报告范围。
3.3.3新药监测期已满的药品,报告该药品引起的新的和严重的不良反应。
3.4管理程序与要求
3.4 .1药品不良反应管理的组织:公司指定质量保证部为企业药品不良反应管理专门机构,并成立不良反应监测小组,由质量保证部、研发部、生产部相关技术人员与药品销售人员组成不良反应监测报告小组,并指定专人(QA人员)负责监测报告本公司上市销售产品的不良反应。由质量受权人担任小组组长,负责药品不良反应监测和报告。
3.4 .2 药品不良反应的收集方式
3.4 .2.1 用户(患者、医生、医院)来信、来访和投诉。
3.4 .2.2 用户访问、用户座谈会。
3.4 .2.3 医药销售会议、定货会议和在国外发生的该药品不良反应。
3.4 .2.4 国内外信息刊物上报道的。
3.4.2发现可能与用药有关的不良反应,不良反应监测小组应详细记录、调查、分析、评价、处理,并填写《药品不良反应/事件报告表》,每季度集中向所在地的省、自治区、直辖市药品不良反应监测中心报告,其中新的或严重的药品不良反应应于发现之日起15日内报告,死亡病例须及时报告。
3.4.3发现群体不良反应,应立即向所在地的省、自治区、直辖市(食品)药品监督管理局、卫生厅(局)以及药品不良反应监测中心报告。
3.4.4凡接到用户对药品不良反应的报告,不良反应监测小组应立即跟踪调查,并及时按《药品不良反应报告和监测管理办法》填写 “药品不良反应/事件报告表”,按3.4.2条报告。
3.4.5药品生产企业除按3.4.2条规定报告外,还应以《药品不良反应/事件定期汇总表》的形式进行年度汇总后,向所在地的省、自治区、直辖市药品不良反应监测中心报告。对新药监测期内的药品,每年汇总报告一次; 对新药监测期已满的药品, 在首次药品批准证明文件有效期届满当年汇总报告一次,以后每5年汇总报告一次。
3.4.6不良反应的调查应在接到用户报告或发现之日起的七个工作日内做出处理。
3.4.7药品不良反应报告由不良反应监测小组负责记录报告。
3.4.8《药品不良反应/事件报告表》的填报内容应真实、完整、准确。
3.4.9对本单位生产、经营、使用的药品所发生的不良反应,不良反应监测小组组长应组织相关人员进行分析、评价,并应采取有效措施减少和防止药品不良反应的重复发生。
3.4.10所有不良反应相关文件均由质保部归档保存。
3.4.11新的、严重的药品不良反应/事件病例报告要求药品生产企业报告要求:
①填报《药品不良反应/事件报告表》;
②产品质量检验报告;
③药品说明书(进口药品还须报送国外药品说明书);
④产品注册、再注册时间,是否在监测期内(进口药是否为首次获准进口5年内);
⑤产品状态(是否是国家基本药物、国家非处方药、国家医疗保险药品、中药保护品种);
⑥国内上年度的销售量和销售范围;
⑦境外使用情况(包括注册国家、注册时间);
⑧变更情况(药品成分或处方、质量标准、生产工艺、说明书变更情况);
⑨国内外临床安全性研究及有关文献报道情况;
⑩除第1、2项以外,其他项目一年之内如无变更,可以免报。
3.5 不良反应的调查
3.5.1 一经发现可疑的不良反应,需进行详细记录、调查。并保管好该批药品。
3.5.2 组织有关专业人员进行分析研究,确定是药品不良反应,还是药品质量问题。如无法确定是药品质量问题则一律以药品不良反应上报。
3.5.3 填写药品不良反应报告表(药品不良反应调查及处理单、国家药品监督管理局发放的药品不良反应报告表)。
3.6 不良反应的报告时限
3.6.1 上市5年以内的药品(包括新药和进口药)应追踪药品的安全性和有效性,并随时收集所有可疑不良反应病例,必须每三个月向省市药品不良反应监测中心报告一次该产品所有的不良反应(ADR)和不良事件或经历(ADE),包括其说明书上已经注明的不良反应。
3.6.2 无论是新药还是老药出现的严重、罕见或新的不良反应病例,须用快速有效的方式快速报告,最迟不超过15个工作日报告给省、市药品不良反应监测中心,必要时可以越级报告。
3.7 药品不良反应的资料保密
3.7.1 未经国家药品监督管理局公布的药品不良反应监测,统计资料,不得向国内外机构、组织、团体和个人提供和引用。
3.8 药品不良反应的处理
3.8.1 出现药品可疑不良反应的,应立即向省市药品不良反应监测中心报告。
3.8.2 对出现严重的药品不良反应,该批产品应立即停止销售,并责成营销部按《药品召回管理规程》对该批已上市销售的产品和相关批号的产品实施召回。
3.8.3 对不良反应受害者,应及时慰问、治疗,并给予必要的补助。
3.8.4 对该药品的生产工艺规程、质量标准进行一次分析研究。
3.8.5 对产品说明书进行修改并报食品药品监督管理局审批。
3.9 报告程序
3.9.1 依照《药品不良反应报告和监测管理办法》的有关规定,实行逐级、定期报告制度,必要时可以越级报告。括药品生产发生、发现的可疑不良反应病例均应填写“药品不良反应/事件报告表”,按《办法》的有关规定及所在行政区域的要求报告省级ADR监测中心;省级ADR监测中心进行核实,作出客观、科学、全面的分析,提出关联性评价后上报国家ADR监测中心;国家ADR监测中心按规定向国家食品药品监督管理局和卫生部报告。个人发现药品引起的新的或严重的ADR,可直接向所在地的省、自治区、直辖市ADR监测中心或(食品)药品监督管理局报告。
3.10 报告时限要求
3.10.1 一般病例逐级、定期报告,应在发现之日起三个月内完成上报工作。
3.10.2 发现新的或严重的药品不良反应/事件,应于发现之日起15日内报告,其中死亡病例须及时向所在地省、自治区、直辖市ADR监测中心报告,必要时可以越级报告。
3.10.3 群体不良反应/事件应立即以有效方式(书面、电子文本、传真等)向所在地省、自治区、直辖市(食品)药品监督管理局、卫生厅(局)以及ADR监测中心报告。省、自治区、直辖市(食品)药品监督管理局应立即会同同级卫生厅(局)组织调查核实,并向国家食品药品监督管理局、卫生部和国家ADR监测中心报告。
3.10.4 对于定期汇总报告,新药和进口药品以注册日期为起点。新药监测期内的药品,每年的1月份提交定期汇总报告;对新药监测期已满的药品,在首次药品批准证明文件有效期届满当年1月份提交定期汇总报告,以后每隔5年汇总报告一次,上报时间是规定年度的1月份。首次获准进口之日起5年内的进口药品,每年的1月份提交定期汇总报告;满5年的,在首次进口药品注册证书有效期届满当年1月份提交定期汇总报告,以后每隔5年汇总报告一次,上报时间是规定年度的1月份。其他药品以国家食品药品监督管理局统一换发药品批准文号当年1月1日为起点,每隔5年汇总报告一次,上报时间是规定年度的1月份。
3.10 药品群体不良反应/事件报告要求
3.10.1 医疗卫生机构报告要求:
3.10.1.1.事件描述
① 发生时间
② 地点
③ 涉及药品名称
④ 药品不良反应/事件主要表现
⑤ 诊治过程
⑥ 转归情况
⑦ 在该地区是否为计划内免疫药品
2.典型病例详细填写《药品不良反应/事件报告表》
3.报告人及联系电话
3.10.1.2 药品生产企业报告要求:
1.事件发生、发展、处理等相关情况
2.药品说明书(进口药品须提供国外说明书)
3.质量检验报告
4.是否在监测期内(进口药是否为首次获准进口五年内)
5.注册、再注册时间
6.药品生产批件
7.执行标准
8.国内外药品安全性研究情况、国内外药品不良反应发生情况包括文献报道
9.典型病例详细填写《药品不良反应/事件报告表》
10.报告人及联系电话
3.3.12.3 省、自治区、直辖市药品不良反应监测中心报告要求
1.组织填写《药品群体不良反应/事件报告表》
2.整理、分析收到材料
3.提出关联性评价意见
4.密切关注事件后续发展
5.事件过程详细调查报告(事件发生、发展、处理、结果等)
3.3.13 全国药品不良反应监测网络
网址:http://www.adr.gov.cn/base/index.asp
单位代码:
登录密码:
附件:1.药品不良反应/事件报告表
2.药品群体不良反应/事件报告表
3.药品不良反应/事件定期汇总表
附表1 制表单位:国家食品药品监督管理局
药品不良反应 / 事件报告表
新的□严重□一般□ 医疗卫生机构□ 生产企业经营企业□ 个人□ 编码□□□□□□□□□□□□□□□□□□□
单位名称: 部门: 电话: 报告日期: 年 月 日

报告人职业(医疗机构):医生□ 药师□ 护士□ 其他□ 报告人职务职称(企业): 报告人签名:
◇不良反应/事件分析

◇严重药品不良反应/事件是指有下列情形之一者:
① 引起死亡 □
② 致畸、致癌或出生缺陷 □
③ 对生命有危险并能够导致人体永久的或显著的伤残 □
④ 对器官功能产生永久损伤 □
⑤ 导致住院或住院时间延长 □
◇编码规则:
省(自治区、直辖市) 市(地区) 县(区) 单位 年代 流水号
□□ □□ □□ □□□□ □□□□ □□□□□
注:省(自治区、直辖市)、市(地区)、县(区)编码按中华人民共和国行政区划代码填写。
单位编码第一位如下填写:医疗机构1、军队医院2、计生机构3、生产企业4、经营企业5。
个人报告单位编码一栏填写6000
◇注:通用名称一栏,首次获准进口5年内的进口品种用*注明
国家药品不良反应监测中心 药品不良反应监测中心
通信地址:北京市崇文区法华南里11号楼二层 通信地址:
邮 编:100061 邮 编:
电 话:(010)67164979 电 话:
传 真:(010)67184951 传 真:
E – mail :report@adr.gov.cn E – mail:
附表2 药品群体不良反应/事件报告表 制表单位:国家食品药品监督管理局
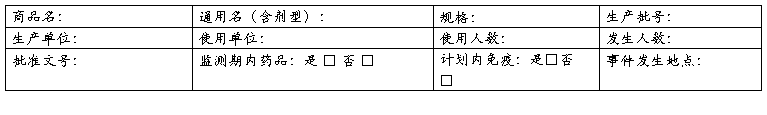
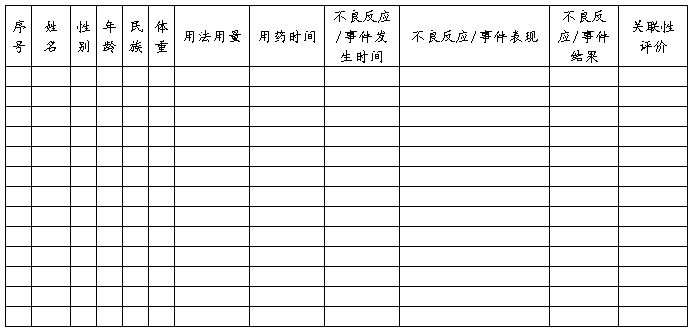
上报单位: 地址: 报告日期:
报告人: 联系电话: 省级ADR中心(签章):
附:1)其它相关资料请按附录C要求另附页报告;
2)典型病例请填写《药品不良反应/事件报告表》;3)不良反应/事件结果指治愈、好转、有后遗症或死亡。
附表3 制表单位:国家食品药品监督管理局
药品不良反应/事件定期汇总表

报告人: 报告日期:
药品生产企业(签章) 省ADR中心(签章)
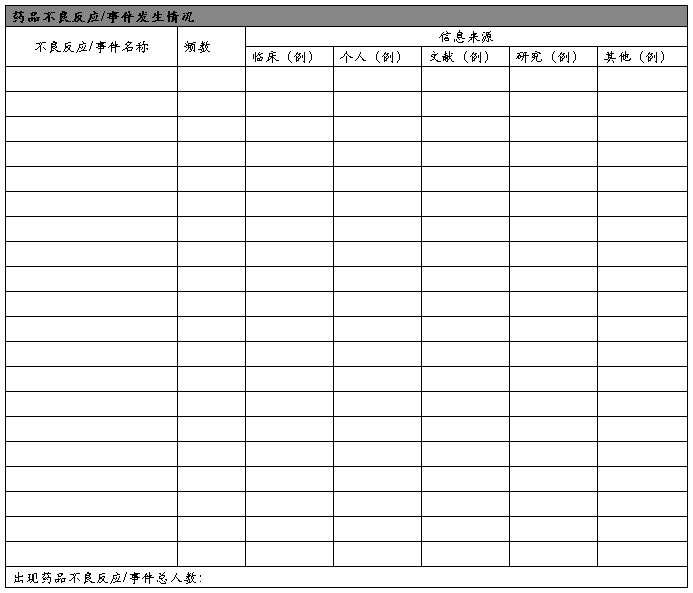
附:1)请附汇总时间内药品说明书一份,质量标准一份;
2)品种有无不良反应/事件发生,企业均应提交汇总报告表;
3)相关研究只需列明题目、发表论文出处、研究内容论点,对应详细资料另附。
4)以上栏目如无情况说明请注明“无”,如表格空间不够可另附页说明。
