蔬菜中维生素C的测定设计实验
设计者: 张茹佳(0113号)
祝 玲(0112号)
邓 楠(0130号)
李 厦(0132号)
组 长: 张茹佳
班 级: 09化学一班
实验日期:20xx年4月20日
蔬菜中维生素C的测定设计实验
一:教学目标
(1):通过测定黄瓜中Vc的含量来了解果蔬中Vc含量情况;
(2):学习和掌握测定Vc的原理和方法,来掌握正确的设计实
验方法和能力。
二:教学重难点
重点:维生素C测定中的滴定方法;
难点:维生素C的含量测定原理及方法;
三:教学用具
药品:醋酸缓冲溶液 、10%KI溶液 、淀粉、碘酸钾、硫酸、 仪器:酸式滴定管 、烧杯 、离心机、榨汁机、胶头滴管 四:实验原理
测量果蔬及其制品中Vc含量的方法有很多种,各有特点,本实验采取间接碘量法来对红尖辣椒中VC的含量进行测定,维生素C的结构中有—C = C—基团,又具有烯醇式结构,还原性强,水溶液中可解离成氧化型抗坏血酸。因此具有还原性,又称为还原性抗坏血酸。
维生素C能还原KIO3中的碘,还原性抗坏血酸还原碘后,本身被氧化成脱氢抗坏血酸,在没有杂质干扰时,一定量的样品提取液还原标准KIO3的量与样品中所含抗坏血酸量成正比(1:3)。
当KIO3刚刚加入时,IO3-离子会与溶液中的I-离子迅速发生氧化还原反应生成I2
IO3-+ 5I-+6H+=3I2+3H2O
然后生成的I2会与VC发生反应氧化还原反应,反应方程式如下: I2 + C6H8O6 = 2HI + C6H6O6
生成的I2被迅速消耗,当溶液中的Vc全部反应完后,会生成多余的I2
所以可以用淀粉作指示剂,通过淀粉作指示剂可迅速判断终点,当有多余碘存在时,淀粉呈蓝色,即可指示终点。
由于维生素C具在较强的还原性,在空气中极易被氧化成而成黄色,尤其在碱性条件下更甚,所以在搅拌和测定时加入HAC缓冲溶液,以减少维生素的副反应。
并且应当注意的是应该在终点附近加入淀粉,因为淀粉是大分子物质,会吸附溶液中的分子和离子,过早加入淀粉生成的物质会吸附在淀粉上,影响反应终点的判断,所以应该在终点附近加入淀粉。
而且在测定时还要在溶液中加入过量的KI溶液。这有两个原因:一是过量的KI会确保KIO3中的I(+5价)会完全参加反应,第二个原因是I2在一般水溶液中溶解度很小,会影响终点的灵敏度,但是在KI溶液中I2中的溶解度较大,这样当反应刚刚过量时,生成的I2会迅速与淀粉发生显色反应,提高终点的灵敏度,使反应的误差相对较小。所以KI溶液只要保证过量就可以,不必要进行精确配制。
记下终点消耗的KIO3体积,通过KIO3的消耗量来计算出红尖辣椒中的VC含量。由以上两步反应方程可知,消耗的VC的量是KIO3量的3倍。所以根据KIO3溶液的用量可以算出溶液中Vc的含量进而求出样品中VC的含量。
测定反应关系式如下:
n(VC)=3 ×V(KIO3) ×C(KIO3)
即:M×参考值(mg/100g)÷M(VC) =3 ×V(KIO3) ×C(KIO3) 其中:M为样品质量M的范围,即样品称量范围,黄瓜的参考值大约是176mg/100g C(KIO3)为大致配制,一般配制0.002mol/L ,0.005mol/L或 0.01mol/L, 本实
验大概配制的浓度为0.005mol/L。
。
五:教学过程
一、溶液的配制与准备
用减量法称取为0.25g≤M≤0.27g,将C(KIO3)配制成约0.005 mol/L的KIO3溶液,记下质量,用容量瓶配制成250毫升溶液。
HAC缓冲溶液和KI溶液可由标淮溶液大概配制。
二、样品准备
取黄瓜用自来水洗净后,再用蒸馏水冲洗2遍,待基本沥去水分,去皮备用。
取上述黄瓜约20g移入搅拌机内,搅拌5分钟,搅拌完后取出溶液,注意要在搅拌时要用专用的容器来承装,并且在取出时要对容器进行多次冲洗,取出后倒入锥形瓶并立即加入10~20ml的HAC缓冲溶液,摇匀。注意溶液最后的体积要尽量小,最好能在30ml左右。
最后用漏斗对溶液进行过滤,在滤纸上过滤得提取液。注意动作要迅速以减少VC被氧化。
三、测定VC的含量
取滤液加10ml-15ml10%KI溶液和8mL 2g/L的硫酸溶液,并加入蒸馏水,使全部溶液达40~60ml,摇匀。
以约0.005mol/L的碘酸钾溶液滴定,用1%淀粉试剂作指示剂,至溶液呈蓝色且不褪色为终点,记下终点时消耗的碘酸钾溶液读数。
【实验装置图】:
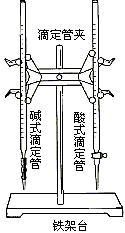
【实验现象】:
滴入淀粉时,溶液变为蓝色。
【实验结论】: 黄瓜中VC含量较平均值较低。
评分标准及作业评价
实验操作占60% ;实验报告占40%
实验操作:60分
1. 清洗仪器 3分
2. 仪器安装顺序3分;
3. 润洗滴定管4分;
4. 检查仪器、药品。3分
5. 液体药品的取用 3分;
6. 滴定时量取液体药品的方法7分;
7. 滴定方法正确7分
8. 实验数据的记录10分;
9. 实验现象和实验结论准确、规范10分;
10. 实验态度和习惯(整理仪器、废品的存放等)10分。 实验报告:40分
1.实验名称 2分
2.实验目的 2分
3.实验仪器 3分
4.实验原理 5分
5.实验报告书写规范 7分
6.实验记录 5分
7.实验数据处理 7分
8.实验结果与分析 9分
总成绩:实验操作+实验报告
作业反馈:
作业等级分为优、良加、良、良减。同学们的实验报告都写的很认真,步骤完整,但在细节方面还存在问题,如有的同学不花实验装置图,有的同学不记录实验现象和数据,或者只有现象没有数据。大多数同学之计算了结果,没有对结果进行分析,即得出实验结论。
第二篇:水果、蔬菜中维生素C含量的测定——紫外分光光度快速测定方法探讨
第23卷,第4期
2oo光谱实验室Ch油eseV01.23,No.46年7月Jo吖nn}ofspectroscop,La6仃r砒or,July,20O6
水果、蔬菜中维生素C含量的测定
——紫外分光光度快速测定方法探讨
郑京平①
(福建省测试技术研究所福州市北环中路61号350003)
摘要本文利用维生素C具有对紫外产生吸收和对碱不稳定的特性。建立了紫外分光光度快速测
定水果、蔬菜维生素c含量的新方法。维生索c浓度在1.oo一12.opg/mL范围内与吸收值呈良好的线性关系;检出限为o.01他g/mL;力口标回收率在97.9%一99.o%之间。该法操作简单,结果准确,应用于维生素C含量的测定.结果令人满意。
关键词维生素C,紫外分光光度法.水果.蔬菜。
中图分类号:0657.32文献标识码:A文章编号:1004—8138(2006)04一0731一05
1前言
维生素c又称抗坏血酸,是所有具有抗坏血酸生物活性的化合物的统称。它在人体内不能合成,必须依靠膳食供给。维生素c不仅具有广泛的生理功能,能防止坏血病,关节肿,促进外伤愈合,使机体增强抵抗能力。而且在食品工业上常用作抗氧化剂、酸味剂及强化剂。因此,测定食品中维生素c的含量以评价食品品质及食品加工过程中维生素c的变化情况具有重要的意义。
维生素c纯品为白色无臭结晶,熔点在190一192rc,易溶于水,微溶于丙酮,在乙醇中溶解度更低,不溶于油剂。结晶抗坏血酸在空气中稳定,但它在水溶液中易被空气和其他氧化剂氧化,生成脱氢抗坏血酸;在碱性条件下易分解,见光加速分解;在弱酸条件中较稳定。
维生素C含量的测定方法很多。一般方法有2.6一二氯靛酚滴定法;2.4一二硝基苯肼比色法;荧光分光光度法;电化学法和高效液相色谱法。
维生素c广泛存在于植物组织中,新鲜的水果、蔬菜中含量较多。水果、蔬菜维生素c含量的测定依国标GB/T6195—1986是采用2.6一二氯靛酚滴定法[1]。根据维生素C的氧化还原性质,从样品溶液由蓝色转变为粉红色来辨别其终点的到达。但是多数水果、蔬菜样品其提取液都具有一定的色泽,有的即使用硅藻土电很难脱色,因此,滴定终点不易辨认。而GB/T6195—1986附录A二甲苯一二氯靛酚比色法虽然适用于测定深色样品还原型抗坏血酸,但由于萃取液二甲苯为有机溶剂,有很强的毒性,既不利于操作人员的健康,也不利于环境保护,故不推荐此测试方法。紫外分光光度快速测定法【21是根据维生素C具有对紫外产生吸收和对碱不稳定的特性,于波长243nm处测定样品溶液与碱处理样品两者吸光度之差,通过查校准曲线,即可计算样品中维生素C的含量。此法操作简单、快速准确、重现性好,结果令人满意。特别适合含深色样品的测定。
①联系人.电话:(0591)87814374(办);(0591)87732389(宅);E—mail:zzn9910513@sina.com
作者简介:郑京平(196l~).女.福州市人.工程师.主要从事化学分析工作。收稿日期:2006一03一07;接受日期:2006一03—29
万方数据
光谱实验室第23卷
2实验部分
DV2.1仪器与试剂650单光束扫描型紫外分光光度计(美国贝克曼公司);A乒一240电子天平(瑞士梅特勒公司);高速组织捣碎机;800型离心沉淀器(上海手术器械厂)。
浸提剂:2.o%(Ⅳ∥)偏磷酸溶液:o.5mol/I。氢氧化钠溶液;100弘g/mL抗坏血酸标准溶液。以上试剂均为分析纯,实验用水为蒸馏水。
2.2实验方法
2.2.1校准曲线的绘制
称取抗坏血酸10mg(准确至o.1mg),用2%偏磷酸溶解,小心转移到100mI。容量瓶中,并加偏磷酸稀释到刻度,混匀,此抗坏血酸溶液的浓度为100弘g/mI。。吸取o.oo、o.10、o.20、o.40、o.60、o.80、1.00、1.20mL抗坏血酸标准使用溶液,置于10mL比色管中;用2%偏磷酸定容,摇匀。此标准系列抗坏血酸的浓度分别为o.00、1.00、2.00、4.00、6.00、8.00、10.o、12.opg/mI。。以蒸馏水为参比,在波长243nm处,用1cm石英皿测定标准系列抗坏血酸溶液的吸光度。抗坏血酸吸光度为A,试剂空白吸光度为Ao,计算吸光度差△A—A一4。的值。以吸光度差值△A对抗坏血酸浓度C绘制校准曲线。
2.2.2样品的测定
样液的制备;将水果、蔬菜样品洗净、擦干,称取具有代表性样品的可食部分1009,放人组织捣碎机中,加入100mL浸提剂,迅速捣成匀浆。称取10一509浆状样品,用浸提剂将样品移入100mL容量瓶中,并稀释至刻度,摇匀。若提取液澄清透明,则可直接取样测定,若有浑浊现象,可通过离心来消除。
样液的测定:准确移取澄清透明的o.1一o.5mL提取液,置于10mL的比色管中,用2%偏磷酸稀释至刻度后摇匀。以蒸馏水为参比,在波长243nm处,用1cm石英皿测定其吸光度。
待测碱处理样液的测定:分别吸取o.1一o.5mI。澄清透明提取液,加入6滴o.5mol/I。氢氧化钠溶液,置于10mI。比色管中混匀,在室温放置40min后'力口入2%偏磷酸稀释至刻度后摇匀。以蒸馏水为参比,在波长243nm处测定其吸光度。
2.2.3结果计算
由待测样品与待测碱处理样品的吸光值之差查校准曲线,即可计算出样品中维生素c的含量,也可直接以待测碱处理液为参比,测得待测液的吸光值,通过查校准曲线,计算出样品的维生素C的含量。
维生素c的含量,mg/1009一篇簧等;
其中:肌——样品重量,g;200——稀释倍数;C——从校准曲线上查得抗坏血酸的含量,pg/mL;
y——测试时吸取提取液体积,mI。。
3结果与讨论
测定波长的选择3.1反应条件选择3.1.1
维生素c是烯醇化合物,具有一C—c一基,在可见区无吸收,在紫外区有吸收,按实验方法,分别对不同浓度的维生素C与试剂空白溶液在200—400nm波长范围内进行扫描,结果见图1。由紫外吸收光谱图表明,最大吸收峰在243nm。因此,选243nm作为测量波长。
万方数据
第4期郑京平:水果、蔬菜中维生素c含量的测定——紫外分光光度快速测定方法探讨7333.1.2溶剂的选择o?8000
由于维生素c极不稳定,在样品前
常重要的。可采用添加偏磷酸、草酸的方蚤o.44005处理过程中,防止抗坏血酸的氧化是非篆
o.0800
吸光度A
3.1.4o.4ld2().3863o.3670Na()H试剂用量选择.
水果、蔬菜加碱量与提取液的取样量有关,当提取液取样量≤o.5mI。时,加入6滴(约o.3mL)o.5mol/I。Na()H溶液,溶液呈碱性(pH值>10),利用维生素在碱性介质中不稳定特性,达到破坏维生素c的目的。若碱液加入量过大,会影响最终测定液的酸碱度,故选加人6滴o.5mol/I。NaOH溶液。若取样体积大于o.5mI。时,应适当多加碱液至溶液pH值>10,此时在室温静置的时间也必须延长。
3.2方法的相关性和检测范围
在优化的实验条件下,校准曲线按本法测定,数据见表2,最大吸光度值最好不要超过o.8A,否则浓度过高容易造成曲线弯曲。以吸光度差值△A对维生素C含量作图,得回归方程△A—o.05496c+o.00651,相关系数7一o.9999,结果表明,维生素C在1.oO一12.o肛g/mI。范围内吸光度△A与浓度c之间呈良好的线性关系,服从比耳定律,结果见图2。
表2校准系列测定结果
3.3方法检出限
连续测定空白吸光值10次,吸光表3空白10次平行测定结果
度值见表3,在置信度约90%时,取置
信系数K一3,按上述线性方程,其校
准曲线斜率5一o.05496,则相对应的万方数据
光谱实验室第23卷
分析物浓度作为方程的检出限D?L—KSD/S—o.014(pg/mI。)。
3.4方法准确度jo.7
为确认分析结果的可靠性,了解试样中有藕“3
无干扰物质存在,应用本法对样品进行加标回
率在97.9%一99.o%之间,平均回收率为‘
98.3%,认为共存物质构成干扰已消除。
表4加标回收率测定结果粢。。26lO14收试验,结果见表4,由表4可知,本方法回收。维生素C浓度/ug?m∥图2维生素C的校准曲线
3.5方法精密度
取2种维生素C表5平行样品测定结果(n=5)
含量不同的样品,每
种样品平行测定5次,
结果见表5,从测定结
果可以看出,平行样测定有较好的重现性。
3.6不同方法对比试验.
紫外分光光度法与2.6一二氯靛酚滴定法采用相同的前处理溶液,只是测试方法不同,从表6可以看出,不同方法测得维生素C的相对平均偏差均<5.o%,表明2种方法结果相吻合,且紫外分光光度法不受颜色干扰和其他还原性物质的影响,更适合于含深色泽样品的测定。
表6不同方法对几种水果、蔬菜的测定结果
3.7干扰物质的消除
由于水果、蔬菜中成分复杂,有些成分在紫外区243nm处也会产生吸收,利用维生素C在碱性溶液中具有不稳定性,可在样品中先加入碱液,调节溶液的pH值至碱性,破坏样品中维生素C,用此液作为空白,来校正干扰物质所产生的吸光值,此法具有较强的专一性。
3.8酸度的影响
在波长为243nm,石英皿为1cm时,10mI,2%的偏磷酸的吸光值与6滴o.5mol/I,NaOH溶液和2%偏磷酸配制成1omI.溶液的吸光值,6次测定,结果吸光度恒定,说明少量的Na0H溶液而引起溶液微弱酸碱度变化,对吸光值不影响。
万方数据
第4期郑京平:水果、蔬菜中维生素c含量的测定——紫外分光光度快速测定方法探讨7354分析过程中的注意点
(1)标准抗坏血酸溶液必须现用现配。
(2)要求每批测定样品都要有校准曲线。
(3)在处理各种样品时,如遇到泡沫产生,可以加入数滴辛醇消除。
(4)若样品浑浊,则可用离一亡I、机分离。用转速3000r/min,时间约为20一30min,至样液澄清、透明,取上清液分析。
(5)一般分析纯抗坏血酸纯度为99.5%以上,可不标定。如试剂发黄,则弃去不用。或按GB/T6195—1986附录B方法标定后再用。
5结论
本文利用维生素C具有对紫外产生吸收和对碱不稳定的特性,建立了紫外分光光度快速测定水果、蔬菜维生素c的新方法。实验结果表明,维生素c浓度在1.oo一12.opg/mI。范围内与紫外吸收值呈良好的线性关系,利用此方法测定样品中维生素c含量最低检出限为o.014弘g/mI。,回收率在97.9%一99.o%之间,相对标准偏差RsD<5%,表明该方法简单易行,结果准确、灵敏度高,检出限低,可快速测定水果、蔬菜中维生素C,值得推广应用。
参考文献
[1]中华人民共和国国家标准汇编.2.6一二氯靛酚滴定法[s].GB/T6195/86.北京:中国标准出版社,1986.ol一18
[2]何照范.张迪清.保健食品化学及其检测技术[M].北京:中国轻工业出版社,1999.10l—102.
DeterminationoftheVitaminCinFruitsandVegetables
DiscussiononUVSpectrophotometry
ZHENGJing—Ping
LThllf、t’Ⅱ(“,¨tyojT{?髓i}lgTt.thnoCfJgytJfFujimt,FMzhon350Q03,P.R.Chin曲
AbstractAccordinglothecharacteristicsthatVitaminCcanabsorbultraVioletradiationandisvolatiletoalkali,thisarticlcestablishesanewandfastmethodtodeterminethecontentofvitaminCinfruitsandVegetablesbyultraVi()letspectrophotonletry.Whentheconcentrationisbetween1.00弘g/mI。and12.0pg/mI.,VitaminChasfavorabklinearrelationshipwiththevalueofabsorption.ThedetectionlimitisO.014『』g/n1I。,andtherecoveryratiosarebetween97.9%and99.0%.Thismethodiseasytooperatewithhigllprccision.TheresultissatisfactorywhenitwasusedtodeterminevitaminC.
KeywordsVitamillC,UV—Spectrophotometry,Fruit,Vegetable.
万 方数据

水果、蔬菜中维生素C含量的测定——紫外分光光度快速测定
方法探讨
作者:
作者单位:
刊名:
英文刊名:
年,卷(期):
被引用次数:郑京平, ZHENG Jing-Ping福建省测试技术研究所,350003光谱实验室CHINESE JOURNAL OF SPECTROSCOPY LABORATORY2006,23(4)22次
参考文献(2条)
1.中华人民共和国国家标准汇 GB/T 6195/1986.2,6-二氯靛酚滴定法 1986
2.何照范;张迪清 保健食品化学及其检测技术 1999
本文读者也读过(4条)
1. 谷雪贤.Gu Xuexian 蔬果中维生素C含量的检测方法[期刊论文]-广东化工2010,37(7)
2. 孙义 水果和蔬菜中维生素C含量的测定方法综述[期刊论文]-天津化工2008,22(3)
3. 吴春艳.WU Chun-yan 水果中维生素C含量的测定及比较[期刊论文]-武汉理工大学学报2007,29(3)
4. 赵连俊.ZHAO Lian-jun 水果中维生素C含量测定的研究[期刊论文]-当代化工2008,37(6)
引证文献(22条)
1.庞燕军.陈靖.曹春英.张悫 高效液相色谱法测定食品和饮料中维生素C含量[期刊论文]-现代中西医结合杂志2009(5)
2.俞洁敏.傅晓航.李成平 库仑滴定法测定Vitamin C片及黄瓜、青椒中抗坏血酸的含量[期刊论文]-广东微量元素科学 2008(4)
3.王建国.王瑞斌 高锰酸钾滴定法快速测定蔬菜中抗坏血酸含量[期刊论文]-食品科学 2008(10)
4.张云楚.张新规 高效液相色谱-示差折光检测法同时测定维生素C葡萄糖注射液中维生素C与葡萄糖的含量[期刊论文]-中国药品标准 2008(6)
5.马赛箭.安超 普鲁兰多糖涂膜对苹果的保鲜研究[期刊论文]-陕西农业科学 2011(4)
6.李志洲.刘军海 野生猕猴桃三种有效成分的光谱测定[期刊论文]-食品研究与开发 2009(2)
7.沈明星.刘凤军.施林林.陆长婴.陈凤生.王海侯.吴彤东 水葫芦沼液肥对菜薹产量和品质的影响[期刊论文]-江苏农业科学 2009(4)
8.王征帆.杨艳丽 恒电流库仑分析法测定蔬菜中抗坏血酸[期刊论文]-食品科学 2008(1)
9.罗桂林.张林.肖尊宏 蓝光转光剂对小白菜产量和营养品质的影响[期刊论文]-湖北农业科学 2011(4)
10.沈明星.刘凤军.吴彤东.王海侯.陆长婴.施林林.沈晓萍 有机无机氮肥比例对小白菜产量和硝酸盐、VC含量的影响[期刊论文]-江苏农业学报 2009(3)
11.王园朝.周冰.成美容 阻抑退色光度法测定维生素C含量[期刊论文]-化学试剂 2009(10)
12.魏强华.张娜萍.陈业.罗妤娴.冼健荣 蜂胶涂膜剂在番茄保鲜中的应用[期刊论文]-食品工业科技 2009(2)
13.王征帆.杨艳丽 恒电流库仑分析法在水果Vc含量测定中的应用[期刊论文]-安徽农业科学 2008(10)
14.张赟彬.龚钢明.戴妙妙 甘薯多酚粗提液的抗氧化活性研究[期刊论文]-中国粮油学报 2007(5)
15.刘二东.张淑芳.张红 铬天青S分光光度法测定药物中的维生素C[期刊论文]-山东化工 2011(1)
16.魏强华.张娜萍.陈业.罗妤娴.冼健荣 蜂胶涂膜剂研制及其在柑橘保鲜中的应用[期刊论文]-食品研究与开发
2009(4)
17.李元玲.贺龙强 紫外分光光度法测定新鲜蔬菜中维生素C的含量[期刊论文]-焦作大学学报 2011(3)
18.张建夫.陈亚红.田丰收.邓聪 酶催化动力学光度法测定抗坏血酸[期刊论文]-光谱实验室 2010(1)
19.张怡.关文强.张娜.刘莉莉.阎瑞香.孙德岭 温度对西兰花抗氧化活性及其品质指标影响[期刊论文]-食品研究与开发 2011(8)
20.付婷婷.秦文.张正周 冷害对采后"大五星"枇杷果实贮藏品质及木质化败坏的影响[期刊论文]-四川农业大学学报 2011(1)
21.李军.刘凤军.徐君 不同发光二极管(LED)光源补光对大棚秋番茄植株生长及果实产量和品质的影响[期刊论文]-江苏农业学报 2011(6)
22.郑羽茜.张钦发 影响包装番茄汁货架寿命因素的研究[期刊论文]-食品研究与开发 2008(9)
本文链接:http://d..cn/Periodical_gpsys200604020.aspx
