齐 齐 哈 尔 大 学
实 验 报 告
题 目:三草酸合铁(III)酸钾的制备和组成测定
学 校:_ ___
专业班级:___ ____
学生姓名:__ __ ____
同组者姓名: _ _____
成 绩:___________
[实验目的]
1 掌握合成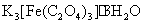 的基本原理和操作技术;
的基本原理和操作技术;
2 加深对铁(III)和铁(II)化合物性质的了解;
3 掌握容量分析等基本操作。
[实验原理]
三草酸合铁(III)酸钾(含三个结晶水)为翠绿色单斜晶体,易溶于水且难溶于乙醇,受光易分解。
本实验以硫酸亚铁铵为原料,与草酸在酸性溶液中先制得草酸亚铁沉淀,然后再用草酸亚铁在草酸钾和草酸的存在下,以过氧化氢为氧化剂,得到铁(III)草酸配合物。主要反应为

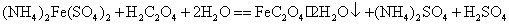
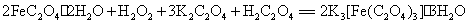
改变溶剂极性并加少量盐析剂,可析出绿色单斜晶体纯的三草酸合铁(III)酸钾,通过化学分析确定配离子的组成。用高锰酸钾标准溶液在酸性介质中滴定测得草酸根的含量。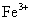 含量可先用过量镁粉将其还原为
含量可先用过量镁粉将其还原为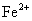 ,然后再用高锰酸钾标准溶液滴定而测得,其反应式为
,然后再用高锰酸钾标准溶液滴定而测得,其反应式为
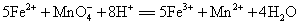
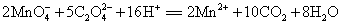
[仪器与实验药品]
托盘天平;分析天平;抽滤装置;烧杯;电炉;移液管;容量瓶;锥形瓶;量筒;试管;表面皿;玻璃棒;滤纸;点滴板;恒温水浴槽;恒温干燥箱。
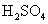 (3mol/L);
(3mol/L);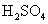 (1mol/L);
(1mol/L);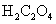 (饱和);
(饱和);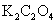 (饱和);
(饱和);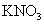 (300g/L);乙醇(95%);
(300g/L);乙醇(95%);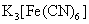 (5%);
(5%);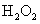 (3%);镁粉;
(3%);镁粉;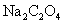 ;高锰酸钾。
;高锰酸钾。
[实验步骤]
1 溶液的配制
按照实验的要求配置各种溶液,检查实验仪器。
2 草酸亚铁的制备
称取5g硫酸亚铁铵固体放在250ml烧杯中,然后加15ml蒸馏水和5~6滴1mol/L的硫酸。
加热溶解后,再加入25ml饱和草酸溶液,加热搅拌至沸,同时不断搅拌,防止飞溅。
维持微沸4min后,停止加热,取少量清液于试管中、煮沸,如还有沉淀还需加热,直到没有沉淀为止,将溶液静置。
带黄色晶体析出后倾析,弃去上层清液,用总量20ml的蒸馏水分三次用倾泻法洗涤晶体,搅拌并温热、静置,弃去上层清液,即得黄色晶体草酸亚铁。
3 三草酸合铁(III)酸钾的制备
往草酸亚铁沉淀中加入饱和草酸钠溶液10毫升,水浴加热40℃,恒温下慢慢滴加3%的过氧化氢溶液20毫升,沉淀转为深棕色。
边加边搅拌,加完后取一滴所得悬浊液于点滴板中,加一滴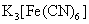 溶液,如有蓝色出现,则还需要加过氧化氢溶液,至检测不到
溶液,如有蓝色出现,则还需要加过氧化氢溶液,至检测不到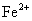 。
。
将溶液加热至沸,然后加入20ml饱和草酸溶液,沉淀立即溶解,溶液转为绿色。
趁热过滤,滤液转入100ml烧杯中,加入95%的乙醇25ml,加入几滴硝酸钾,均匀后冷却,可以看到烧杯底部有晶体析出。
晶体完全析出后,抽滤,将固体至于一表面皿上,放在恒温干燥箱中干燥。
4 高锰酸钾溶液的标定
准确称取0.13~0.17g草酸钠两份,分别置于250ml锥形瓶中。分别加水50ml使其溶解,加入10ml3mol/L硫酸溶液。
在水浴上加热到75~85℃,趁热用待标定的高锰酸钾溶液滴定。滴定至溶液呈现为红色并持续30s内不褪色即为终点。
根据每份滴定中草酸钠的质量和消耗的高锰酸钾的体积,计算出高锰酸钾溶液的浓度。
5 草酸根含量的测定
精确称取制得的样品约0.2~0.3g,放入250ml小烧杯中加水溶解后定量转移至250ml容量瓶中,稀释至刻度,摇匀,待测。
分别取2份25ml试液于锥形瓶中,加入25ml水和5ml 1mol/L硫酸溶液,用已标定的高锰酸钾溶液滴定。滴定前先一滴一滴地加入高锰酸钾溶液,然后加热到75~85℃,再用高锰酸钾滴定热溶液,直至微红色在30s内不消失。
记下消耗的高锰酸钾溶液的总体积,计算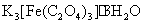 中草酸根的质量分数,并换算成物质的量。
中草酸根的质量分数,并换算成物质的量。
6 铁含量的测定
在上述滴定过草酸根的保留溶液中加镁粉还原,至黄色消失。加热3分钟,使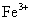 完全转化成
完全转化成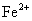 ,过滤,滤液转入250ml容量瓶中,用高锰酸钾滴定至微红色。
,过滤,滤液转入250ml容量瓶中,用高锰酸钾滴定至微红色。
计算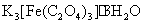 中铁的质量分数,并换成物质的量。
中铁的质量分数,并换成物质的量。
[实验结果与讨论]
三草酸合铁(III)酸钾的产率=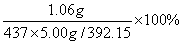 =19.02%
=19.02%
1 高锰酸钾溶液标定的数据处理
根据草酸钠与高锰酸钾的反应计量关系:2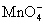
 5
5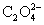 ;
;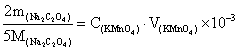
①当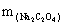 =0.145g,
=0.145g,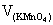 =24.31ml时;
=24.31ml时;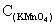 =
=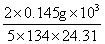 =0.01780mol/L
=0.01780mol/L
②当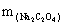 =0.149g,
=0.149g,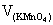 =25.101ml时;
=25.101ml时;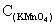 =
=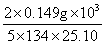 =0.01772mol/L
=0.01772mol/L
表一 高锰酸钾溶液浓度的标定数据处理(M[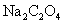 ]=134)
]=134)

2 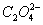 含量测定的数据处理
含量测定的数据处理
根据草酸钠与高锰酸钾的反应计量关系:2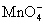
 5
5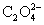 ;所以
;所以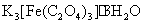
 3
3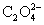


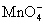 ;所以
;所以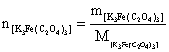 ;
;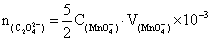
①当m[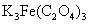 ]=0.0251g;V[
]=0.0251g;V[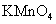 ]=3.81ml时;已知
]=3.81ml时;已知 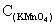 =0.01776mol/L;则n[
=0.01776mol/L;则n[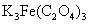 ]=
]=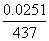 =5.74×
=5.74×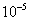 mol; n[
mol; n[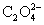 ]=
]=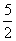 ×0.01776×3.81×
×0.01776×3.81×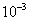 =1.69×
=1.69×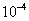 mol
mol
②当m[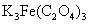 ]=0.0251g;V[
]=0.0251g;V[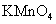 ]=3.77ml时;已知
]=3.77ml时;已知 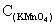 =0.01776mol/L;则n[
=0.01776mol/L;则n[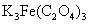 ]=
]=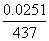 =5.74×
=5.74×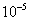 mol; n[
mol; n[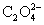 ]=
]=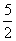 ×0.01776×3.77×
×0.01776×3.77×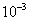 =1.67×
=1.67×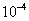 mol
mol
表2 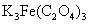 中
中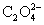 的测定数据处理(M[
的测定数据处理(M[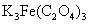 ]=437)
]=437)

3  含量测定的数据处理
含量测定的数据处理
根据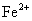 与高锰酸根反应计量关系得出5
与高锰酸根反应计量关系得出5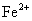

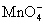 ;
;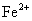

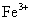 所以n[
所以n[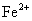 ]=5C[
]=5C[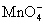 ]
] V[
V[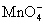 ]×
]×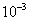
①当V[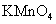 ]=0.25ml时,n[
]=0.25ml时,n[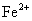 ]=5×0.01776×0.25×
]=5×0.01776×0.25×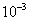 =2.22×
=2.22×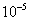 mol
mol
②当V[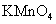 ]=0.22ml时,n[
]=0.22ml时,n[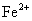 ]=5×0.01776×0.22×
]=5×0.01776×0.22×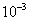 =1.95×
=1.95×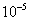 mol
mol
表3 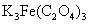 中
中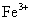 的测定数据处理(M[
的测定数据处理(M[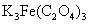 ]=437)
]=437)

在草酸根含量测定中,称取0.3g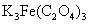 配成250ml溶液,移取25ml滴定。
配成250ml溶液,移取25ml滴定。
在1mol产品中含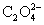 2.93mol,
2.93mol,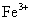 0.98mol,该物质的化学式为
0.98mol,该物质的化学式为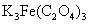 。
。
[误差分析]
根据三草酸合铁(III)酸钾的化学式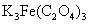 ,理论上1mol产品中含草酸根3mol,三价铁离子1mol,但实验结果其含量都偏低,说明实验存在一定的误差。
,理论上1mol产品中含草酸根3mol,三价铁离子1mol,但实验结果其含量都偏低,说明实验存在一定的误差。
对于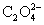 ,在配置饱和草酸溶液时,为了加快其溶解速度,对其进行了加热,草酸发生脱羧反应,造成
,在配置饱和草酸溶液时,为了加快其溶解速度,对其进行了加热,草酸发生脱羧反应,造成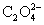 损失。
损失。
对于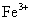 ,本实验实际测得的
,本实验实际测得的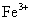 偏低,分析其可能原因有:在溶解硫酸亚铁铵时,硫酸的量不够,造成
偏低,分析其可能原因有:在溶解硫酸亚铁铵时,硫酸的量不够,造成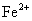 水解;在三草酸合铁(III)酸钾的制备过程中,过氧化氢加入的量不够,
水解;在三草酸合铁(III)酸钾的制备过程中,过氧化氢加入的量不够,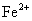 没有完全转化为
没有完全转化为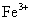 ;在测定铁含量时,加入的镁粉量不够,
;在测定铁含量时,加入的镁粉量不够,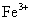 没有完全转化为
没有完全转化为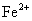 ,导致实验结果偏小。
,导致实验结果偏小。
[注意事项]
1 慢慢滴加过氧化氢,以防止过氧化氢分解。
2 铁(II)为氧化完全,则后一步加入再多的草酸溶液都不能使溶液完全变透明,基本能完全转化为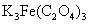 溶液,而仍会产生难容的
溶液,而仍会产生难容的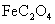 ,此时应采取趁热过滤,或网沉淀上再加过氧化氢等补救措施。
,此时应采取趁热过滤,或网沉淀上再加过氧化氢等补救措施。
3 在抽滤过程中,不要用水洗粘附在烧杯和布氏漏斗上的绿色产品。
4 温度不能高于85摄氏度,否则草酸分解。
5 高锰酸钾滴定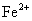 或
或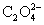 时,滴定速度不能太快,否则部分高锰酸钾会转变成二氧化锰沉淀。
时,滴定速度不能太快,否则部分高锰酸钾会转变成二氧化锰沉淀。
[思考题]
1 能否用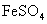 代替硫酸亚铁铵来合成
代替硫酸亚铁铵来合成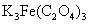 ?这时可用硝酸代替过氧化氢做氧化剂,写出用硝酸做氧化剂的主要反应式。你认为哪个做氧化剂较好?为什么?
?这时可用硝酸代替过氧化氢做氧化剂,写出用硝酸做氧化剂的主要反应式。你认为哪个做氧化剂较好?为什么?
答:能;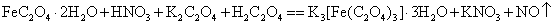
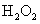 做氧化剂好,没有引入其它杂质,不污染环境。
做氧化剂好,没有引入其它杂质,不污染环境。
2 根据三草酸合铁(III)酸钾的合成过程及它的TG曲线,你认为该化合物该如何保存?
答:三草酸合铁(III)酸钾受光易分解,易溶于水,应保存在棕色试剂瓶中且置于阴凉干 燥处。
3 在三草酸合铁(III)酸钾制备过程中,加入15ml饱和草酸溶液后,沉淀溶解,溶液转为绿色。若此溶液中加入25ml95%乙醇或将此溶液过滤后往滤液中加入25ml95%乙醇,现象有何不同?为什么?并说明对产品质量有何影响。
答:若不过滤就加入乙醇,则会有杂质参加晶体的形成,使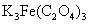
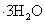 不纯净,而且会有部分铁(II)参与晶体形成,使产品质量增加。
不纯净,而且会有部分铁(II)参与晶体形成,使产品质量增加。
第二篇:实验三草酸合铁(III)酸钾的制备和组成测定2齐齐哈尔大学化学专业 实验报告无机部分
齐 齐 哈 尔 大 学
实 验 报 告
题 目:三草酸合铁(III)酸钾的制备和组成测定
学 校:_齐齐哈尔大学__
专业班级:_化学101__ _
学生姓名: ____叶梦_____
同组者姓名:___苟登红____
成 绩:___________
2013 年 10 月 9 日
实验5 三草酸合铁(III)酸钾的制备和组成测定
实验目的
1 掌握合成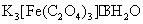 的基本原理和操作技术;
的基本原理和操作技术;
2 加深对铁(III)和铁(II)化合物性质的了解;
3 掌握容量分析等基本操作。
实验原理
三草酸合铁(III)酸钾(含三个结晶水)为翠绿色单斜晶体,易溶于水且难溶于乙醇,受光易分解。
本实验以硫酸亚铁铵为原料,与草酸在酸性溶液中先制得草酸亚铁沉淀,然后再用草酸亚铁在草酸钾和草酸的存在下,以过氧化氢为氧化剂,得到铁(III)草酸配合物。主要反应为

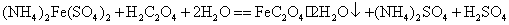
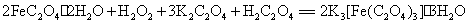
改变溶剂极性并加少量盐析剂,可析出绿色单斜晶体纯的三草酸合铁(III)酸钾,通过化学分析确定配离子的组成。用高锰酸钾标准溶液在酸性介质中滴定测得草酸根的含量。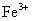 含量可先用过量镁粉将其还原为
含量可先用过量镁粉将其还原为 ,然后再用高锰酸钾标准溶液滴定而测得,其反应式为
,然后再用高锰酸钾标准溶液滴定而测得,其反应式为

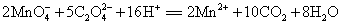
仪器与实验药品
托盘天平;分析天平;抽滤装置;烧杯;电炉;移液管;容量瓶;锥形瓶;量筒;试管;表面皿;玻璃棒;滤纸;点滴板;恒温水浴槽;恒温干燥箱。
铁屑;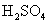 (3mol/L);Na2CO3 (0.1mol/L);硫酸铵;
(3mol/L);Na2CO3 (0.1mol/L);硫酸铵; 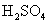 (1mol/L);
(1mol/L);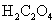 (饱和);
(饱和);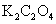 (饱和);KCl;
(饱和);KCl;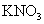 (300g/L);乙醇(95%);
(300g/L);乙醇(95%);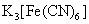 (5%);
(5%);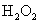 (3%);镁粉;
(3%);镁粉; ;高锰酸钾。
;高锰酸钾。
实验步骤
1. 草酸亚铁的制备
称取5g硫酸亚铁铵固体放在250ml烧杯中,然后加15ml蒸馏水和5~6滴1mol/L的硫酸。
加热溶解后,再加入25ml饱和草酸溶液,加热搅拌至沸,同时不断搅拌,防止飞溅。
维持微沸4min后,停止加热,取少量清液于试管中、煮沸,如还有沉淀还需加热,直到没有沉淀为止,将溶液静置。
带黄色晶体析出后倾析,弃去上层清液,用总量20ml的蒸馏水分三次用倾泻法洗涤晶体,搅拌并温热、静置,弃去上层清液,即得黄色晶体草酸亚铁。
2 三草酸合铁(III)酸钾的制备
往草酸亚铁沉淀中加入饱和草酸钠溶液10毫升,水浴加热40℃,恒温下慢慢滴加3%的过氧化氢溶液20毫升,沉淀转为深棕色。
边加边搅拌,加完后取一滴所得悬浊液于点滴板中,加一滴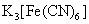 溶液,如有蓝色出现,则还需要加过氧化氢溶液,至检测不到
溶液,如有蓝色出现,则还需要加过氧化氢溶液,至检测不到 。
。
将溶液加热至沸,然后加入20ml饱和草酸溶液,沉淀立即溶解,溶液转为绿色。
趁热过滤,滤液转入100ml烧杯中,加入95%的乙醇25ml,加入几滴硝酸钾,均匀后冷却,可以看到烧杯底部有晶体析出。
晶体完全析出后,抽滤,将固体至于一表面皿上,放在恒温干燥箱中干燥。
得透明的绿色晶体,称重,计算产率。
3 高锰酸钾溶液的标定
准确称取0.13~0.17g草酸钠两份,分别置于250ml锥形瓶中。分别加水50ml使其溶解,加入10ml3mol/L硫酸溶液。
在水浴上加热到75~85℃,趁热用待标定的高锰酸钾溶液滴定。滴定至溶液呈现为红色并持续30s内不褪色即为终点。
根据每份滴定中草酸钠的质量和消耗的高锰酸钾的体积,计算出高锰酸钾溶液的浓度。
4 草酸根含量的测定
精确称取制得的样品约0.2~0.3g,放入250ml小烧杯中加水溶解后定量转移至250ml容量瓶中,稀释至刻度,摇匀,待测。
分别取2份25ml试液于锥形瓶中,加入25ml水和5ml 1mol/L硫酸溶液,用已标定的高锰酸钾溶液滴定。滴定前先一滴一滴地加入高锰酸钾溶液,然后加热到75~85℃,再用高锰酸钾滴定热溶液,直至微红色在30s内不消失。
记下消耗的高锰酸钾溶液的总体积,计算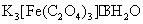 中草酸根的质量分数,并换算成物质的量。
中草酸根的质量分数,并换算成物质的量。
5 铁含量的测定
在上述滴定过草酸根的保留溶液中加镁粉还原,至黄色消失。加热3分钟,使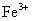 完全转化成
完全转化成 ,过滤,滤液转入250ml容量瓶中,用高锰酸钾滴定至微红色。
,过滤,滤液转入250ml容量瓶中,用高锰酸钾滴定至微红色。
计算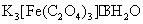 中铁的质量分数,并换成物质的量。
中铁的质量分数,并换成物质的量。
实验结果与讨论
三草酸合铁(III)酸钾的产率=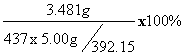 =62.5%
=62.5%
1 高锰酸钾溶液标定的数据处理
根据草酸钠与高锰酸钾的反应计量关系:
2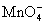 ~5
~5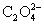 ;
;
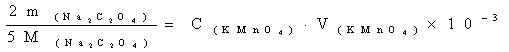
①当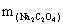 =0.151g,
=0.151g,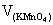 =22.75ml时;
=22.75ml时;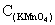 =
=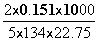 =0.01981mol/L
=0.01981mol/L
②当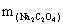 =0.150g,
=0.150g,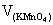 =22.45ml时;
=22.45ml时;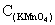 =
=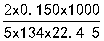 =0.01994mol/L
=0.01994mol/L
③当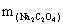 =0.149g,
=0.149g,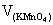 =21.85ml时;
=21.85ml时;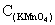 =
=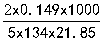 =0.02036mol/L
=0.02036mol/L

表一 高锰酸钾溶液浓度的标定数据处理(M[NaC2O4]=134)
2 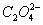 含量测定的数据处理
含量测定的数据处理
根据草酸钠与高锰酸钾的反应计量关系:2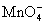 ~5
~5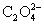 ;所以
;所以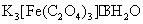 ~3
~3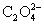 ~
~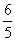
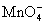 ;所以
;所以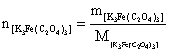
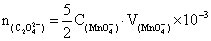
①当m[ ]=0.0300g;V[
]=0.0300g;V[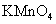 ]=3.40ml时;已知
]=3.40ml时;已知 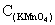 =0.02003mol/L;则n[
=0.02003mol/L;则n[ ]=
]=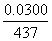 =6.86×
=6.86×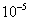 mol; n[
mol; n[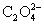 ]=
]=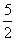 ×0.02003×3.40×
×0.02003×3.40× =1.70×
=1.70×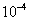 mol
mol
②当m[ ]=0.0300g;V[
]=0.0300g;V[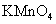 ]=3.45ml时;已知
]=3.45ml时;已知 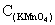 =0.02003mol/L;则n[
=0.02003mol/L;则n[ ]=
]=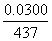 =6.86×
=6.86×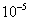 mol; n[
mol; n[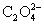 ]=
]=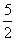 ×0.02003×3.45×
×0.02003×3.45× =1.73×
=1.73×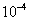 mol
mol
表2  中
中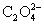 的测定数据处理(M[
的测定数据处理(M[ ]=437)
]=437)

③当m[ ]=0.0300g;V[
]=0.0300g;V[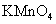 ]=3.35ml时;已知
]=3.35ml时;已知 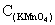 =0.02003mol/L;则n[
=0.02003mol/L;则n[ ]=
]=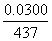 =6.86×
=6.86×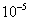 mol; n[
mol; n[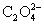 ]=
]=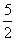 ×0.02003×3.35×
×0.02003×3.35× =1.68×
=1.68×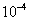 mol
mol
3  含量测定的数据处理
含量测定的数据处理
根据 与高锰酸根反应计量关系得出5
与高锰酸根反应计量关系得出5 ~
~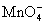 ;
; ~
~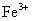 所以n[
所以n[ ]=5C[
]=5C[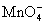 ]
] V[
V[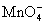 ]×
]×
①当V[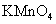 ]=0.26ml时,n[
]=0.26ml时,n[ ]=5×0.02003×0.26×
]=5×0.02003×0.26× =2.60×
=2.60×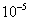 mol
mol
②当V[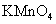 ]=0.25ml时,n[
]=0.25ml时,n[ ]=5×0.02003×0.25×
]=5×0.02003×0.25× =2.50×
=2.50×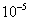 mol
mol
③当V[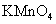 ]=0.27ml时,n[
]=0.27ml时,n[ ]=5×0.02003×0.27×
]=5×0.02003×0.27× =2.70×
=2.70×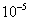 mol
mol
表3  中
中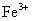 的测定数据处理(M[
的测定数据处理(M[ ]=437)
]=437)

在草酸根含量测定中,称取0.300g 配成250ml溶液,移取25ml滴定。
配成250ml溶液,移取25ml滴定。
在1mol产品中含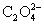 2.48mol,
2.48mol,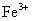 0.38mol,该物质的化学式为
0.38mol,该物质的化学式为 。
。
思考题
1 能否用 代替硫酸亚铁铵来合成
代替硫酸亚铁铵来合成 ?这时可用硝酸代替过氧化氢做氧化剂,写出用硝酸做氧化剂的主要反应式。你认为哪个做氧化剂较好?为什么?
?这时可用硝酸代替过氧化氢做氧化剂,写出用硝酸做氧化剂的主要反应式。你认为哪个做氧化剂较好?为什么?
答:能;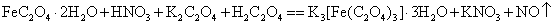
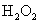 做氧化剂好,没有引入其它杂质,不污染环境。
做氧化剂好,没有引入其它杂质,不污染环境。
2 根据三草酸合铁(III)酸钾的合成过程及它的TG曲线,你认为该化合物该如何保存?
答:三草酸合铁(III)酸钾受光易分解,易溶于水,应保存在棕色试剂瓶中且置于阴凉干 燥处。
3 在三草酸合铁(III)酸钾制备过程中,加入15ml饱和草酸溶液后,沉淀溶解,溶液转为绿色。若此溶液中加入25ml95%乙醇或将此溶液过滤后往滤液中加入25ml95%乙醇,现象有何不同?为什么?并说明对产品质量有何影响。
答:若不过滤就加入乙醇,则会有杂质参加晶体的形成,使
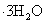 不纯净,而且会有部分铁(II)参与晶体形成,使产品质量增加。
不纯净,而且会有部分铁(II)参与晶体形成,使产品质量增加。
