醋酸纤维薄膜电泳法分离牛血清蛋白
一、目的
掌握醋酸纤维薄膜电泳法分离蛋白质的原理和方法。
二、原理
蛋白质是两性电解质。当PH>PI时,蛋白质为负离子,在电场中向阳极移动;当PH<PI时,蛋白质为正离子,在电场中向阴极移动。血清中含有数种蛋白质,在同一PH值时,因所带电荷不同,而在电场中的移动速度也不相同,故可用电泳法将其分离。
本试验以牛血清为材料,醋酸纤维薄膜为支持物,通过点样、电泳、染色、脱色从而得到血清中蛋白质的分离图谱,再进行观察和定量分析。
血清中含白蛋白、α-球蛋白、β-球蛋白、γ-球蛋白等。其等电点低于pH7.0,在缓冲液中(pH8.6)中,电离成负离子,在电场中向阳极移动。
用醋酸纤维薄膜作蛋白电泳有简便,快速,分离清晰,容易定量等优点。
三、实验仪器
1、牛血清
2、醋酸纤维薄膜
3、镊子
4、电泳仪
5、电泳槽
6、盖玻片
四、实验试剂
1、巴比妥—巴比妥钠缓冲液(离子强度,PH8.6):称取巴比妥1.66g和巴比妥钠12.76g,溶于蒸馏水并稀释至1000ml。用pH计较正后使用。
2、染色液:氨基黑10B0.5g,甲醇50ml,冰乙酸10ml,蒸馏水40ml混匀即可。
3、漂洗液:95%乙醇45ml,冰乙酸5ml和蒸馏水50ml混匀即可。
五、试验步骤
1、准备:用镊子取薄膜一条,浸入缓冲液中,完全浸透后(大约3-5分钟),用镊子取出,将无光泽的一面向上,平放在干净滤纸上,将滤纸对折,吸取多余的缓冲液(注意不要吸的太干)。
2、点样:取盖玻片一块,用玻璃棒将血清均匀的涂在盖玻片的一端面上,垂直地在薄膜一端1/3处点样(无光泽面)。
3、电泳:将薄膜平贴于放在电泳槽上并已浸透缓冲液的滤纸上,无光泽面要向下放置,点样端放在阴极,进行电泳。电泳条件:电压90-110V,电流0.4-0.6mA,通电60分钟。
4、染色:电泳完毕,将薄膜浸入染色液(回收)中10分钟,进行染色。
5、漂洗:染色完毕,将薄膜取出,放入漂洗液中漂洗至背景无色,再浸入蒸馏水中。 (少量多漂)
6、图谱观察:观察图谱,将各种血清蛋白质按实际比例大小绘于实验报告纸上。
六、实验结果
由下图可以得出结论:至少含有三种血清蛋白质。

七、实验分析
1、镊子要回收。
2、醋酸纤维薄膜在光下面能明显区分有光泽面和无光泽面。
3、电泳槽中间为正极,两端为负极。
4、染色液请用完后回收到原来的试剂瓶中。
5、漂洗薄膜时,请做到“少量多漂”,即用少量的漂洗液去漂洗薄膜,多漂几次,这样既不浪费漂洗液,还达到了漂洗的效果。
6、点样时动作要轻并且稳。
第二篇:血清蛋白电泳(醋酸纤维薄膜法)
实验一 血清蛋白电泳(醋酸纤维薄膜法)
[目的]
了解电泳法分离蛋白质的原理、操作方法及临床意义。
[原理]
带电荷的蛋白质,在电场中向着与其所带电荷电性相反的电极泳动称为电泳。血清中各种蛋白质的等电点不同,但大都在pH7以下,若将血清置于pH8.6的缓冲液中,则这些蛋白质均带负电,在电场中都向阳极移动。由于各种蛋白质在同一pH环境中所带负电荷多少及分子大小不同,所以在电场中向阳极泳动速度也不同。蛋白质分子小而带电荷多者,泳动速度快;反之,则泳动速度慢。因此可将血清蛋白质依次分为清蛋白、a1-球蛋白、a2-球蛋白、b-球蛋白和g球蛋白五条区带,经染色可计算出各血清蛋白质含量的百分数。
醋酸纤维薄膜电泳具有微量、快速、简便及分辨率较高等优点,广泛应用于血清蛋白、血红蛋白、脂蛋白、同工酶的分离和测定。
[仪器与材料]
1.仪器:电泳仪、电泳槽、分光光度计或光密度仪。
2.材料:醋酸纤维薄膜、培养皿、滤纸、镊子、点样器、直尺、铅笔、剪刀等。
[试剂]
1.巴比妥—巴比妥钠缓冲液(pH8.6,m=0.06)。称取巴比妥2.21克和巴比妥钠12.36克,溶于500毫升蒸馏水中,加热溶解。待冷至室温后,再加蒸馏水稀释至1000毫升。
2.染色液。称取丽春红S0.4克及三氯醋酸6克;用蒸馏水溶解,并稀释至100毫升。
3.漂洗液。3%(V/V)醋酸溶液。
4.透明液。取无水乙醇75毫升和冰醋酸25毫升混匀备用。
5.0.4mol/L氢氧化钠溶液。
6.40%(V/V)醋酸溶液。
[操作]
1.薄膜的准备:取醋纤薄膜(2厘米*8厘米)在毛面的一端约1.5厘米处,用铅笔轻划一直线,表露点样位置并编号。然后将此薄膜置于巴比妥缓冲液中浸泡,待充分浸透(即膜条无白斑时)后取出,用洁净滤纸轻轻吸去表面的多余缓冲液。
2.点样。取少量血清置于普通玻璃板上,用点样器的钢口蘸取血清(约3~5ml),随后将钢口垂直“印”在点样线上,待血清渗入膜后移开点样器。点样应注意,要适量、均匀和垂直,并避免弄破薄膜。
3.平衡与电泳。将已点样的薄膜加样面朝下,加样端置于阴极端,平整地贴于电泳槽的支架上拉直。支架上事先放置好两端浸入缓冲液的用四层滤纸条作的“滤纸桥”(如图2)。平衡数分钟至薄膜重又湿润时方可通电进行电泳。一般电压为120~160伏,电流约0.4~0.6毫安/厘米,通电时间40~50分钟,待电泳区带展开约3.5厘米时断电。
4.染色。小心取出薄膜,直接浸于丽春红S染色剂中5~10分钟(以清蛋白区带染透为止)。然后在漂洗液中连续浸洗数次,使薄膜底色漂净,即得五条蛋白色带。从阳极端起依次为清蛋白、a1、a2、b和g-球蛋白。
5.透明。若要保存薄膜,待薄膜完全干燥后,置透明液中10~20分钟,取出贴于玻璃板上,干后则透明,可长期保存。
6.定量及计算。将漂洗净的薄膜吸干,剪下各蛋白色带,另于空白部位剪一相当于清蛋白宽度的膜条做空白,分别置于0.4mol/L NaOH溶液的试管中,清蛋白管加4毫升,其余各管加2毫升,振摇,使溶液浸没膜条后,置37℃水浴10分钟,使其色泽浸出。再向各管加40%(V/V)醋酸0.4毫升,清蛋白管则加0.4毫升,以中和部分NaOH,使色泽变红色。取各管上清液用分光光度计,在520nm处,以空白管调工作零点后。分别测得清蛋白管、a1、a2、b和g-球蛋白各管的吸光度值。
定量计算时,先计算各光密度值的总和:
A T = 2×A清+ A a1 + A a2 + A b + A g
再计算血清各部分蛋白质所占的百分率:
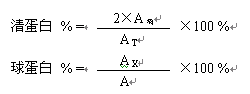
Ax表示各球蛋白组分 (a1、a2、b 和 g ) 的吸光度。
若条件许可,也可将已透明的薄膜放入全自动光密度计或其他光密度计暗箱内,进行扫描分析与计算。
血清蛋白醋纤薄膜电泳的参考正常值为:
白蛋白 62~71 %
a1球蛋白 3~4 %
a2-球蛋白 6~10 %
b-球蛋白 7~11 %
g-球蛋白 9~18 %
