醋酸纤维薄膜电泳法分离血清蛋白
【目的】
1 .掌握醋酸纤维薄膜电泳法分离血清蛋白的操作技术与原理。
2 . 熟悉醋酸纤维薄膜电泳法分离血清蛋白的临床意义。
【原理】
带电粒子在电场中向着与其电荷相反的电极方向移动的现象称为电泳 (Electrophoresis) 。蛋白质为两性电解质。在不同 PH 下,其带电情况不同。在等电点时,蛋白质为兼性离子,其实效电荷为零,不发生泳动。蛋白分子在 pH 小于其等电点的溶液中,呈碱式解离带正电向负极泳动。在 pH 大于其等电点溶液中, 呈酸式解离带负电,泳向正极。带电粒子在电场中的泳动速度常用迁移率 (Mobility) 来表示。它除与电场强度、溶液的性质等有关外,主要决定于分子颗粒的电荷量以及其分子的大小与形状等。电荷较多,分子较小的球状蛋白质泳动较快。
血清中的各种蛋白质的等电点均低于 7 ,故在 PH8.6 缓冲液中,均带负电荷。由于各种蛋白质的等电点不同,带电荷量不等,加之分子量不同,导致在电场中泳动速度不同,从而加以分离。清蛋白泳动最快,其次为 α 1 、α 2 、β及γ 球蛋白。将蛋白质固定染色后,洗去多余染料,可看到清晰的色带(图 3-3 )。将各色带剪开,分别溶于碱性液中,可进行比色分析,计算出各种蛋白质的百分含量,或用吸光度计进行扫描定量。

图 3-3 正常人血清蛋白醋酸纤维薄膜电泳示意图谱
【器材】
1 .电泳仪 ( 稳压器、电泳槽 )
2 .分光光度计
3 .点样器 (1.4× 1.8cm 的 X 光片 )
4 .血清 ( 放置于载玻片上 )
5 .醋酸纤维薄膜 (2× 8cm )
【试剂】
1 . pH8.6 0.06M 巴比妥缓冲液
取巴比妥 1.62g ,巴比妥钠 12.38g ,用蒸馏水加热溶解冷却后加至 1000ml 。测试 pH 值,若 pH 偏离 8.6 ,可用 1mol/LHCl 或 NaOH 校正。
2 .染色液 ( 任选其一 )
( 1 )氨基黑 10 B 1g ,三氯醋酸 13.4g ,磺柳酸 13.4g ,蒸馏水加至 1000ml 。
( 2 )丽春红 2 R 0.8g ,溶于 6% 三氯醋酸 100ml 中。
3 .漂洗液
( 1 ) 3% 冰醋酸溶液 ( 用于氨基黑染色 )
( 2 ) 2.5% 醋酸溶液 ( 用于丽春红染色 ) ;
4 .洗脱液
0.4mol/LNaOH 溶液。
5 .透明液
冰醋酸 30ml ,无水乙醇 70ml ,醋酸乙酯 1ml 混匀。
【操作】
? 准备
电泳槽内放适量的缓冲液于两侧。液槽间放一充满缓冲液的连通管,经过一定时间使两侧液面达到平衡后,取下连通管。
在电泳槽的两侧液槽内侧的支持板上分别用四层滤纸 ( 或纱布 ) 搭桥。即使其一端达到支持板上,另一端浸入缓冲液中。
在醋酸纤维薄膜 ( 2cm × 8cm ) 的无光泽面距一端 1.5cm 处,用铅笔画一线 ( 与此端平行 ) 。作为点样线。把膜放进缓冲液中浸泡数 h ,使膜完全浸透。
? 点样
用点样器均匀蘸取血清后,垂直将血清点在薄膜的点样线上,使血清全部渗入膜内。
? 电泳
将点样后的膜条置于电泳槽架上。放置时点样面向下,点样端置于阴极侧。槽架上四层滤纸作桥垫,膜条与滤纸需贴紧,膜条要拉展。约平衡 5min 后通电。电压为 6V/cm 长 ( 长指膜条与缓种液面上的滤纸桥总长度 ) ,电流为 0.4~0.8mA/cm 宽,夏季通电约 45min ,冬季通电约 1h 。关闭电源。
? 染色与漂洗
通电毕,用无齿小镊子将膜取出并水平移于染色液中固定染色, 2~5min 后取出立即浸入盛有漂洗液的培养皿中,反复漂洗数次,直至背景无色为止。用滤纸吸干多余的漂洗液。此时可见界限清晰的五条区带 ( 氨基黑染色为蓝黑色区带,丽春红染色为红色区带 ) 。最前面的一条为清蛋白带。如右图:
? 定量分析
取试管 6 支,编号,分别用吸量管吸取 0.4mol/L NaOHml 。剪开薄膜上各条蛋白色带,另于空白部位剪一平均大小的薄膜条,将各条分别浸于上述试管内,不时摇动,使颜色洗出。约半小时后用分光光度计进行比色。氨基黑 10B 染色者,选用 620nm 波长,丽春红染色者选 580nm 波长。用空白管调 “0” ,分别读取各管吸光度值之和作为 100% ,求出每管吸光度值占总吸光度值的百分数,即该种蛋白质占血清蛋白的百分比含量。
另外,如用吸光度计扫描,需要先使膜透明化。可把染色后干燥的薄膜放透明液中 10~20min ,取出贴到玻璃板上放干。得到透明薄膜,可用吸光度扫描计描记出电泳曲线。亦可据此算出各蛋白百分数。正常血清血清蛋白的等电点、分子量及含量见表 3-1 。
表 3-1 正常血清蛋白的等电点、分子量及含量
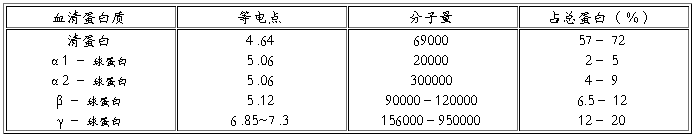
血清蛋白电泳结果有一定临床意义。肝硬化清蛋白明显降低。而 γ – 球蛋白可增高 2~3 倍。肾病综合症和慢性肾小球肾炎时可见到清蛋白降低, α 2 和 β 球蛋白增高。从电泳谱上亦可查出某些异常,例如多发性骨髓瘤病人血清,有时在 β 和 γ 球蛋白之间出现巨球蛋白。原发性肝癌病人血清在清蛋白与 α 1 球蛋白之间可见到甲胎蛋白。
【注意事项】
? 点样线要细窄、均匀、集中,量不宜过多,保持薄膜清洁。
? 盐桥及醋纤膜要放置平整,保证电场均匀。
? 严格控制好电流,电压与电泳时间。电压高,电流强度大,则电泳快,电泳时间虽可缩短,但其产热多,薄膜上水分蒸发也多,严重时会使图谱短而不清晰;相反,电流、电压过低,电泳所需时间延长,由于样品的扩散,也不能获得良好的图谱。一般气温低时,可用较大的电流、电压;气温高时,则宜用较低的电流、电压。
【思考题】
1 .为什么薄膜的点样面朝下,点样端置于阴极?
2 .用醋酸纤维薄膜作为电泳的支持物有何优点?
第二篇:16 生物化学实验--醋酸纤维薄膜电泳法分离血清乳酸脱氢酶同工酶
醋酸纤维薄膜电泳法分离血清乳酸脱氢酶同工酶
【目的】
1 . 掌握电泳法分离血清乳酸脱氢酶同工酶的原理与技术。
2 . 熟悉测定血清乳酸脱氢酶同工酶的临床意义。
【原理】
体内 LDH 同工酶均由四个亚基组成。亚基分二种,即 “ H ” 亚基(多分布于心肌)与 “ M ” 亚基(多分布于肌肉)。根据亚基不同, LDH 同工酶分为以下五种(表 3-8 )。
表 3-8 LDH 同工酶的分类与组成
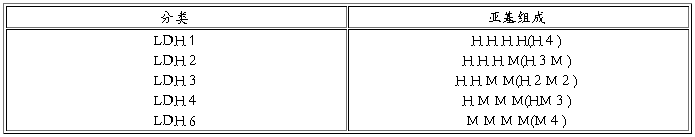
由于 LDH 同工酶的亚基组成不同,在 pH8.6 巴比妥缓冲液中所带电荷不同,通过醋酸纤维薄膜电泳可以将血清样品中的各种 LDH 同工酶彼此分开。
以乳酸钠(钾)为基质,在有氧化型辅酶 Ⅰ 存在时, LDH 可是乳酸脱氢生成丙酮酸、使 NAD + 还原为 NADH+H + , NADH+H + 又将氢传递给吩嗪二甲酯硫酸盐( PMS ), PMS 再将氢传递给氯化硝基四氮唑蓝( NBT) ,使其还原为紫蓝色化合物,因此有 LDH 活性的区带即着紫色,生成颜色深浅与 LDH 活性成正比。其反应如下:

将电泳后的 醋酸纤维薄膜与含有底物乳酸和显色剂的染色液一起保温,便可显示出血清 LDH 同工酶的谱带(图 3-8 )。将各谱带洗脱进行比色分析,即可求得各同功酶的相对百分比。
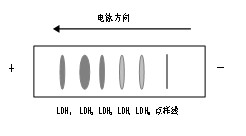
图 3-8 LDH 同工酶电泳图谱
【器材】
1 . 电泳仪
2 . 电泳槽(用二层滤纸或纱布搭桥)
3 . 恒温水浴
4 . 分光光度计
5 . 点样器
6 . 白瓷盘
7 .玻璃板
8 .镊子
【试剂】
1 . pH8.6 巴比妥电泳缓冲液(离子强度 0.05 )
巴比妥钠 20.6g , 巴比妥 3.68g , 蒸馏水加至 2 000ml 。
2 . pH7.5 磷酸盐缓冲液( 0.1M )
磷酸二氢钾 2.16g , 磷酸二氢钠 30.13g , 蒸馏水加至 1 000ml 。 4 ℃ 冰箱保存。
3 . 吩嗪二甲酯硫酸盐液
吩嗪二甲酯硫酸盐 0.5g , 蒸馏水加至 500ml 。
4 . 氯化硝基四氮唑蓝液
氯化硝四氮唑蓝 1.25g , 加入 pH7.5 的磷酸盐缓冲液至 300ml( 温水助溶过滤 ) 。
5 . 1M 乳酸钠液(或 0.5M 乳酸钠液)
取 70% ~ 80% 液体乳酸钠 8ml ,加水至 200ml 为 0.5M 乳酸钠液。取 70% ~ 80% 液体乳酸钠 16ml ,加水到 200ml 为 1M 乳酸钠液。
6 . 染色应用液
NAD + 40mg , 0.1M 磷酸盐缓冲液 4ml , 氯化硝基四氮唑蓝 12ml , 1M 乳酸钠 4ml , 吩嗪二甲酯硫酸盐 1.2ml , 混合即可。临用前配制,避光保存。
7 . 洗脱剂
氯仿 9 份,无水乙醇 1 份,混匀。
8 .固定液
10% 冰醋酸。
【操作】
1 . 准备
将醋纤膜浸入 pH8.6 巴比妥缓冲液中浸泡 15 ~ 20min (注意:先让膜漂浮在液面,待膜全部湿润后在将膜浸入液内)。取出后用干滤纸吸去多余的水分。
2 . 点样
将血清样本用小吸管吸出置于载玻片上,用点样器充分蘸满血清,然后将点样器垂直接触到膜一端 1.5cm 处,待血清全部渗入膜内,静置 2 ~ 5min (点样线应细窄均匀集中)。
3 .电泳
点好血清的薄膜条放置于电泳槽滤纸桥上,糙面(点样面)朝下,点样端在阴极端,膜条与滤纸紧贴、拉直,然后盖上槽盖,平衡 5min 后即可通电。电压为 25V/cm ,通电 30 ~ 40min ,关闭电源,电泳完毕。
4 . 染色
在电泳结束前 10min 配制染色应用液,取未用过的 2.5cm × 8cm 醋纤膜一条,使其漂浮在染色液上直到膜条完全湿透。将电泳毕的膜条自电泳槽内取出,点样面朝上贴于载玻片上。然后取出浸泡在染色液中的薄膜小心覆盖于载玻片的电泳膜上,切勿拖动,操作需迅速,避免起泡和干燥。将载玻片移置于有盖搪瓷盘内,盘内放一块湿润的纱布,以保持盘内湿度,置 37 ℃ 恒温水浴箱中,保温 40min (为节省时间可在 40 ℃ 温度下保温 5 ~ 10min ),在有 LDH 活性的地方即可显出紫色区带。
5 . 定量
将染色后的膜条置于固定液中固定 10min ,待干后将各区带剪下溶于 2ml 洗脱液中,待膜溶解、色泽浸出以后用分光光度计在 560nm 波长处以洗脱液调 “ 0 ” ,求得各管吸光度。
【计算】
血清中,某种 LDH 同工酶 占血清总 LDH 的百分比,按以下公式计算:
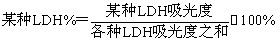
【注意事项】
1 . 红细胞内 LDH 活力比血清约高 100 倍,标本不能溶血。血清标本宜新鲜,室温下应在 24h 内做完。
2 . 所用器材必须绝对清洁,整个试验过程必须控制温度和时间,以求结果准确。
3 . 缓冲液 pH 要准确。
4 . 电泳时温度不宜过高。室温超过 25 ℃ 时需用冰降温,以免影响酶的活力。
5 . 最近有一些文献报导 LDH 同工酶 H 和 M 亚基均有突变种,导致电泳图谱有五种以上区带。
6 . 也有文献报导人血中存在有抗 H 或抗 M 抗体,以至做同工酶分析时含 H 或 M 亚基的同工酶减少,甚至完全丧失。
7 . 四氮唑蓝染色反应被用来测定同工酶活力,但有种非特异的酶被称为 “ 无名脱氢酶( Nothing dehydrogenase, 简称 NDH )也可以产生类似反应,它干扰同工酶分析。在同工酶谱上 NDH 区带位置相当于 LDH 1 和 LDH 3 处。
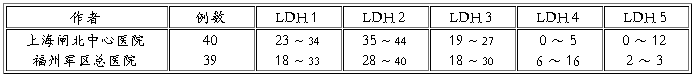
8 .不同方法测定正常值不同,用同一种方法测定,各家报告的结果亦略有差异。醋纤膜电泳分离血清 LDH 同工酶参考正常值见表 3-9 。
表 3-9 醋纤膜电泳分离血清 LDH 同工酶参考正常值( % )
9 .临床意义
在不同的组织中 LDH 同工酶谱是不同的(表 3-10 ),因此,器官损害可以在血清 LDH 同工酶谱中反映出来。 LDH 同工酶测定目前主要应用于协助心肌梗塞和某些肝脏疾病的诊断。在心肌梗塞时 LDH 1 增加, LDH 2 /LDH 1 的比率低于 1 。
血清 LDH 5 增加者可以做为急性肝炎早期指征,且可以在黄疸出现之前。持续升高或继续增加提示有慢性肝炎。肝癌 LDH 5 增加,胆汁性梗阻时 LDH 4 和 LDH 5 均增加,升高最多的是 LDH 4 。
骨骼肌损害,血清中 LDH 5 增高,创伤之后也有短暂升高,如臀部骨折及广泛性的外科手术后。
此外,活动性风湿性心肌炎,急性病毒性心肌炎、恶性贫血、获得性溶血性贫血、淋巴瘤和白血病(伴有溶血性贫血)时, LDH 4 均增高。充血性心力衰竭(代偿失调)、坏死性肝硬化、肝内肿瘤转移等, LDH 5 增加。
表 3-10 人体组织中 LDH 同工酶的分布

【思考题】
1 . 血清标本为什么要求新鲜且不应溶血?
2 .影响本实验的可能因素有哪些?应采取什么样的有效措施加以避免?
3 . 测定血清乳酸脱氢酶同工酶有何临床意义?
