实验十二 邻二氮菲分光光度法测定铁(3学时)
一、实验目的
1. 掌握用邻二氮菲分光光度法测定铁的原理和方法。
2. 练习分光光度计的操作技术。
3. 学会吸收曲线的制作,并选择测量铁的适宜波长。
二、实验原理
邻二氮菲(又称邻菲罗啉)是测定微量铁的较好试剂。在pH2~9的溶液中,试剂与Fe2+生成稳定的红色配合物,其logKf=21.3,摩尔吸光系数ε510=1.1 × 104,其反应式如下:
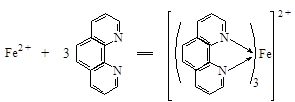
生成的红色配合物的最大吸收峰在510nm处。本方法的选择性很高,相当于含铁量40倍的Sn2+、Al3+、Ca2+、Mg2+、Zn2+、SiO32-,20倍的Cr3+、Mn2+、V(Ⅴ) 、PO43-,5倍的Cu2+、Co2+等均不干扰测定。Fe3+也能与邻二氮菲反应生成淡蓝色配合物,因此,在显色前,首先用盐酸羟胺把Fe3+离子还原为Fe2+离子,其反应式如下:
4Fe3+ + 2NH2OH·HCl → 2Fe2+ + N2↑ + 2H2O + 4H+ + 2Cl-
测定时,pH值控制在5左右,酸度高时,反应进行较慢,酸度太低,则Fe2+离子水解,影响显色。
三、仪器和试剂
(一)仪器
分光光度计1台,50mL容量瓶 8个,1mL吸量管 1支,2mL吸量管2支,5mL吸量管2支,10mL吸量管1支。
(二)试剂
(1)20μg·mL-1铁标准溶液:准确称取0.1727g NH4Fe(SO4)2·12H2O于烧杯中,加入20mL1︰1的HCl溶液和少量水,溶解后定量转至1000mL容量瓶中,稀释至刻度,摇匀。即20μg·mL-1的Fe3+标准溶液。
(2)0.15%邻二氮菲溶液(临用时配制)。
(3)10%盐酸羟氨溶液(临用时配制)。
(4)l mol·L-1NaAc溶液。
四、实验内容
(一)吸收曲线的绘制
用吸量管移取0.00、5.00mL的20μg·mL-1Fe3+标准溶液于2只50mL容量瓶中,各加入1mL10%盐酸羟氨溶液,摇匀,加入5mL 1mol·L-1NaAc溶液和2mL0.15%邻二氮菲溶液,用水稀释至刻度,摇匀。以试剂空白溶液为参比溶液,用分光光度计在430~570nm间,每隔20nm测定一次吸光度A,然后以波长λ为横坐标,吸光度A为纵坐标绘出吸收曲线,从而选择测量铁的适宜波长。
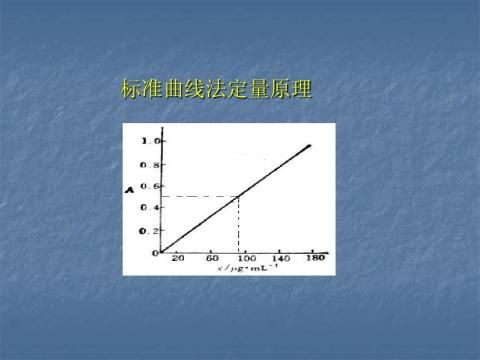
(二)标准曲线的绘制
分别吸取0.00、1.00mL、2.00mL、3.00mL、4.00mL、5.00mL 20μg·mL-1的Fe3+标准溶液于6只已编号的50mL容量瓶中,各加入1mL10%盐酸羟氨溶液,充分摇匀后加入5mL 1mol·L-1NaAc溶液和2mL0.15%邻二氮菲溶液,用水稀释至刻度,摇匀。以试剂空白为参比溶液,用分光光度计,在510nm处分别测定各溶液的吸光度,然后绘制标准曲线。
(三)未知溶液中铁含量测定
用吸量管吸取5.00mL未知液于50mL容量瓶中,其它步骤均同上,测定其吸光度。据未知液的吸光度,在标准曲线上查出5.00mL未知液中的铁含量,并以每毫升未知液中含铁微克数表示。

思考题
1.Fe3+离子标准溶液在显色前加盐酸羟胺的目的是什么?如测定一般铁盐的总铁量,是否需要加盐酸羟胺?
2.如用配制已久的盐酸羟胺溶液,对分析结果将带来什么影响?
3.为什么在分光光度法中必须使用参比溶液?
4.显色时,加入还原剂、缓冲溶液、显色剂的顺序可否颠倒?为什么?
5.何谓吸收曲线?何谓标准曲线?各有何实际意义?
6.吸光度A与百分透光率T之间的关系如何?分光光度法测定时,A值取什么范围为宜?为什么?怎么来加以控制? A为何值时测定误差最小?
第二篇:邻二氮菲分光光度法 测定水样中的铁含量