实验七 邻二氮菲分光光度法测定铁的含量
一、实验目的
1.学会吸收曲线及标准曲线的绘制,了解分光光度法的基本原理。
2.掌握用邻二氮菲分光光度法测定微量铁的方法原理。
3.学会722S型分光光度计的正确使用,了解其工作原理。
4.学会数据处理的基本方法。
5.掌握比色皿的正确使用。
二、实验原理
根据朗伯—比耳定律:A=εbc,当入射光波长λ及光程b一定时,在一定浓度范围内,有色物质的吸光度A与该物质的浓度c成正比。只要绘出以吸光度A为纵坐标,浓度c为横坐标的标准曲线,测出试液的吸光度,就可以由标准曲线查得对应的浓度值,即未知样的含量。同时,还可应用相关的回归分析软件,将数据输入计算机,得到相应的分析结果。
用分光光度法测定试样中的微量铁,可选用的显色剂有邻二氮菲(又称邻菲罗啉)及其衍生物、磺基水杨酸、硫氰酸盐等。而目前一般采用邻二氮菲法,该法具有高灵敏度、高选择性,且稳定性好,干扰易消除等优点。
在pH=2~9的溶液中,Fe2+与邻二氮菲(phen)生成稳定的桔红色配合物Fe(phen)32+,

此配合物的lgK稳=21.3,摩尔吸光系数ε510 = 1.1×104 L·mol-1·cm-1,而Fe3+能与邻二氮菲生成3∶1配合物,呈淡蓝色,lgK稳=14.1。所以在加入显色剂之前,应用盐酸羟胺(NH2OH·HCl)将Fe3+还原为Fe2+,其反应式如下:
2Fe3+ + 2NH2OH·HCl → 2Fe2+ + N2 + H2O + 4H+ + 2Cl-
测定时控制溶液的酸度为pH≈5较为适宜。
三、仪器与试剂
722S型或721型分光光度计、容量瓶(100mL,50mL)、吸量管
1、铁标准溶液:含铁0.1mg/ml。
准确称取0.8634g的NH4Fe(SO4)2·12H2O,置于烧杯中,加入20ml1:1HCl和少量水,溶解后,定量地转移至1升容量瓶中,以水稀释之刻度,摇匀。
2、邻二氮菲:0.15%(10-3mol/L)新配制的水溶液。
3、盐酸羟胺: 10%水溶液(临用时配制)
4、醋酸钠溶液 1mol/L
四、实验步骤
1.标准溶液配制
1) 10μg·mL-1铁标准溶液配制 准确称取0.8634g硫酸铁铵NH4Fe(SO4)2·12H2O于100mL烧杯中,加60mL 3mol·L-1 H2SO4溶液,溶解后定容至1L,摇匀,得100μg·mL-1储备液(可由实验室提供)。用时吸取10.00mL稀释至100mL,得10μg·mL-1工作液。
2) 系列标准溶液配制 取6个50mL容量瓶,分别加入铁标准溶液0.00,2.00,4.00,6.00,8.00,10.00mL,然后加入1mL盐酸羟胺,2.00mL邻二氮菲,5mLNaAc溶液(为什么?),每加入一种试剂都应初步混匀。用去离子水定容至刻度,充分摇匀,放置10min。
2.吸收曲线的绘制
选用1cm比色皿,以试剂空白为参比溶液(为什么?),取4号容量瓶试液,选择440~560nm波长,每隔10nm测一次吸光度,其中500~520nm之间,每隔5nm测定一次吸光度。以所得吸光度A为纵坐标,以相应波长λ为横坐标,在坐标纸上绘制A与λ的吸收曲线。从吸收曲线上选择测定Fe的适宜波长,一般选用最大吸收波长λmax为测定波长。
3.标准曲线(工作曲线)的绘制
用1cm比色皿,以试剂空白为参比溶液,在选定波长下,测定各溶液的吸光度。在坐标纸上,以铁含量为横坐标,吸光度A为纵坐标,绘制标准曲线。
4.试样中铁含量的测定
从实验教师处领取含铁未知液一份,放入50mL容量瓶中,按以上方法显色,并测其吸光度。此步操作应与系列标准溶液显色、测定同时进行。
依据试液的A值,从标准曲线上即可查得其浓度,最后计算出原试液中含铁量(以μg·mL-1表示)。并选择相应的回归分析软件,将所得的各次测定结果输入计算机,得出相应的分析结果。
五.数据处理
1.数据
分光光度计型号 ,比色皿厚 ,光源电压
(1)吸收曲线的绘制

(2)标准曲线的绘制与铁含量的测定
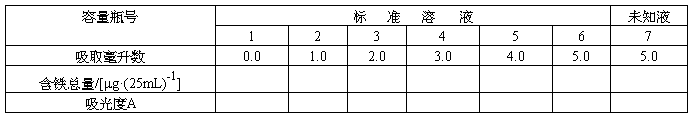
2.绘制以下曲线
(1)吸收曲线 (2)标准曲线
3.计算未知液中铁的含量
C铁=Cx/5×10-3(g/L)
式中:Cx—未知液吸光度在标准曲线上对应的含铁总量μg/25mL
六.思考题
1.本实验中哪些试剂应准确加入,哪些不必严格准确加入?为什么?
2.加入盐酸羟胺的目的是什么?
3.配制NH4Fe(SO4)2·12H2O溶液时,能否直接用水溶解?为什么?
4.如何正确使用比色皿?
5.何谓“吸收曲线”、“工作曲线”? 绘制及目的各有什么不同?
七.分光光度计(722S型)的使用方法
分光光度计是根据物质对光的选择性吸收来测量微量物质浓度的。722S型光栅分光光度计是数字显示的单光束、可见分光光度计。它具有灵敏度和准确度高、操作简便、快速等优点,允许测量的波长范围为330~800nm,吸光度的显示范围为0~1.999,是在可见光区进行吸光光度分析的常用仪器。
1.测量原理
一束单色光通过有色溶液时,一部分光线通过,一部分被吸收,一部分被器皿的表面反射。设I0为入射光的强度,I为透过光的强度,则I/I0称为透光度,用T表示。透光度越大,光被吸收越少。把lgI0/I定义为吸光度,用A表示。吸光度越大,溶液对光的吸收越多。吸光度A与透光度T之间的关系为A=lg[SX()1[]T[SX]]。吸光度A与待测溶液的浓度c(mol· L-1)和液层的厚度b(cm)成正比,即:A=εbc。这是光的吸收定律,亦称朗伯-比耳(Lambert-Beer)定律。式中ε为比例常数,叫摩尔吸收系数,它与入射光的波长、溶液的性质、温度等因素有关。当入射光波长一定,溶液的温度和比色皿(溶液的厚度)均一定时,则吸光度A只与溶液浓度c成正比。将单色光通过待测溶液,并使通过光射在光电管上变为电讯号,在数字显示器上可直接读出吸光度A或浓度c。
2.仪器构造
722S型分光光度计由光源室、单色器、试样室、光电管暗盒、电子系统及数字显示器等部件组成。其结构如图3-3所示,外形如教材P104页图3-3所示。
3.使用方法
(1)取下防尘罩,将灵敏度调节旋钮13置于“1”档(信号放大倍率最小)。
(2)接通电源,按下仪器上的电源开关7,指示灯即亮。将选择开关3置于“T”
档(即透光度)。调节波长手轮8使波长刻度盘9中标线对准的波长为所需波长。仪器预热20min。
(3)打开试样室盖(光门自动关闭),调节0%T旋钮12,使显示“00.0”。
(4)把盛参比溶液的比色皿放入试样架的第一格内,盛试样的比色皿放入第二、
三、四格内,然后盖上试样室盖(光门打开,光电管受光)。推动试样架拉手10把参比溶液推入光路,调节100%T旋钮11,使之显示为“100.0”,若显示不到“100.0”,应增大灵敏度档,但尽可能倍率置低档使用,这样仪器将有更高的稳定性。改变灵敏度后,应按(3)重新调“0”后再调节100%T旋钮,直至显示为“100.0”。
(5)重复(3)和(4)操作,显示稳定后即可进行测定工作。
(6)吸光度A的测量:稳定地显示“100.0”透光度后,将选择开关置于“A”
档(即吸光度),此时吸光度显示应为“00.0”,若不是,则调节吸光度调零旋钮2,使显示为“00.0”,然后将试样推入光路,这时的显示值即为试样的吸光度。
(7)浓度C的测量:选择开关由“A”旋置“C”,将已标定浓度的样品放入光路,
调节浓度旋钮5,使得数字显示为标定值,将被测样品放入光路,即可读出被测样品的浓度值。
(8)测定完毕,关闭仪器电源开关(短时间不用,不必关闭电源,可打开试样室
盖,即可停止照射光电管),将比色皿取出,洗干净,擦干,放回原处。拔下电源插头,待仪器冷却10min后盖上防尘罩。
4.注意事项
(1) 测定过程中,不要将参比溶液拿出试样室,应将其随时推入光路以检查吸
光度零点是否变化。如不为“00.0”,则不要先调节旋钮2,而应将选择开关3置于“T”档,用100%旋钮调至“100.0”,再将选择开关置于“A”,这时如不为“00.0”,才可调节旋钮2。
(2) 为了避免光电管长时间受光照射引起的疲劳现象,应尽可能减少光电管受
光照射的时间,不测定时应打开暗室盖,特别应避免光电管受强光照射。
(3)使用前若发现仪器上所附硅胶管已变红应及时更换硅胶。
(3) 比色皿盛取溶液时只需装至比色皿的3/4即可,不要过满,避免在测定的
拉动过程中溅出,使仪器受湿、被腐蚀。
(5)若大幅度调整波长,应稍等一段时间再测定,让光电管有一定的适应时间。(6)每台仪器所配套的比色皿,不能与其它仪器上的比色皿单个调换。
(7)仪器上各旋钮应细心操作,不要用劲拧动,以免损坏机件。若发现仪器工
作异常,应及时报告指导教师,不得自行处理。
第二篇:04实验四 邻二氮菲分光光度法测定铁的含量-教案
实验四邻二氮菲分光光度法测定铁的含量教案
课程名称:分析化学实验B
教学内容:邻二氮菲分光光度法测定铁的含量
实验类型:验证
教学对象:化工、环境工程、药学、生物科学、应用化学、医学检验、制药、复合材料、生物工程、生物技术
授课地点:中南大学南校区化学实验楼401
授课学时:4学时
一、教学目的与要求
1、练习巩固吸量管、比色管(容量瓶)、比色皿的正确使用;
2、了解分光光度法的基本原理,学会吸收曲线测绘及选择测定波长和标准曲线的绘制;
3、掌握用邻二氮菲分光光度法测定微量铁的原理、方法和计算;
4、学习掌握722S型分光光度计的正确使用,了解其工作原理;
5、掌握利用标准曲线法进行定量分析的操作与数据处理方法。
二、知识点
分光光度法、朗伯—比耳定律、配位反应、显色反应、标准溶液、吸收曲线、最大吸收波长、标准曲线、吸量管、比色管、比色皿、实验报告的撰写(数据处理三线表表格化)、有效数字
三、技能点
玻璃器皿的洗涤、吸量管的使用、标准系列溶液的配制、比色皿的使用、分光光度计的使用
四、教学重点及难点
重点:邻二氮菲分光光度法测定微量铁的基本原理和操作方法
难点:722s型分光度计的操作
五、教学方法
任务驱动法、分组讨论法、阅读指导法、现场讲解指导等
六、复习引入
1、复习分光光度法有关知识,提问学生:
(1) 分光光度法测定对象是什么?(有色溶液物质)
(2) 在用分光光度法测定微量铁中,以什么试剂作显色剂?(邻二氮菲)
(3) 测定波长如何选择?(吸收曲线)
[引入] 分光光度法的应用:邻二氮菲分光光度法测定微量铁-标准曲线法
[引言] 铁是最重要的基本结构材料,铁合金用途很广,国防和战争更是钢铁的较量,钢铁的年产量代表一个国家的现代化水平,因而,对各种样品中所含的铁进行测定,有助于对产品的生产进行监督。
测定铁的方法很多,选择不同方法主要是看不同样品中铁的含量,含量高的含铁试样采用滴定分析法测定,含量低的含铁试样采用仪器分析方法测定。常用的仪器分析方法有分光光度法、原子吸收分光光度法、原子发射光谱法等,其中邻二氮菲分光光度法测定微量铁的含量是国际国内规定的标准分析方法,因而生产和实验室中广泛采用标准曲线法邻二氮菲分光光度法测定微量铁的方法测定样品中微量铁的含量。
[新授]课题:邻二氮菲分光光度法测定铁的含量-标准曲线法
[提出任务]教师提出本课题的学习任务:
1、邻二氮菲分光光度法测定铁的基本原理是什么?
2、邻二氮菲吸光光度法测定微量铁的实验中,吸收曲线与标准曲线有何区别?
3、邻二氮菲分光光度法测定铁的操作方法。
[任务探索]
1、邻二氮菲分光光度法测定铁的基本原理是什么?
根据有关学习资料,思考下列问题:
(1) 邻二氮菲分光光度法测定铁中的铁主要是由什么形式存在?如何保障溶液中的铁离子是以邻二氮菲络合铁的价态形式存在?
(2) 邻二氮菲络合铁时,溶液pH值最好控制在多少?用什么缓冲溶液调节溶液pH?
(3) 邻二氮菲分光光度法测定铁时,哪些离子有干扰?如何消除干扰?
[归纳]引导学生归纳总结出邻二氮菲分光光度法测定铁的基本原理
测定溶液中的微量铁,一般采用邻二氮菲分光光度法。即在pH=3~9的溶液中,Fe2+与邻二氮菲(phen)生成稳定的桔红色配合物Fe(phen)32+, 反应如下:
2Fe3+ + 2NH2OH·HC1=2Fe2+ +N2↑+2H2O+4H++2C1-

根据朗伯—比耳定律:A=εbc,当入射光波长λ及光程b一定时,在一定浓度范围内,有色物质的吸光度A与该物质的浓度c成正比。采用标准曲线分析方法,测定被测物质中微量铁的含量。
[学生回答]
(1) 邻二氮菲分光光度法测定铁中的铁主要是由什么价态形式存在?如何保障溶液中的铁离子是以邻二氮菲络合铁的价态形式存在?
邻二氮菲分光光度法测定铁中的铁主要是以Fe2+离子形式存在的。通常在酸性条件下,加入盐酸羟胺或抗坏血酸来保障溶液中的铁离子是Fe2+离子形式存在。
(2) 邻二氮菲络合铁时,溶液pH值最好控制在多少?用什么缓冲溶液调节溶液pH?
[讲解] 溶液pH值最好控制在5左右。用HAc-NaAc缓冲溶液调节溶液pH值。
(3) 邻二氮菲分光光度法测定铁时,哪些离子有干扰?如何消除干扰?
[讲解] 产生干扰的离子较多,根据干扰的特性不同,选用适当的方法进行掩蔽或分离而消除干扰。样品中若含三价铁离子、钴、镍、铜等共存离子,会干扰Fe2+的测定,可以加入盐酸羟胺、KCN等掩蔽消除干扰。
2、邻二氮菲吸光光度法测定微量铁的实验中,吸收曲线与标准曲线有何区别?
[讲解] 吸收曲线和标准曲线是两个完全不同用途的曲线,吸收曲线一般是指做全波段扫描时候的信号曲线,为吸光度-波长曲线,用于确定测定样品所用的最佳波长;标准曲线一般是在定波长测定时,用不同浓度的标准样品作为不同的样品点,测定绘制而成的吸光度-浓度曲线,根据样品测得的吸光度值,可从曲线上查找或计算出样品的浓度。
3、邻二氮菲分光光度法测定铁的操作方法。
[阅读] 指导学生阅读实验报告中的实验步骤。
[讨论] 四个学生一组,归纳测定操作要点。
[提问] 学生代表小组发言:邻二氮菲分光光度法测定铁的测定步骤
(1) 系列标准溶液及分析试液的配制
取6只25mL比色管,用5ml吸量管分别加入铁标准工作溶液0.00、1.00、2.00、3.00、4.00、5.00mL,另取3只25mL比色管,分别加入含铁分析试液5.00mL,然后加入1mL盐酸羟胺,2.00mL邻二氮菲,5mLNaAc溶液,每加入一种试剂都应混匀。用去离子水定容至刻度,充分摇匀,放置10min,待测。
(2)722s型分光度计操作步骤
(a) 开机
(b) 定波长入=510nm
(c) 打开盖子调零T=0。
(d) 关上盖子,调满刻度至T=100(A=0)。
(e) 参比溶液比色皿放入其中,均合T=100调满(A=0)。
(f) 第一格不动,二,三,四格换上标液(共计六个点)调换标液时先用蒸馏水清洗后,再用待测液(标液)清洗,再测其分光度
(3) 吸收曲线(获得最佳工作波长)
选用1cm比色皿,以试剂空白(1号)为参比溶液,取4号比色管试液,在440~560nm波长范围内,每隔10nm测一次吸光度,其中500~520nm之间,每隔5nm测定一次吸光度(每改变一次波长,都要在参比溶液下调整T=0、T=100、A=0)。以所得吸光度A为纵坐标,以相应波长λ为横坐标,在坐标纸上绘制A与λ的吸收曲线。从吸收曲线上选择最大吸收波长λmax作为测定波长。
(4) 标准曲线(获得线性范围)及测定分析样品的吸光度A
用1cm比色皿,以试剂空白(1号)为参比溶液,在选定波长下,测定各溶液的吸光度。在坐标纸上,以铁含量(浓度单位是××μg/25ml)为横坐标,吸光度A为纵坐标,绘制标准曲线。依据试液的A值,从标准曲线上即可查得其浓度,计算出原含铁分析试液中含铁含量(以mg·L-1表示)。(按下式计算)
ρFe=cx/5
(5) 数据记录与处理及结论
(a) 吸收曲线的绘制
表1 不同波长下的吸光度

以吸光度A为纵坐标,以相应波长λ为横坐标,在坐标纸上绘制吸收曲线。
(b) 标准曲线的绘制与铁含量的测定
表2 不同浓度长下的吸光度

以铁含量(浓度单位是××μg/25ml)为横坐标,吸光度A为纵坐标,在坐标纸上绘制标准曲线。依据未知液的A值,从标准曲线上即可查得其对应浓度。
(c)原含铁分析试液中含铁含量

结论:铁未知液中铁的含量ρFe=
95%置信度下平均值的置信区间ρFe=
[小结] 用邻二氮菲分光光度法测定铁是国际国内规定的标准分析方法。在酸性条件下,加入盐酸羟胺,保障溶液中的铁离子是Fe2+离子形式存在,在pH=5的醋酸缓冲溶液中,以邻二氮菲为显示剂,与Fe2+生成一种稳定的桔红色络合物Fe(phen) 32+,用分光光度法测定物质的含量。定量测定方法一般采用标准曲线法,即配制一系列浓度的标准溶液,在实验条件下依次测量各标准溶液的吸光度(A),以溶液的浓度为横坐标,相应的吸光度为纵坐标,绘制标准曲线。在同样实验条件下,测定待测溶液的吸光度,根据测得吸光度值从标准曲线上查出相应的浓度值,即可计算试样中被测物质的质量浓度。
[演示] 学生代表上讲台演示测定操作过程,其余学生观察其操作。
[讲解、示范] 教师点评学生演示操作过程的正误之处并讲解示范操作要点:
(1) 取样的方法:取样量5.0mL,取样仪器:吸量管
(2) 吸量管的操作:吸液、调整液面的方法、放液
(3) 分光光度计的操作:
(a) 预热30min。
(b) 调节T = 0。
(c) 调节T = 100% (A=0)。
(d) 测定样品的吸光度A。
[讲解注意事项]
1、试剂的加入必须按顺序进行;
2、定容后必须充分摇匀后进行测量;
3、分光光度计必须预热30min,稳定后才能进行测量;
4、比色皿必须配套,装上待测液后透光面必须擦拭干净;切勿用手接触透光面;
5、在进行条件试验时,每改变一次试液浓度,比色皿都要洗干净;
6、同一组溶液必须在同一台仪器上测量;
7、标准曲线的质量是测定准确与否的关键,标准系列溶液配制时,必须严格按规范进行操作
8、 待测溶液一定要在工作曲线线形范围内,如果浓度超出直线的线性范围,则有可能偏离朗伯-比耳定律是光吸收的基本定律,就不能使用吸光光度法测定。
[学生分组] 以每两个同学一组分为12~16个小组
[学生实训] 测定样品中的铁含量并完成实验报告。教师巡回指导
[交流讨论] 引导学生说出自己完成任务的情况 (成功或失误之处)
[试验小结] 教师小结本课题实验完成情况。
1、吸量管的规范操作:克服多加或少加的现象;
2、分光光度计使用时的注意事项:(1)为了防止光电管疲劳,不测定时必须将试样室盖打开,使光路切断,以延长光电管的使用寿命。 (2)取拿比色皿时,手指只能捏住比色皿的毛玻璃面,而不能碰比色皿的光学表面。 (3)比色皿不能用碱溶液或氧化性强的洗涤液洗涤,也不能用毛刷清洗。比色皿外壁附着的水或溶液应用擦镜纸或细而软的吸水纸吸干,不要擦拭,以免损伤它的光学表面。
3、分析误差产生原因:取液不当;溶液没有摇匀;显色时间不足;改动了仪器的工作条件等因素。
[布置作业]:根据你的测定,我们本地区的水中铁的浓度在什么范围?(写出测定实验操作步骤、实验数据和测定结果)
