AEFI个案报告卡
1. 县国标码* 2. 发生年份 3. 编号 4. 姓名* 5. 性别* 6. 出生日期* 7. 职业 8. 现住址 9. 联系电话 10. 监护人
1男 2女
年 月 日
□□□□□□
□□□□ □□□□
□
□□□□/□□/□□
□□
12. 反应发生日期* 13. 发现/就诊日期* 14. 就诊单位 15. 主要临床经过* 16. 是否住院* 17. 反应获得方式* 18. 报告日期* 19. 报告单位 20. 报告人 21. 联系电话
年 月 日 年 月 日 1是 2否
1被动监测报告 2主动监测报告 年 月 日
□□□□/□□/□□ □□□□/□□/□□
□ □
□□□□/□□/□□
说明:① * 为关键项目;②按照“AEFI个案调查表填表说明”的有关项目填写。
1
群体性AEFI登记表
群体性AEFI编码: 县国标码□□□□□□ 首例发生年份□□□□ 编号□□ 发生地区: 疫苗名称*: 生产企业*: 规格(剂/支或粒) : 有无批签发合格证: 接种单位: 接种人数*: 反应发生人数*: 报告单位: 报告人: 联系电话:

2
AEFI个案调查表
一、基本情况
1. 县国标码* 2. 发生年份 3. 编号 4. 姓名* 5. 性别* 6. 出生日期* 7. 职业 8. 现住址 9. 联系电话 10. 监护人
1男 2女
年 月 日
1有 2无 3不详
1有 2无 3不详
1有 2无 3不详
1有 2无 3不详 年 月 日
疫苗1
疫苗2
疫苗3
疫苗4 □□□□□□
□□□□ □□□□
□
□□□□/□□/□□
□□
□ □ □ □
□□□□/□□/□□
二、既往史
1. 接种前患病史
如有,疾病名称 2. 接种前过敏史
如有,过敏物名称 3. 家族患病史
如有,疾病名称 4. 既往异常反应史
如有,反应发生日期 接种疫苗名称 临床诊断
1. 疫苗名称* 2. 规格(剂/支或粒) 3. 生产企业* 4. 疫苗批号* 5. 有效日期 6. 有无批签发合格证 7. 疫苗外观是否正常 8. 保存容器 9. 保存温度(℃) 10. 送检日期 11. 检定结果是否合格
三、可疑疫苗情况(按最可疑的疫苗顺序填写)
疫苗1
疫苗2
疫苗3
疫苗4
3
四、稀释液情况
1. 稀释液名称
2. 规格(ml/支) 3. 生产企业 4. 稀释液批号 5. 有效日期 6. 稀释液外观是否正常 7. 保存容器 8. 保存温度(℃) 9. 送检日期 10. 检定结果是否合格
疫苗1 疫苗2 疫苗3 疫苗4
疫苗1 疫苗2 疫苗3 疫苗4
年 月 日
年 月 日
1轻度(37.1-37.5) 2中度(37.6-38.5)
3重度(≥38.6) 4 无
1弱反应(≤2.5) 2中反应(2.6-5.0)
3强反应(>5.0) 4无
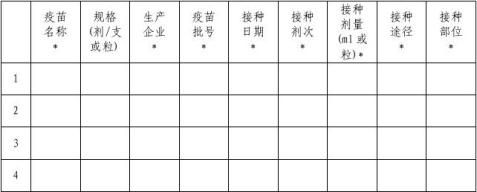
1有 2无 □□□□/□□/□□ □□□□/□□/□□ □ □ □ 五、注射器情况 1. 注射器名称 2. 注射器类型 3. 规格(ml/支) 4. 生产企业 5. 注射器批号 6. 有效日期 7. 送检日期 8. 检定结果是否合格 六、接种实施情况 1. 接种日期* 2. 接种剂次* 3. 接种剂量(ml或粒)* 4. 接种途径* 5. 接种部位* 6. 接种单位 7. 接种地点 8. 接种人员 9. 有无预防接种培训合格证 10. 接种实施是否正确* 七、临床情况 1. 反应发生日期* 2. 发现/就诊日期* 3. 就诊单位 4. 主要临床经过* 发热(腋温℃)* 局部红肿(直径cm) * 局部硬结*
4
5. 是否住院*
如是,医院名称 病历号 住院日期 出院日期 6. 病人转归*
如死亡,死亡日期 是否进行尸体解剖 尸体解剖结论
1是 2否
年 月 日 年 月 日
1痊愈 2好转 3 后遗症 4死亡 5不详 年 月 日 1是 2否
□
□□□□/□□/□□ □□□□/□□/□□
□
□□□□/□□/□□
□
八、其他有关情况
1. 疫苗流通情况及接种组
织实施过程
2. 同批次疫苗接种剂次数
及反应发生情况 3. 同品种疫苗既往接种剂
次数及反应发生情况 4. 当地类似疾病发生情况
1被动监测报告 2主动监测报告 年 月 日
年 月 日
1 调查组 2专家组
1一般反应 2异常反应 3疫苗质量事故 4实施差错事故 5偶合症 6心因性反应 7不明原因 8待定
如为异常反应,机体 损害程度 3. 临床诊断* 4. 是否群体性AEFI
说明:① * 为关键项目;②按照“AEFI个案调查表填表说明”填写。
□
□□□□/□□/□□
□□□□/□□/□□
□ □
九、报告及调查情况
1. 反应获得方式* 2. 报告日期* 3. 报告单位 4. 报告人 5. 联系电话 6. 调查日期* 7. 调查单位 8. 调查人
十、结论
1. 做出结论的组织* 2. 反应分类*
1一级甲 2一级乙 3二级甲 4二级乙 5三级甲 6三级乙 7四级 8待定 1是 2否
□ □□ □
如是,群体性AEFI编码 □□□□□□□□□□□□
5
AEFI个案调查表填表说明
一、基本情况
1.县国标码:填写报告单位所在县(市、区)的6位国标码,例如东城区“110101”。
2.发生年份:填写AEFI发生的4位年份,不是反应报告或调查年份。“发生年份”应与“发生日期”的年份一致。
3.编号:填写反应的4位流水号,如0001。“县国标码+发生年份+编号”可生成反应的唯一编码,即ID编码,因此,同一县同一发生年份的编号不能重复。
4.姓名:填写病人真实姓名,尚未取名的儿童可填写父或母姓名+“子”或“女”。
5.性别:选填1-男 2-女。
6.出生日期:按年月日格式填写,日期指公历日期(下同)。
7.职业:选填01-幼托儿童 02-散居儿童 03-大学生 04-中学生 05-小学生06-教师 07-保育员及保姆 08-餐饮食品业 09-商业服务 10-医务人员 11-工人 12-民工 13-农民 14-牧民 15-渔(船)民 16-干部职员 17-离退人员 18-家务及待业 19-其他。
8.现住址:填写病人当前的家庭住址,包括省、市、县、乡、村各级名称和门牌号。
9.联系电话:填写病人的联络电话,如为儿童,填写其监护人电话,号码内包括地区码。
10. 监护人:如果病人为儿童,填写其监护人姓名。
二、既往史
1.接种前患病史:接种前1个月内有无患过或现患某种疾病(如发热、感冒、传染病、遗传病、慢性病等),选填1-有 2-无 3-不详。如有,疾病名称:填写所患全部疾病的名称。
2.接种前过敏史:选填1-有 2-无3-不详。如有,过敏物名称:填写过敏物(如疫苗、血清、药物、花粉、食物等)的名称。
3.家族患病史:三代以内直系亲属成员中有无遗传病、传染病、精神病、癫痫、过敏或惊厥等病史,选填1-有 2-无 3-不详。如有,疾病名称:填写所患全部疾病的名称。
4.既往异常反应史:在既往接种疫苗中有无发生异常反应,选填1-有 2-无3-不详。如有,反应发生日期:按“年月日”格式填写。接种疫苗名称:指发生异常反应的既往接种疫苗名称,按《儿童预防接种信息管理系统数据交换集成标准》(简称《集成标准》,中疾控信发[2007]154号)的“疫苗名称编码表”填写。临床诊断:填写临床诊断的病名,按“AEFI临床诊断编码表”填写。
AEFI临床诊断编码表:01-无菌性脓肿 02-热性惊厥 03-过敏性休克 04-过敏性皮疹 05-过敏性紫癜 06-血小板减少性紫癜 07-局部过敏反应(Arthus反应) 08-血管性水肿 09-其他系统过敏性反应 10-多发性神经炎 11-急性多发性神经根炎(格林巴利综合征) 12-臂丛神经炎 13-癫痫 14-脑病 15-脑炎和脑膜炎 16-类中毒性休克综合征 17-疫苗相关麻痹型脊髓灰质炎 18-卡介苗淋巴结炎 19-卡介苗骨髓炎 20-全身播散性卡介苗感染 21-局部化脓性感染-局部脓肿 22-局部化脓性感染-淋巴管炎和淋巴结炎 23-局部化脓性感染-蜂窝织炎 24-全身化脓性感染-毒血症 25-全身化脓性感染-败血症 26-全身化脓性感染-脓毒血症 27-晕厥 28-癔症 99-其它
三、可疑疫苗情况
AEFI通常涉及一种疫苗/生物制品,但个别情况下病人可能同时或先后接种数种疫苗(一般最多4种)。因此,必须对所有的可疑疫苗进行调查,按最可疑的疫苗顺序填写此项内容,与反应根本无关的疫苗不必填写。例如,同时接种了OPV(口服)、DPT(左臂)和HepB(右臂)后,在左臂注射部位出现无菌化脓,则可以完全排除系OPV和HepB引起,只填写DPT即可;但如果出现全身过敏性皮疹,则3种疫苗均有可能引起,都应填写,最可疑的疫苗排在前面。
1.疫苗名称:按《集成标准》的“疫苗名称编码表”填写。
2.规格:按“剂/支(粒)”填写疫苗的规格,只填数字。例如DPT为4剂/支,填写“4”即可, OPV为1剂/粒,填写“1”即可。
3.生产企业:按《集成标准》的“疫苗生产企业编码表”填写。
4.疫苗批号:填写接种疫苗安瓿或包装上所标名的批号。
5.有效日期:指有效截至日期,按“年月日”格式填写。如果接种疫苗安瓿或包装上所标 1
名的不是有效日期 和 “年月日”格式,则转化成此格式。例如,“生产日期20xx年4月1日,有效期1年”,则有效日期为“20xx年3月31日”; “有效期至20xx年8月”,则有效日期为“20xx年8月31日”;“失效期20xx年4月25日”,则有效日期为“20xx年4月24日” ;“失效期20xx年4月”,则有效日期为“20xx年3月31日”。
6.有无批签发合格证书:查看疫苗批签发合格证书的复印件,选填1-有 2-无。
7.疫苗外观是否正常:检查同批号剩余疫苗有无变色、霉变、异常沉淀物或安瓿有无裂纹
等,选填1-是 2-否。
8.保存容器:接种过程中疫苗保存在何处,选填1-冰箱 2-冷藏箱 3-冷藏包 4-其它。
9.保存温度:填写保存疫苗的摄氏温度,只填写数字,例如4℃,填写“4”即可。
10. 送检日期:按“年月日”格式填写。
11. 检定结果是否合格:疫苗检定机构对疫苗的所有检定结果是否合格,
选填1-是,2-否。
四、 稀释液情况
1.稀释液名称:如果疫苗有稀释液,填写稀释液安瓿标明的名称。
2.规格:每支稀释液的毫升数,只填写数字,如10ml/支,填“10”即可。
3.生产企业:填写生产稀释液的企业名称。
4.稀释液批号:填写稀释液安瓿或包装上标明的批号。
5.有效日期:有效截至日期,按“年月日”格式填写,如果稀释液安瓿或包装上所标名的
不是有效日期和“年月日”格式,则转化成此格式。
6.稀释液外观是否正常:判断同批号剩余稀释液有无变色、霉变、异常沉淀物或安瓿有无
裂纹等,选填1-是 2-否。
7.保存容器:接种过程中稀释液保存在何处,选填1-冰箱 2-冷藏箱 3-冷藏包 4-其它。
8.保存温度:填写保存稀释液的摄氏温度,只填写数字,例如4℃,填写“4”即可。
9.送检日期:按“年月日”格式填写。
10. 检定结果是否合格:稀释液检定机构对稀释液的检定结果是否合格,
选填1-是,2-否。
五、注射器情况
1.注射器名称:填写注射器的商品名称,例如BD等。
2.注射器类型:选填1-一次性注射器 2-自毁型注射器 3-玻璃注射器 4-其它。
3.规格:注射器的容积规格(ml数),只填写数字(保留1位小数),如0.5ml,填写 “0.5”。
4.生产企业:填写生产注射器的企业名称。
5.注射器批号:填写注射器或包装上标明的批号。
6.有效日期:指有效截至日期,按“年月日”格式填写。
7.送检日期:按“年月日”格式填写。
8.检定结果是否合格:注射器检定机构对注射器的检定结果是否合格,选填1-是,2-否。
六、接种实施情况
1.接种日期:按“年月日”格式填写。
2.接种剂次:疫苗接种的第几剂(针),只填写数字,例如DPT第2针,填写“2”即可。
3.接种剂量:填写接种的疫苗剂量,脊灰糖丸疫苗或某些胶囊疫苗的剂量单位为“粒”,
注射疫苗为“ml”。只填写数字,例如DPT接种0.5ml,填写“0.5”。
4.接种途径:选填1-肌内 2-皮下 3-皮内 4-口服 5-其它。
5.接种部位:选填1-左上臂 2-右上臂 3-左臀部 4-右臀部 5-大腿内侧 6-其它。
6.接种单位:填写接种单位代码,即县国标码6位+乡编号2位+接种单位编号2位。
7.接种地点:选填1-医院或卫生院 2-村卫生室 3-学校 4-家中 5-其它。
8.接种人员:填写实施疫苗接种的人员姓名。
9.有无预防接种培训合格证:接种人员有无上级部门颁发的培训合格证,选填1-有 2-无。
10. 接种实施是否正确:根据对接种过程的调查,判断接种实施的全部程序是否正确,选
填1-是 2-否。
2
七、临床情况
1.反应发生日期:反应的症状最早出现日期,按“年月日”格式填写。
2.发现/就诊日期:责任报告单位和报告人发现AEFI的日期,或诊为AEFI的最早就诊日
期。按“年月日”格式填写。
3.就诊单位:指在就诊日期就诊的医疗卫生机构名称。
4.主要临床经过:按时间顺序描述反应的发生经过,包括临床症状、体征、实验室检查(如
血液、尿液、粪便、脑脊液等)结果、辅助检查(如X线、心电图、超声波、CT等)结果、初步临床诊断以及反应的治疗手段和效果等情况。
发热(腋温℃):选填1-轻度(37.1-37.5) 2-中度(37.6-38.5) 3-重度(≥38.6) 4-无。
局部红肿(直径cm):选填1-弱反应(≤2.5) 2-中反应(2.6-5.0) 3-强反应(>5.0) 4-无。
局部硬结: 选填1-有 2-无。
5.是否住院:选填1-是 2-否。如是,医院名称:填写住院医院名称。病历号:填写住院
医院的病历号。住院日期:按“年月日”格式填写。出院日期:按“年月日”格式填写。
6.病人转归:选填1-治愈 2-好转 3-后遗症 4-死亡 5-不详。如死亡,死亡日期:按“年
月日”格式填写。是否进行尸体解剖:指是否对尸体进行病理解剖,选填1-是 2-否。尸体解剖结论:按尸体解剖诊断书上的死因诊断结论填写。
八、其它有关情况
1.疫苗流通情况及接种组织实施过程:描述可疑批号的疫苗在领发或购销、运输、储存、
接种等各环节的操作过程。
2.同批次疫苗接种剂次数及反应发生情况:描述调查者辖区内同种批号可疑疫苗的接种
数量、发生的反应和人数。
3.同品种疫苗既往接种剂次及反应发生情况:描述调查者辖区内同品种疫苗近1年内接
种的数量、发生的反应和人数。
4.当地类似疾病发生情况:描述当地近1-2年内类似疾病的发生人数、发生率。
九、报告与调查情况
1.反应获得方式:AEFI是通过被动监测(或称常规监测)报告方式还是主动监测(即接
种人员主动随访)报告方式获得,选填1-被动监测报告 2-主动监测报告。
2.报告日期:反应最早上报的日期,按“年月日”格式填写。
3.报告单位:填写反应报告的责任报告单位名称,如“某某医院”等。
4.报告人:填写反应报告人的真实姓名。
5.联系电话:填写报告单位的联系电话。
6.调查日期:按“年月日”格式填写。
7.调查单位:填写对反应进行调查的疾病控制机构名称,如“某某CDC”等。
8.调查人:填写反应调查人员的真实姓名。
十、结论
1.做出结论的组织:结论是由AEFI调查组还是预防接种异常反应诊断专家组做出,当两
种结论同时存在时,以专家组结论为准,选填1-调查组 2-专家组。
2.反应分类:AEFI发生的最终原因分类,选填1-一般反应 2-异常反应 3-疫苗质量事故 4
-实施差错事故 5-偶合症 6-心因性反应 7-不明原因 8-待定。如为异常反应,机体损害程度:选填1-一级甲 2-一级乙 3-二级甲 4-二级乙 5-三级甲 6-三级乙 7-四级 8-待定。
预防接种异常反应损害程度分级标准:一级:死亡,严重残疾。①甲等:死亡;②乙等:重要器官缺失或功能完全丧失,其他器官不能代偿,存在特殊医疗依赖,生活完全不能自理。二级:造成中度残疾、器官组织损伤,导致严重功能障碍。①甲等:器官功能缺失或功能完全丧失, 其他器官不能代偿,存在特殊医疗依赖,生活完全不能自理;②乙等:存在器官严重功能障碍, 存在特殊医疗依赖,生活部分不能自理。三级:造成轻度残疾、器官组织损伤,导致一般功能障碍。①甲等: 存 3
在较重器官功能障碍, 可能存在特殊医疗依赖,生活能自理;②乙等: 存在中度器官功能障碍, 可能存在一般医疗依赖,生活能自理。四级:造成明显健康损害或其他后果的。
3.临床诊断:填写一种最主要的临床诊断病名,按“AEFI临床诊断编码表”填写。如果
反应分类为一般反应,此项应空缺。
是否为群体性AEFI:选填1-是 2-否。如是,群体性AEFI编码:为某起群体性反应的唯一码,即县国标码6位+首例发生年份4位+编号2位;同一起群体性反应中所有个案的群体性反应编码相同。
4
