AEFI个案报告卡(1)
1. 县国标码* 2. 发生年份 3. 编号 4. 姓名* 5. 性别* 6. 出生日期* 7. 职业 8. 现住址 9. 联系电话 10. 监护人
孙硕 1男√ 2女 2011 年 3 月 19 日 散居儿童 长安村、马家屯 136xxxxxxxx 孙忠亮
□□□□□□
□□□□ □□□□
□
□□□□/□□/□□
□□
12. 反应发生日期* 13. 发现/就诊日期* 14. 就诊单位 15. 主要临床经过* 16. 是否住院* 17. 反应获得方式* 18. 报告日期* 19. 报告单位 20. 报告人 21. 联系电话
2011 年 10 月 13 日 2011 年 10月 15 日 高烧 1是 2否
1被动监测报告√ 2主动监测报告 2011 年 10 月 15 日 增盛镇防疫站 王阳 5680990
□□□□/□□/□□ □□□□/□□/□□
□ □
□□□□/□□/□□
说明:① * 为关键项目;②按照“AEFI个案调查表填表说明”的有关项目填写。
1
AEFI个案报告卡(2)
一、既往史
1. 接种前患病史
如有,疾病名称 2. 接种前过敏史
如有,过敏物名称 3. 家族患病史
如有,疾病名称 4. 既往异常反应史
如有,反应发生日期 接种疫苗名称 临床诊断
1. 疫苗名称* 2. 规格(剂/支或粒) 3. 有效日期 4. 疫苗外观是否正常 5. 保存容器 6. 保存温度(℃)
1有 2无√ 3不详
1有 2无√ 3不详
1有 2无√ 3不详
1有 2无√ 3不详 年 月 日
疫苗1 A群脑膜炎 支 2012.05.16 正常 冷藏箱 6 ℃
疫苗1 缓冲生理盐水 1.5ml/支 北京天坛生物 2010061001 2013.06.28 正常 冷藏箱 6 ℃
疫苗1 一次性使用自毁式无菌注射器
2. 注射器类型 3. 规格(ml/支) 4. 生产企业 5. 注射器批号 6. 有效日期
自毁型注射器 0.5ml 江西三鑫医疗 100820 2013.08
疫苗1 增盛镇
2
□ □ □ □
□□□□/□□/□□
疫苗3
疫苗4
二、可疑疫苗情况(按最可疑的疫苗顺序填写)
疫苗2
疫苗2
疫苗3
疫苗4
疫苗2
疫苗3
疫苗4
三、稀释液情况
1. 稀释液名称 2. 规格(ml/支) 3. 生产企业 4. 稀释液批号 5. 有效日期
6. 稀释液外观是否正常 7. 保存容器 8. 保存温度(℃)
四、注射器情况
1. 注射器名称
疫苗2
疫苗3
疫苗4
器械集团公司
五、接种实施情况
1. 接种单位 2. 接种地点
增盛镇防疫站
3. 接种人员
4. 有无预防接种培训合格证 5. 接种实施是否正确*
王阳 有 正确
□ □ □ □
□□□□/□□/□□ □□□□/□□/□□
□
□□□□/□□/□□
□
□□□□□□□□□□□□
六、临床情况
1. 就诊单位 2. 主要临床经过*
发热(腋温℃)* 局部红肿(直径cm) * 局部硬结* 3. 是否住院*
如是,医院名称 病历号 住院日期 出院日期 4. 病人转归*
如死亡,死亡日期 是否进行尸体解剖 尸体解剖结论
说明:① * 为关键项目;②按照“AEFI个案调查表填表说明”填写。
增盛镇中心卫生院
1轻度(37.1-37.5) √ 2中度(37.6-38.5) 3重度(≥38.6) 4 无
1弱反应(≤2.5) √ 2中反应(2.6-5.0) 3强反应(>5.0) 4无
1弱反应(≤2.5) √ 2中反应(2.6-5.0) 3强反应(>5.0) 4无 1是 2否√
年 月 日 年 月 日
1痊愈 2好转√ 3 后遗症 4死亡 5不详
年 月 日 1是 2否
如是,群体性AEFI编码
1
第二篇:AEFI个案报告卡和调查表表样
附表1
疑似预防接种异常反应个案报告卡
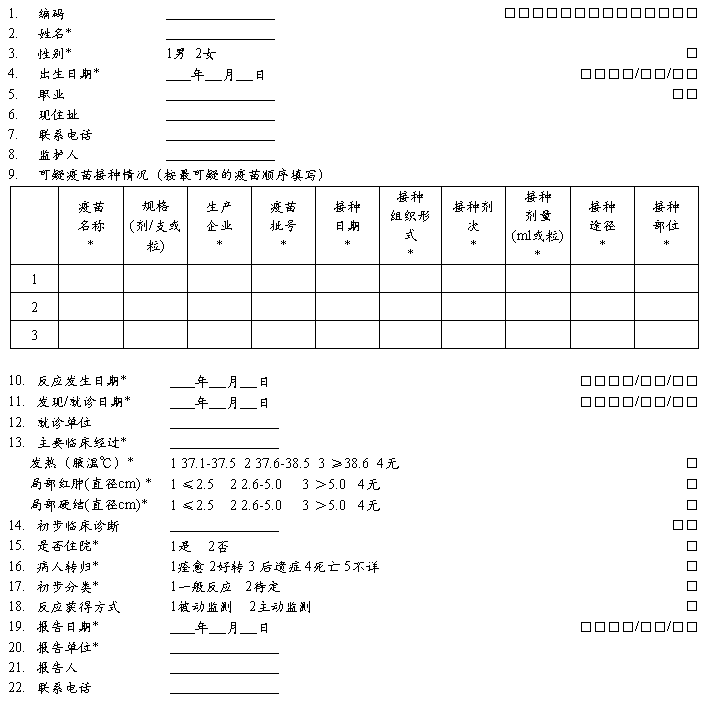
说明:* 为关键项目。
附表2
群体性疑似预防接种异常反应登记表
群体性疑似预防接种异常反应编码: 县国标码□□□□□□-首例发生年份□□□□-编号□□ 发生地区:
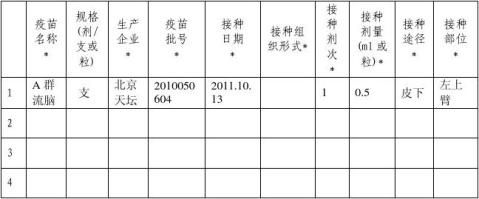
疫苗名称*: 生产企业*: 规格(剂/支或粒) : 有无批签发合格证: 接种单位:
接种人数*: 反应发生人数*: 报告单位*: 报告人: 联系电话:

说明:* 为关键项目。
附表3
疑似预防接种异常反应个案调查表
一、基本情况

二、既往史

三、可疑疫苗情况(按最可疑的疫苗顺序填写)

七、临床情况

八、其他有关情况

九、报告及调查情况

十、结论

说明:* 为关键项目。
附表4
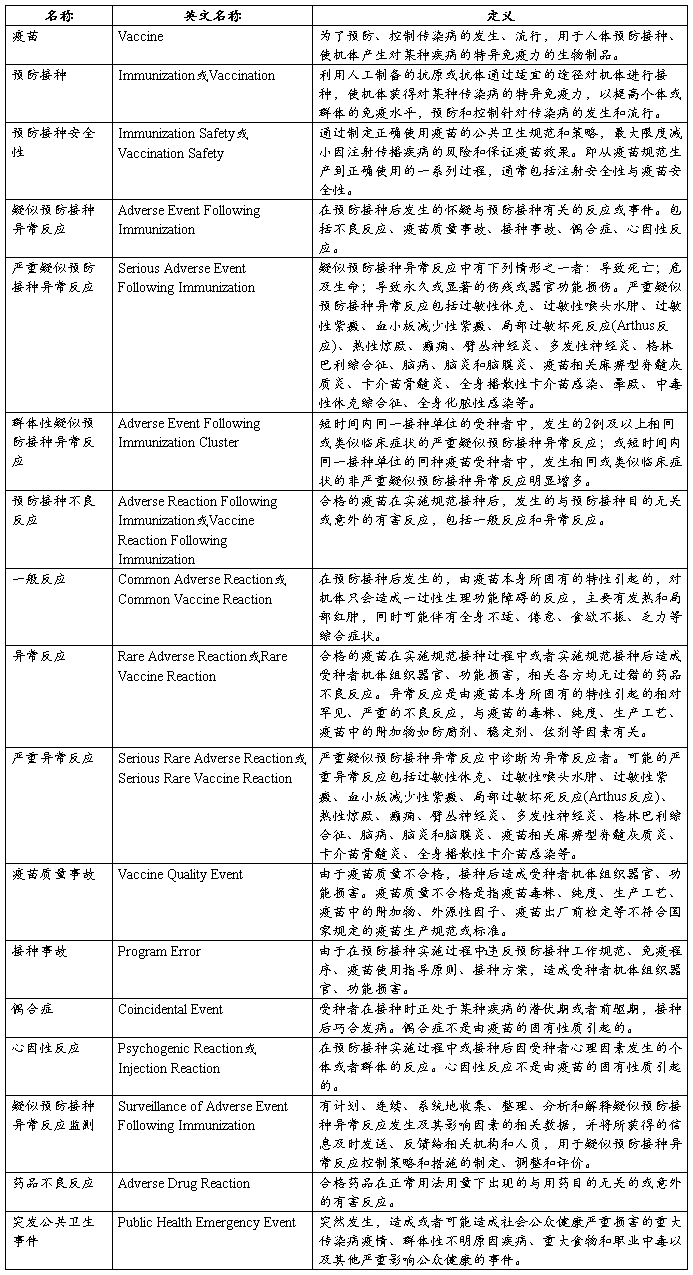
名词解释