实验十 全回流精馏塔总板效率的测定
一、实验目的
1、了解精馏装置的基本流程及筛板精馏塔的结构,熟悉精馏操作方法;
2、测定全回流条件下总板效率(或单板效率)。
二、基本原理
精馏塔是分离均相混合液的重要设备,衡量板式精馏塔分离性能,一般用总板效率表示:
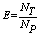 (式10-1)
(式10-1)
式中:E——总板效率;
NT——理论板层数;
NP——实际板层数。
 理论板层数NT的求法可用M-T图解法。本实验是使用乙醇-水二元物系在全回流条件下操作,只需测定塔顶馏出液组成χD和釜液组成χW,即可用图解法求得NT,实际板层数NP为已知,所以利用式(1)可求得塔效率E。
理论板层数NT的求法可用M-T图解法。本实验是使用乙醇-水二元物系在全回流条件下操作,只需测定塔顶馏出液组成χD和釜液组成χW,即可用图解法求得NT,实际板层数NP为已知,所以利用式(1)可求得塔效率E。
若相邻两块塔板设有液体取样口,则可通过测定液相组成χn-1和χn求得第n块板在全回流下的单板效率EmL。
 (式10-2)
(式10-2)
而全回流时,yn = χn-1
式中:χn-1——离开上块板的液相中易挥发组分摩尔分率;
χn——离开下块板的液相中易挥发组分摩尔分率;
yn——离开下块板的气相中易挥发组分摩尔分率;
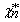 ——与yn与平衡的液相组成摩尔分率,以χn-1作为气相组成在平衡线上查得。
——与yn与平衡的液相组成摩尔分率,以χn-1作为气相组成在平衡线上查得。
三、装置与流程
实验装置为一个小型筛板塔,如图10-1所示。
原料液在蒸馏釜2中被加热汽化进入塔体4,与回流液在塔板上进行热、质交换后进入塔顶冷凝器5,冷凝为饱和液体后,又全部回流到塔内,由取样口7取样分析馏出液组成,从塔釜取样分析液组成。
四、操作步骤
1、熟悉精馏装置的流程和结构,以及所需的控制仪表盘和布置情况,检查蒸馏釜中料液量是否适当,釜内液面高度控制在液面计2/3左右;
2、检查电源并接通电源,加热釜液。用调压器调节加热功率(电流以3~4A为宜),注意观察塔顶和塔釜的温度变化,塔顶第一块板上开始有回流时,打开冷却水,冷却水用量以能将蒸汽全凝为宜;
3、打开塔顶放空阀8排出不凝性气体,塔板上鼓泡正常、温度稳定即表明操作稳定,可开始取样;
4、取样前先用少量试样冲锥形瓶。取样后将锥形瓶口用插有温度计的塞子塞严,用流水将样品间接冷却至20℃,再用天平测量样品的相对密度,一般取样2次(塔顶、塔釜各一次);
5、以上步骤经教师检查无误后,加大电流至5A左右,观察塔内的液泛现象,然后将电流缓慢减小,观察漏液现象,最后将电流减小至零,切断电源,待塔内无回流时关闭冷却水,清理现场。
若精馏塔塔板上设有液体取样品,则可在操作稳定后,在相邻两板取样分析液体组成χn和χn-1,再按式(2)计算单板效率。
五、实验记录与数据处理
数据记录如表10-1所示。
表10-1 实验数据表
塔内径 mm 板间距 mm 实际板数 块
数据处理:根据酒精计测定的体积分率计算成摩尔分率,其余见本节基本原理部分。
六、实验报告
1、将塔顶和塔釜的温度组成等原始数据用表格形式列出;
2、利用图解法求理论板数及全塔效率。
七、思考题
1、什么是全回流,全回流时的操作特征是什么?如何测定全回流时的总板效率?
2、如何判断塔的操作已达到稳定?影响精馏操作稳定的因素有哪些?
3、影响板式塔效率的因素有哪些?
4、进料量对塔板层数有无影响?为什么?
5、板式塔有哪些不正常操作现象?如何调节处理?
实验十一 部分回流精馏塔塔板数的确定
一、实验目的
1、熟悉精馏塔结构和精馏流程,掌握精馏操作方法;
2、掌握精馏塔全塔效率的测定方法。
二、基本原理
1、精馏塔操作要领
(1)维持好物料平衡,即:
F = D + W FxF = DxD + Wxw (式11-1)
或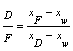
 (式11-2)
(式11-2)
式中:F、D、W——分别为进料、馏出液、釜残液的流率,kmol/s;
xF、xD、xW——分别为进料、馏出液、釜残液中轻组分的组成摩尔分率;
D/F、W/F——分别为塔顶、塔底的采出率。
若物料不平衡,当F>D+W时,将导致塔釜、降液管和塔板液面升高,压降增大,雾沫夹带增加,严重时甚至会淹塔;当F<D+W时,将导致塔釜,降液管和塔板液面降低,漏液量增加,塔板上气液分布不均匀,严重时甚至会干塔。
在规定的精馏条件下,若塔顶采出率D/F超出正常值,即使精馏塔具有足够的分离能力,从塔顶也不能得到规定的合格产品;若塔底采出率W/F超出正常值,则釜残液的组成将增加,既不能达到分离要求,也增加了轻组分的损失。
(2)控制好回流比。精馏塔应采用适宜的回流比操作,在塔板数固定的情况下,当满足DxD≤FxF且塔处于正常流体力学状态时,加大回流比能提高塔顶馏出液组成XD,但能耗也随之增加。加大回流比的措施,一是减少馏出液量,二是加大釜的加热速率和塔顶的冷凝速率,但塔釜的加热速率和塔顶的冷凝速率在装置中是有限度的。因此在操作过程中,调节回流比时要将两者协调好,尤其是后者涉及维持热量平衡。
2、精馏全效率测定
参见实验十
三、装置与流程
精馏实验装置如图11-1所示。
料液由料液槽10经转子流量计9、阀13进入精馏塔,蒸汽由蒸馏釜2上升至塔体5,上升过程中与回流液进行热量、质量传递,再进入冷凝器6、回流分配器12,其中一部分冷凝液作为产品进入贮槽,另一部分回流至塔内。与此同时,釜内液体的一部分经阀14流出。
四、操作步骤
1、正常操作步骤
(1)熟悉流程和主要控制点。
 (2)在料液槽10内配制5%的酒精水溶液,其液位应高于供料泵,启动输液泵将料液注入蒸馏釜,釜内液位应在液位计两标记线之间。
(2)在料液槽10内配制5%的酒精水溶液,其液位应高于供料泵,启动输液泵将料液注入蒸馏釜,釜内液位应在液位计两标记线之间。
(3)接通电源加热釜液,为加快预热速度,可先开两组加热器,将电压调至220V,开启塔顶冷凝器的冷却水进口阀。
密切注视加热釜的温度和表盘上的温度和压力,当压力不断上升时,应适当开启塔顶排气阀,及时将塔内不凝性气体排出。操作压力应稳定在0.026~0.030Mpa(表压)。
(4)待加热釜内釜液沸腾后,进行全回流操作约20~30分钟。此时,灵敏板温度约为80~81℃,塔顶温度约为79~80℃,塔板鼓泡正常。如果温度过高,可通过自耦变压器调低加热电压或断开一组手动加热器。待操作稳定后,测定全回流时的全塔效率。
(5)关小回流阀,开启馏出液产品出口阀,进行部分回流操作,注意要预先选择好回流比和一个加料口(不能同时选用两上加料口),待有产品后,再加以适当调节。
(6)在料液槽内配制约20%(体积)的料液,启动进料泵进料(4~6l/h),并控制塔釜液位在正常标记范围内,如液位过低,可加大进料,如液位过高,可开大塔底出口阀14,随时注意塔内压力、灵敏板温度等操作参数的变化并及时加以调节。
(7)待操作稳定后,同时对馏出液、釜液进行取样(取样量均为140~150ml,以保证液体相对密度计能正常测量),并按表11-1中的内容做好记录。
继续调节有关参数直至馏出液浓度高于75%(体积百分率),釜残液酒精浓度低于3%,操作才算达到要求。
(8)实验完毕后,关闭总电源,打开玻璃观察罩考克和回流管路上的考克,馏出液排尽。
(9)清理实验现场。
2、操作过程中的不正常现象,其原因分析和处理办法
(1)塔顶温度高于正常值,塔釜温度低于正常值,馏出液和釜液组成不合要求,这是因为塔板分离能力不够,应加大回流比。
(2)塔釜温度变化不大,塔顶温度逐渐升高,馏出液组成降低。这是因为DxD>FxF-Wxw,又可细分为:①D/F> ,即塔顶采出率过大;②XF下降过多。处理办法是:对①应适当使D下降,W上升,待塔顶温度逐步降至正常时,再调节各操作参数使精馏过程处于DxD = FxF-Wxw下进行;对②则应使进料板下移或使R上升。
,即塔顶采出率过大;②XF下降过多。处理办法是:对①应适当使D下降,W上升,待塔顶温度逐步降至正常时,再调节各操作参数使精馏过程处于DxD = FxF-Wxw下进行;对②则应使进料板下移或使R上升。
(3)塔顶温度变化不大,塔釜温度逐渐下降,釜液组成升高。这是因为DxD<FxF-Wxw,又可细分为:①D/F<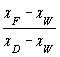 ;②XF上升太快。处理方法是:对①与现象(2)中的①相反,对②可使进料板上移或加大塔釜电热器功率,并使D上升,W下降。
;②XF上升太快。处理方法是:对①与现象(2)中的①相反,对②可使进料板上移或加大塔釜电热器功率,并使D上升,W下降。
(4)塔板漏液,塔釜压力降低,塔板上液面下降或消失。这是因为上升蒸汽量不够,应适当加大塔釜电热器功率。
(5)液沫夹带严重,馏出液和釜残液不符合要求,塔釜压力偏高。这是因为:上升蒸汽量和液体回液量过大,应减少塔釜电加热器功率和回流量。
(6)液体逐板下降不畅,塔釜压力陡升,造成淹塔。这是因为溢流液泛,夹带液泛,应减少回流量和上升蒸汽量。
(7)塔釜压力逐渐升高,塔顶冷凝效果降低。这是因为塔内不凝性气体积聚,应排放不凝气。
五、实验记录与数据处理
数据记录如表11-1所示。
表11-1 实验数据表
塔内径: mm 实际塔板数: 块
回流比R: 塔釜压力P: Mpa

六、实验报告
按实验十的基本原理,用图解法确定理论板数,并计算全塔效率。
七、思考题
1、是否精馏塔越高,产量越大?
2、将精馏塔加高能否得到无水酒精?
3、影响精馏塔操作稳定的因素有哪些?结合本实验说明。
4、操作中加大回流比应如何进行?有何利弊?
5、精馏塔在操作过程中,由于塔顶采出率太大而造成产品不合格时,要恢复正常的最快最有效的办法是什么?
第二篇:实验十 反应精馏
实验十 反应精馏实验
反应精馏是精馏技术中的一个特殊领域。在操作过程中,化学反应与分离同时进行,故能显著提高总体转化率,降低能耗。此法在酯化、醚化、酯交换、水解等化工生产中得到应用,而且越来越显示其优越性。
一、实验目的:
1. 了解反应精馏是既服从质量作用定律又服从相平衡规律的复杂过程。
2. 掌握反应精馏的操作。
3. 能进行全塔物料衡算和塔操作的过程分析。
4. 了解反应精馏与常规精馏的区别。
5. 学会分析塔内物料组成。
二、实验原理:
反应精馏过程不同于一般精馏,它既有精馏的物理相变之传递现象,又有物质变性的化学反应现象。两者同时存在,相互影响,使过程更加复杂。因此.反应精馏对下列两种情况特别适用:
(1)可逆平衡反应。一般情况下,反应受平衡影响,转化率只能维持在平衡转化的水平;但是,若生成物中有低沸点或高沸点物质存在,则精馏过程可使其连续地从系统中排出,结果超过平衡转化率,大大提高了效率。
(2)异构体混合物分离。通常因它们的沸点接近,靠精馏方法不易分离提纯,若异构体中某组分能发生化学反应并能生成沸点不同的物质,这时可在过程中得以分离。
对醇酸酯化反应来说,适于第一种情况。但该反应若无催化剂存在,单独采用反应精馏操作也达不到高效分离的目的,这是因为反应速度非常缓馒,故一般都用催化反应方式。酸是有效的催化剂,常用硫酸。反应随酸浓度增高而加快,浓度在0.2一1.0%(质量分数)。此外,还可用离子交换树脂,重金属盐类和丝光沸石分子筛等固体催化剂。反应精馏的催化剂用硫酸,是由于其催化作用不受塔内温度限制,在全塔内都能进行催化反应,而应用固体催化剂则由于存在一个最适宜的温度,精馏塔本身难以达到此条件,故很难实现最佳化操作。
本实验是以醋酸和乙醇为原料,在酸催化剂作用下生成醋酸乙酯的可逆反应。
反应的化学方程式为:
CH3COOH + C2H5OH → CH3COOC2H5 + H2O
 实验的进料有两种方式:一是直接从塔釜进料;另一种是在塔的某处进料。前者有间歇和连续式操作;后者只有连续式。本实验以后一种方式进料进行说明,即在塔上部某处加带有酸催化剂的醋酸,塔下部某处加乙醇。釜沸腾状态下塔内轻组分逐渐向上移动,重组分向下移动。具体地说,醋酸从上段向下段移动,与向塔上段移动的乙醇接触,在不同填料高度上均发生反应,生成酯和水。塔内此时有4组元。除醋酸外,其它三个组分形成三元或二元共沸物。水—酯,水—醇共沸物沸点较低,醇和酯能不断地从塔顶排出。若控制反应原料比例,可使某组分全部转化。因此,可认为反应精馏的分离塔也是反应器。全过程可用物料衡算式和热量衡算式描述。
实验的进料有两种方式:一是直接从塔釜进料;另一种是在塔的某处进料。前者有间歇和连续式操作;后者只有连续式。本实验以后一种方式进料进行说明,即在塔上部某处加带有酸催化剂的醋酸,塔下部某处加乙醇。釜沸腾状态下塔内轻组分逐渐向上移动,重组分向下移动。具体地说,醋酸从上段向下段移动,与向塔上段移动的乙醇接触,在不同填料高度上均发生反应,生成酯和水。塔内此时有4组元。除醋酸外,其它三个组分形成三元或二元共沸物。水—酯,水—醇共沸物沸点较低,醇和酯能不断地从塔顶排出。若控制反应原料比例,可使某组分全部转化。因此,可认为反应精馏的分离塔也是反应器。全过程可用物料衡算式和热量衡算式描述。
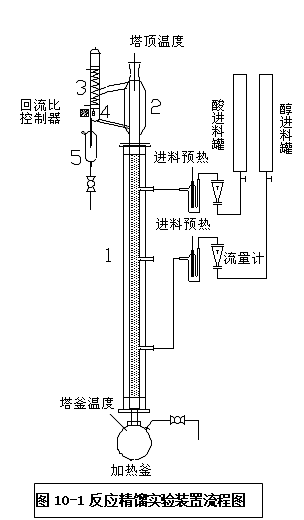
三、实验装置:
1、填料精馏塔 2、塔头3、塔顶冷凝器 4、回流比控制器 5、塔顶液接收灌
反应精馏塔用玻璃制成。直径29mm,塔高1400 mm,塔内填装φ3x 3 mm不锈钢θ环型填料;塔釜为玻璃双循环自动出料塔釜,容积250m1(250g),塔外壁镀有金属保温膜,通电使塔身加热保温。塔釜用500W电加热棒进行加热,采用电压调节器控制釜温。塔顶冷凝液体的回流采用摆动式回流比控制器操作。此控制系统由塔头上摆锤、电磁铁线圈、回流比计数器等仪表组成。进料采用高位槽经转子流量计进入塔内。
四、实验步骤:
操作前在釜内加入250克(醋酸、乙醇各125克)接近稳定操作组成的釜液(稳定液),并分析其组成。检查进料系统各管线是否连接正常。将釜液(稳定液)加入釜内。分别将醋酸、乙醇各150克注入原料量管内(醋酸内含0.3%硫酸),
打开加热开关,注意不要使电流过大,以免设备突然受热而损坏。待釜液沸腾,开启塔身保温电路,调节保温电流(注意:不能过大),开塔头冷却水。从塔头有液体出现,全回流10—15分钟后开始进料,打开进料流量计阀门,向塔内加料。酸醇分子比定在1:1.3,醋酸进料速度约为4.5m1/min,乙醇进料速度约为5.85m1/min。进料后仔细观察塔底和塔顶温度。一般可把回流比给定在3:1。调节塔顶与塔釜出料速度,使处于平衡状态。记录所有数据,稳定操作20分钟,用微量注射器在塔身取样口(由下至上230mm、670mm、1100mm)内取液样,利用气相色谱仪测定组分浓度。
如果时间允许,可改变回流比或改变加料分子比,重复操作,取样分析,并进行对比。
醋酸进料结束后关闭加料,停止加热,让持液全部流至塔釜,停止通冷却水,实验完成。分别称量釜液(包括馏出物)、塔顶产品重量,取样分析组分。
Wi%=fiAi%/∑fiAi%
五、实验数据处理:
自行设计实验数据记录表格,进行醋酸和乙醇的全塔物料衡算,计算塔内浓度分布、反应收率、转化率等。
转化率=[(醋酸加料量+稳定液醋酸量)—(釜残液+馏出液醋酸量)]/(醋酸加料量+稳定液醋酸量)
反应收率=(塔顶采出液+塔釜液+馏出液乙酸乙酯总量-稳定液乙酸乙酯量)/[(醋酸加料量+稳定液醋酸量-(釜残液+馏出液醋酸量))*(85/60)]

计算实例:
1、样品的组分计算以采样位置230mm处水的各组分质量分数计算为例:
水:

乙醇:
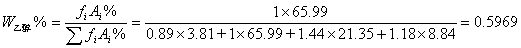
乙酸乙酯:

乙酸:

2、转化率=[(醋酸加料量+稳定液醋酸量)—(釜残液+馏出液醋酸量)]/(醋酸加料量+稳定液醋酸量)

=((150.74+250.1*0.1037)-(397.6*0.1037))/(150.74+250.1*0.1037)=0.7666
3、反应收率=(塔顶采出液+塔釜液+馏出液乙酸乙酯总量-稳定液乙酸乙酯量)/[(醋酸加料量+稳定液醋酸量-(釜残液+馏出液醋酸量))*(85/60)]
=(71.1*0.6115+397.6*0.2144-250.1*0.2144)/((150.74+250.1*0.1037-397.6*0.1037)*85/60)
=0.3914
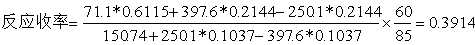
实验结果讨论:
物料衡算
塔顶产品中,水:71.1×0.0471=3.34g
乙醇:71.1×0.3507=24.93g
乙酸乙酯:71.1×0.6115=43.48g
塔釜残液+馏出液中,水:397.6×0.1093=43.46g
乙醇:397.6×0.5726=227.67g
乙酸乙酯:397.6×0.2144=85.25g
乙酸:397.6×0.1037=41.23g
稳定液中, 水:250.1×0.1093=27.34g
乙醇:250.1×0.5726=143.2g
乙酸乙酯:250.1×0.2144=53.62g
乙酸:250.1×0.1037=25.94g
反应共生成乙酸乙酯43.48+85.25-53.62=75.11g,
反应生成乙酸乙酯消耗乙酸=75.11*60/85=53.02g,
反应实际消耗乙酸为:150.74+25.94-41.23=135.45g,两者差值较大,测量结果误差较大。
六、思考题
怎样提高酯化收率?
不同回流比对产物分布有何影响?
加料摩尔比应保持多少为最佳?
对本实验的改进建议。
