《实验活动8 粗盐中难溶性杂质的去除》重难点分析
石家庄第二外国语学校 姜天雷
一、教材分析:
本课程利用之前学习的天然水的净化中,过滤的方法来具体操作,结合有关溶液的知识,向学生介绍分离混合物的一般方法,培养学生实验操作能力及对实验过程和实验结果的表达能力。
本节课的教学重点是:(一)掌握粗盐提纯的一般步骤(二)具备一定的实验分析评价能力。
二、重难点分析
(一)掌握粗盐提纯的一般步骤。
1.突破建议:粗盐提纯的一般步骤是综合了之前学过的称量、溶解、过滤三个基本操作,结合学生对蒸发操作的学习,将其四步操作结合形成完整的实验。
2.突破样例:
【师】出示:一瓶食盐,一瓶粗盐,一瓶食盐的水溶液,一瓶粗盐的水溶液
【生】观察:①固体食盐与粗盐的外观差异;②食盐与粗盐的水溶液的外观差异。
【设计意图】给学生以具体、丰富的感性认识,有利于学生兴趣的保持。
【师】提出问题,如何除去粗盐中难溶性杂质,将粗盐转化为精盐?探究过程第一步:分组讨论,设计实验方案
【生】交流讨论
【设计意图】创设真实问题情景,激发学生掌握知识并积极解决问题的意识和能力。

【师】利用溶解度的概念分析“为什么用10ml水对3克粗盐进行溶解,而不是100ml水去溶解”。
【生】和氯化钠在常温下的溶解度有关
【设计意图】加深学生对溶解度实际应用的理解
【师】实验过程中提醒学生过滤操作的注意事项“一贴、二低、三靠”。
【生】完成溶解、过滤的实验操作。

【设计意图】提高学生的实验技能
【师】提出问题:如何将过滤之后食盐水转变为固体食盐:
【生】根据海水晒盐原理,可以提出蒸发操作

【师】出示温馨提示
1.蒸发过程中要用玻璃棒不断搅拌
2.在加热至有较多晶体析出时,停止加热
3.热的蒸发皿要放在石棉网上冷却,以免烫坏实验台,取用蒸发皿时使用坩埚钳。
思考:1.为什么用玻璃棒?玻璃棒的作用是什么?
2.为什么有较多晶体析出时就停止加热?

【生】学生分组实验, 反思交流,解决实验中问题
【设计意图】1.完善实验步骤 2.理解粗盐提纯原理
【师】完成实验报告,根据实验过程,总结分离混合物的一般思路
【生】小组交流后总结
【设计意图】培养学生总结、概括能力。
(二)具备一定的实验分析评价能力。
1.突破建议:本实验最终各组的产率往往是不一样的,引导学生通过误差分析,培养其对于实验的分析评价能力
2.突破样例:
【师】同学们,经过计算你们得到的产率是多少呢?
【生】汇报展示结果
【师】由于实验误差,我们的结果经常会出现不一致的现象。这个实验的误差是怎么产生的呢?小组讨论解决。
【生】A.食盐还没有全部溶解就过滤了; B.蒸发时,食盐溶液剧烈飞溅; C.蒸发后,所得到的精盐很潮湿; D.蒸发皿里的食盐没有全部转移到纸上。E.称量时,数据不准确
【师】这些误差对于实验数据的影响是偏大还是偏小呢?
【生】A.食盐还没有全部溶解就过滤了──偏小; B.蒸发时,食盐溶液剧烈飞溅──偏小; C.蒸发后,所得到的精盐很潮湿──偏大; D.蒸发皿里的食盐没有全部转移到纸上──偏小E.称量时,数据不准确──偏大或偏小
《实验活动8 粗盐中难溶性杂质的去除》教材习题解答
石家庄市第20中学 贾 薇
【教材P88问题与交流】
1.制取粗盐时,晒盐和煮盐的目的都是通过蒸发盐溶液中的水分使之浓缩。想一想:能否采用降低溶液温度的方法来达到同一目的?(提示:从氯化钠的溶解度曲线考虑。)
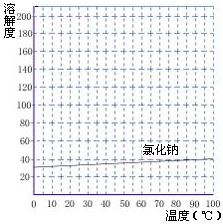
分析:从上图氯化钠溶解度曲线图中可知,氯化钠溶解度受温度影响变化不大,其高温饱和溶液降温后,析出氯化钠晶体的量少,大部分还溶解在水中。另一方面,降温后氯化钠的饱和溶液的浓度小于其高温下饱和溶液的浓度,降温后溶液浓度减小。所以,不能通过降低溶液温度的方法来达到使其溶液浓缩的目的。
2.本实验中采用的方法利用了氯化钠的哪些性质?考虑到粗盐的来源,你判断这样提纯的盐是否为纯净物,并设计实验验证你的判断。
分析:利用了氯化钠易溶于水,其熔、沸点较高的性质。粗盐经溶解、过滤、蒸发后,依然含有可溶性杂质,如氯化钙、氯化镁、硫酸钠等。
将溶解、过滤、蒸发后得到的盐溶于水配成溶液,取少量的溶液于试管中,滴加氢氧化钠溶液(或碳酸钠溶液、氯化钡溶液),有白色沉淀生成,则证明通过上述步骤提纯的盐不是纯净物。
第二篇:实验活动8: 粗盐中难溶性杂质的去除学生实验报告单
顺平县腰山镇中学学生化学实验报告单
实验题目: 实验活动8:粗盐中难溶性杂质的去除
班级: 日期: 指导教师:
第 组 姓名: 同 组 人:
【实验目的】
1、体验固体混合物初步提纯的实验过程。
2、学习蒸发操作技能,巩固溶解、过滤操作技能。
【实验用品】
烧杯、玻璃棒、蒸发皿、坩埚钳、酒精灯、漏斗、药匙、量筒(10mL)、铁架台(带铁圈)、托盘天平、滤纸、火柴。
【实验步骤】
 1、溶解:用托盘天平称取粗盐5.0g粗盐,用药匙将该粗盐逐渐加入盛有10mL水的烧杯里,边加边用玻璃棒搅拌(玻璃棒作用: ),一直加到粗盐不再溶解为止。观察所得食盐水是否浑浊(现象: )。
1、溶解:用托盘天平称取粗盐5.0g粗盐,用药匙将该粗盐逐渐加入盛有10mL水的烧杯里,边加边用玻璃棒搅拌(玻璃棒作用: ),一直加到粗盐不再溶解为止。观察所得食盐水是否浑浊(现象: )。
称量剩下的粗盐,计算10mL水中约溶解了多少克粗盐。

2、过滤:过滤食盐水。仔细观察滤纸上剩余物及滤液的颜色
(现象: )。
3、蒸发:把所得澄清滤液倒入蒸发皿,用酒精灯加热。 图11-13过滤食盐水
 在加热过程中,用玻璃棒不断搅拌(作用: ),
在加热过程中,用玻璃棒不断搅拌(作用: ),
当蒸发皿中出现较多固体时,停止加热。利用蒸发皿的余热使滤液蒸干。
观察蒸发皿中食盐的外观(现象: )。
4、计算产率。用玻璃棒把固体转移到纸上,称量后,回收到教师指定
的容器中。将提纯后的氯化钠与粗盐作比较,并计算精盐的产率。

图11-14蒸发食盐水
【问题交流】
1、制取粗盐时,晒盐和煮盐的目的都是通过蒸发盐溶液中的水分使之浓缩。想一想:能否采用降低溶液温度的方法来达到同一目的?(提示:从氯化钠的溶解度曲线考虑)。
2、本实验中采用的方法利用了氯化钠的哪些性质?考虑到粗盐的来源,你判断这样提纯的盐是否为纯净物,并设计实验验证你的判断。
