饮料中的咖啡因的高效液相色谱分析 院(系) 生化系 年级 10化工
姓名 学号
2课程名称 基础化学实验报告 实验日期 20##年12月27日
实验地点 3# 5楼 指导教师 夏湘 黄玉老师
一.实验目的
(1)熟悉高效液相色谱仪的结构,理解反相HPLC的原理和应用;
(2)掌握外标定量法。
二.实验原理
咖啡因又称咖啡碱,属黄嘌呤衍生物,化学名称为1,3,7-三甲基黄嘌呤,是从茶叶或咖啡中提取的一种生物碱。它能兴奋大脑皮层,使人精神亢奋。咖啡因在咖啡中的含量约为1.2%-1.8%,在茶叶中约为2.0-4.7%。可乐饮料、止痛药等均含咖啡因。咖啡因的分子式为C8H10O2N4,其化学结构式如下图:
在化学键合相色谱法中,若采用的流动相的极性大于固定相的极性,则称为反相化学键合相色谱法。该方法是目前应用最为广泛的色谱方法。本实验采用C18键合相色谱柱分离饮料中的咖啡因,用紫外检测器进行检测,以咖啡因标准系列溶液的色谱峰面积对其浓度作标准曲线,再根据试样中咖啡因的峰面积,由标准曲线计算出试样中咖啡因的浓度。
三.实验用品
仪器:高效液相色谱仪、恒流泵、超声波清洗仪、紫外光检测器等。
试剂:甲醇(分析纯)、咖啡因(分析纯)、二次蒸馏水
咖啡因标准溶液的配制:
(1)标准储备液 配制含咖啡因1000ug/mL的甲醇溶液,备用。
(2)标准系列溶液 用上述备用液配制含咖啡因20ug/mL、40ug/mL、80ug/mL、160ug/mL、320ug/mL的甲醇溶液,备用。
试样 市售的可口可乐和百事可乐。
四.实验条件
(1)色谱柱 长150mm,内径4.6mm,装填C-18烷基键合物,颗粒度10μm的固定相
(2)流动相 甲醇-水(60:40),流量0.6m/mim
(3)紫外光度检测器 测定波长254mm,灵敏度0.08
(4)进样量 10μL
五.实验步骤
(1)将配制好的流动相置于超声波清洗仪上脱气15min;
(2)根据实验条件,将仪器按照仪器的操作步骤调节至进样状态,待仪器液路和电路系统达到平衡时,色谱工作六站或记录仪的基线呈平直,即可进样;
(3)依次分别吸取10μL的可乐试样进样,并记录各色谱仪的数据;
(4)分别将约20mL的可口可乐和百事可乐试样置于25mL的容量瓶中,用超声波清洗仪脱气15min;
(5)依次分别吸取10μL的可乐试样进样,记录各色谱仪的数据;
(6)试验结束后,按要求关好仪器。
六.实验数据处理
(1)记录实验条件
(2)处理色谱数据,将系列对照品溶液与可乐试样的咖啡因色谱峰保留时间及峰面积列于下表中:

(3)绘制咖啡因色谱峰面积-对照品溶液浓度的回归曲线,并计算回归方程和相关系数。
将标样的数据利用EXCEL软件绘图,并计算回归方程,如下:

(4)根据可乐试样中咖啡因色谱峰面积值,计算可乐试样中的咖啡因浓度。

七.思考题
(1)用标准曲线法定量有什么优缺点?
答:标准曲线法的优点是:绘制好标准工作曲线后测定工作就变得相当简单,可直接从标准工作曲线上读出含量,因此特别适合于大量样品的分析。
标准曲线法的缺点是:每次样品分析的色谱条件(检测器的响应性能,柱温,流动相流速及组成,进样量,柱效等)很难完全相同,因此容易出现较大误差。此外,标准工作曲线绘制时,一般使用欲测组分的标准样品(或已知准确含量的样品),而实际样品的组成却千差万别,因此必将给测量带来一定的误差。
(2)根据咖啡因的结构特点,咖啡因还可采用其他类型的色谱方法吗?
(3)采用咖啡因浓度与色谱峰高作回归曲线,能给出准确的测试结果吗?与本实验的峰面积-浓度回归曲线相比,哪一种方法更好一些?为什么?
第二篇:高效液相色谱法测定饮料中的咖啡因(含问题分析)
华南师范大学实验报告
专 业: 材料化学 年 级:20##级
课程名字:近代材料分析测试技术 实验项目:高效液相色谱法
实验类型: 验证 实验时间:20##年3月25日
实验二 高效液相色谱法测定饮料中的咖啡因
一、目的要求
1、学习高效液相色谱仪的操作。
2、了解高效液相色谱法测定咖啡因的基本原理。
3、掌握高效液相色谱法进行定性及定量分析的基本方法。
二、基本原理
咖啡因又称咖啡碱,是由茶叶或咖啡中提取而得的一种生物碱,它属黄嘌呤衍生物,化学名称为1,3,7-三甲基黄嘌呤。咖啡因能兴奋大脑皮层,使人精神兴奋。咖啡中含咖啡因约为1.2~1.8%,茶叶中约含2.0~4.7%。可乐饮料、APC药片等中均含咖啡因。其分子式为C8H10O2N4,结构式为:

定量测定咖啡因的传统分析方法是采用萃取分光光度法。用反相高效液相色谱法将饮料中的咖啡因与其它组分(如:单宁酸、咖啡酸、蔗糖等)分离后,将已配制的浓度不同的咖啡因标准溶液进入色谱系统。如流动相流速和泵的压力在整个实验过程中是恒定的,测定它们在色谱图上的保留时间tR和峰面积A后,可直接用tR定性,用峰面积A作为定量测定的参数,采用工作曲线法(即外标法)测定饮料中的咖啡因含量。
三、仪器和试剂
1、Agilent 1100高效液相色谱仪。
2、色谱柱:Kromasil C18,5µ 150×4.6mm。
3、流动相:30%甲醇(色谱纯)+70%高纯水;流动相进入色谱系统前,用超声波发生器脱气10min。
4、 咖啡因标准贮备溶液:将咖啡因在110℃下烘干1h。准确称取0.1000g咖啡因,用二次蒸馏水溶解,定量转移至100mL容量瓶中,并稀释至刻度。标样浓度1000μg·mL-1。
5、测饮料试液:可乐,茶叶,速溶咖啡。
6、20μL平头微量注射器。
四、实验内容
1、 标准贮备液配制质量浓度分别为20、40、60、80μg·mL-1的标准系列溶液。(1mL,2mL,3mL、4mL稀释为50mL)
2、 谱仪器条件:
泵的流速:1.0mL/min;检测波长:275nm;进样量:10μL;柱温:室温。
3、 仪器基线稳定后,进咖啡因标准样,浓度由低到高。
4、 品处理如下:(1)将约25mL可口可乐置于一100mL洁净、干燥的烧杯中,剧烈搅拌30min或用超声波脱气5min,以赶尽可乐中二氧化碳。(2)准确称取0.04g速溶咖啡,用90℃蒸馏水溶解,冷却后待用。(3)准确称取0.04g茶叶,用20mL蒸馏水煮沸10min,冷却后,将上层清液,并按此步骤再重复一次。将上述三种样品分别转移至50mL容量瓶中,并定容至刻度。
5、 上述三份样品溶液分别进行干过滤(即用干漏斗、干滤纸过滤),弃去前过滤液,取后面的过滤液,备用。
6、 别取5mL可乐、咖啡饮料和茶叶水用0.45µm的过滤膜过滤后,注入2mL样品瓶中备用。
7、 “Agilent 1100高效液相色谱仪操作规程”分析饮料试液。
五、结果处理
1. 测定每一个标准样的保留时间(进样标记至色谱峰顶尖的时间)。
2. 确定未知样中咖啡因的出峰时间。
3. 求取样品中咖啡因的浓度。
记得实验结果如下:
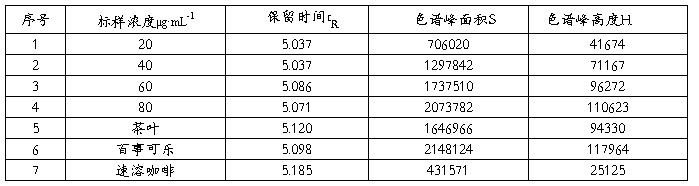
将标样的数据利用EXCEL软件绘图,并计算回归方程,如下:
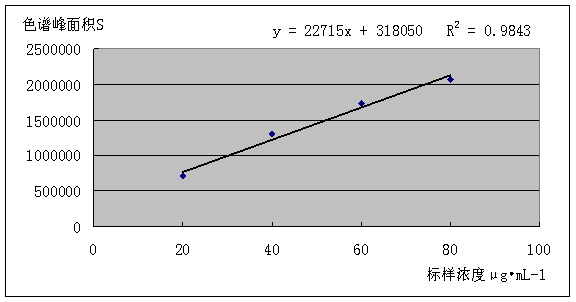 将茶叶、百事可乐、速溶咖啡测试所得的峰面积代入回归方程计算浓度:
将茶叶、百事可乐、速溶咖啡测试所得的峰面积代入回归方程计算浓度:

六、注意事项
1、不同的可乐、茶叶、咖啡中咖啡因含量不大相同,称取的样品量可酌量增减。
2、若样品和标准溶液需保存,应置于冰箱中。
3、为获得良好结果,标准和样品的进样量要严格保持一致。
七、思考题
1、用标准曲线法定量的优缺点是什么?
答:标准曲线法的优点是:绘制好标准工作曲线后测定工作就变得相当简单,可直接从标准工作曲线上读出含量,因此特别适合于大量样品的分析。
标准曲线法的缺点是:每次样品分析的色谱条件(检测器的响应性能,柱温,流动相流速及组成,进样量,柱效等)很难完全相同,因此容易出现较大误差。此外,标准工作曲线绘制时,一般使用欲测组分的标准样品(或已知准确含量的样品),而实际样品的组成却千差万别,因此必将给测量带来一定的误差。
2、根据结构式,咖啡因能用离子交换色谱法分析吗?为什么?
答:不行。因为离子交换色谱以离子交换树脂作为固定相,树脂上具有固定离子基团及可交换的离子基团。当流动相带着组分电离生成的离子通过固定相时,组分离子与树脂上可交换的离子基团进行可逆变换。平衡常数K值越大,表示组分的离子与离子交换树脂的相互作用越强。由于不同的物质在溶剂中离解后,对离子交换中心具有不同的亲合力,因此具有不同的平衡常数。亲合力大的,在柱中的停留时间长,具有高的保留值。依据咖啡因的结构式1,3,7-三甲基黄嘌呤或3,7-二氢-1,3,7三甲基-1H-嘌呤-2,6-二酮,其解离常数很小,不符合离子交换色谱的要求。
4、在样品干过滤时,为什么要弃去前过滤液?这样做会不会影响实验结果?为什么?
答:干过滤主要是保持溶液浓度不变而采取的一种过滤方法,前液中可能有一些滤纸或滤膜上的杂质存在,为了保持溶液浓度不变,所以要将前液去掉。干过滤为分离掉溶液中的固体,并且不改变溶液浓度而采取的一种方法。为保持溶液浓度不变。前段滤液要弃去,并且滤纸漏斗盛接的烧杯都要干的。这样做不会影响实验结果。
