������ѧʵ��κ�˼����
ȼ���ȵIJⶨ
1����ʵ���У���Щ����ϵ����Щ�ǻ������Ը������õ�����ŵУ��ͼ��������ϵ�뻷�����Ƚ����������
����ϵָ���Ʊ�����������Χ���ʣ�����������ˮ��Ͱ����������)������������ϵͳ����IJ��֡�ͼ������136ҳ���ڷ�Ӧ���ڣ����ڻ������ȷ����Լ�����������ϵ���¶�����ΪEE´��Ӧ�۳�������Ӧĩ��������ϵ���¶ȸ��ڻ������¶ȣ���ϵ����©�ⲿ������ΪCC´Ӧ�ò�����EC´��Ϊ��Ӧ��ȼ��ǰ����¶ȱ仯��T��
2��ˮͰ�е�ˮ�£�ΪʲôҪѡ��Ȼ����¶ȵ�0.5~1�棿�����к�Ӱ�죿
��Ϊ������ŵУ��ͼ���õ�ȷ�Ħ�T���������ڻ����ȷ���ͽ���������������۳���
3�����������ȼ�������ݼ������ı������ȣ�
C10H8 +12O2 ��10CO2+4H2O
������ȼ���ȵ��ڸ÷�Ӧ�ķ�Ӧ�ȣ��÷�Ӧ�ķ�Ӧ���ֵ����������ʵ��ܺ��뷴Ӧ����ʵ��ܺ�֮�
Pb-Sn��Ԫ������ͼ�Ļ���
1�� ���ڲ�ͬ�ɷֵĻ����IJ������ߣ���ˮƽ����ʲô��ͬ��Ϊʲô��
�𣺶��ڲ�ͬ�ɷֵĻ����IJ�������ˮƽ�εij��̲�ͬ����Ϊˮƽ�εij��������ʵ����ʣ���ȴ�ٶȺͼ�¼�ٶ��йأ�
2�� ����һ�����Ͳ������ߵ�ÿһ���ֵĺ��壿
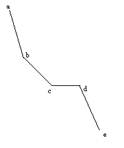 �𣺵����ڵ�ϵͳ������ȴʱ�����ϵͳ��������䣬��ϵͳ���¶���ʱ��ı仯�Ǿ��ȵģ���ȴ���ʽϿ죨��ͼab�߶Σ���������ȴ�����з�������䣬�������������а����ŷ���ЧӦ������ϵͳ���¶���ʱ��仯�����ʷ����ı䣬ϵͳ����ȴ���ʼ��������������ϳ���ת�ۣ���ͼb�㣩������Һ������ȴ��ijһ��ʱ����ͼc�㣩,��ʱ��Һϵͳ�Ե��ۻ��������������ڵ��ۻ����ȫ��������ǰ��ϵͳ�¶ȱ��ֲ��䣬��˲��������ϳ���ˮƽ�߶Σ���ͼcd�߶Σ�������Һ��ȫ���̺��¶Ȳ�Ѹ���½�����ͼde�߶Σ���
�𣺵����ڵ�ϵͳ������ȴʱ�����ϵͳ��������䣬��ϵͳ���¶���ʱ��ı仯�Ǿ��ȵģ���ȴ���ʽϿ죨��ͼab�߶Σ���������ȴ�����з�������䣬�������������а����ŷ���ЧӦ������ϵͳ���¶���ʱ��仯�����ʷ����ı䣬ϵͳ����ȴ���ʼ��������������ϳ���ת�ۣ���ͼb�㣩������Һ������ȴ��ijһ��ʱ����ͼc�㣩,��ʱ��Һϵͳ�Ե��ۻ��������������ڵ��ۻ����ȫ��������ǰ��ϵͳ�¶ȱ��ֲ��䣬��˲��������ϳ���ˮƽ�߶Σ���ͼcd�߶Σ�������Һ��ȫ���̺��¶Ȳ�Ѹ���½�����ͼde�߶Σ���
3�� ���ڴ�����ȵ�����ֻ������������ϵĵ�һ���յ㽫���Ѷ���
��������¶�ȴ����ȷȷ�����෴������һ����ֵĺ������ٵ���Ʒ����һ���յ㽫����ȷȷ�������ڶ����յ㽫��ȷ���ⶨ��Ϊʲô��
�𣺵���������ʱ�ų������ȣ�����������߷���ת�ۣ��۱��Ƿ�����ȡ���ڷų����������ܵ���ɢʧ�����Ķ��٣����ų����������ܵ���ɢʧ�����Ĵ֣��۱�����ԣ�����Ͳ����ԡ����ں��д�����ȵ�����ֻ�������һ���������ʱ�������������Ե�����һ��ּ�����������ɢʧ�����Ե�һ���յ����ȷ��������������ֺ����൱�����ֹ���ͬʱ����ʱ����ǰһ�������ų���������Ӱ���С����˵����¶ȿ���ȷȷ��������һ����ֺ����ٵ���Ʒ����һ���յ����ȷ���ڶ����յ㽫����ȷ����
˫Һ��ϵ��Һƽ����ͼ�Ļ���
1�� �ڲⶨ�У��й��Ȼ�����������ʱ��ʹ��õ���ͼ����ʲô�仯��
��η�ֹ��
�𣺹���ָ���ڱ����ȵ�Һ���м��������ڿ�����ԭ��ʹ��Һ����¶ȿ��������������е�ܶ�������ڣ���ʱ��õ��¶Ȼ��ʵ��ֵƫ�ߣ���ͼ���ƣ������õ���˿���Ȼ������ʯ��ֹ��������ָ�������������ܺ�Բ����ƿ֮������ܹ�����λ�ù��ߣ����·е�ϸߵ�����ȱ�����������������Ʒ��ɷ���ƫ�������������������ܵ�Һ���У�ʹ����ͼ�������������ƣ�����ͨ��ƽ�������ǵ����������������
2�� ����ж���Һ�Ѵ�ƽ��״̬��
���¶ȼƵ�ʾ�����ٱ仯��
3�� ƽ���������е�����֧�ܿ���Һ����ߺ��¶ȼ�ˮ������ߺ��ͣ�
�Բ����к�Ӱ�죿
��ƽ���������е�����֧�ܿ���Һ����ߣ���ɷе�ϸߵ�����ȱ���������������������Ʒ�������ƫ�ʹ��Һ���и߷е����ʺ������٣������и߷е��������࣬��ͼ�����������ơ��෴�Ļ����ڵ�Һ���п��ܽ���С���ڣ���ͼ���Ų������ơ�
�¶ȼ�ˮ������ߣ���õ�Ϊ������¶ȣ��¶ȱ�ߣ���ͼ���ơ�
�¶ȼ�ˮ������ͣ���õ�ΪҺ����¶ȣ��¶ȱ�ͣ���ͼ���ơ�
��������������Ӧ���ʳ����IJⶨ
1�� ʵ���õ絼���ⶨ��������ʲô����Ӧ���Ũ�Ƚϴ�ʱ���ܷ��ø÷�
���ⶨ��Ϊʲô��
��ֻ����ϡ��Һ�У�ij��ǿ����ʵĵ絼�ʲ�������Һ��Ũ�ȳ����ȣ�������Һ���ܵ絼�ʲŵ��������Һ�ĵ���ʵĵ絼��֮�͡���Ӧ��Ũ�ȹ���ʱ���ܲ��ô˷�����Ϊ�絼����Ũ�Ȳ������ι�ϵ��
2�� ��������������ӦΪ������Ӧ����δ�ʵ��������֤��
����Lt�ԣ�L0-Lt��/t��ͼ�õ�һ��ֱ�ߡ�
3�� ��ϴ���ڵ缫ʱӦע��ʲô��
����ϴ���ڵ缫ʱ������ǿ��ǿ�Ҫ������ˮ��ϴ���м����缫�ϵIJ��ڣ����Ⲭ�����䣬Ӱ��缫������
��ͪ�⻯��Ӧ���ʳ����IJⶨ����ܵIJⶨ
1�� ��ʵ���У���ͪ�⻯��Ӧ��������Ӧ������Ϊʲô��
�𣺸÷�Ӧ���㼶��Ӧ��������Ϊ�����Ӧ����������ģ�����ͪ����Ե��ǹ����ģ�����Ϊ�ڷ�Ӧ�����б�ͪ�����Ũ�Ȼ������ֲ��䣬����ͨ��ʵ����֤ʵ�����Ũ�Ȳ�̫�������£���ͪ�⻯��Ӧ�Ե����㼶��Ӧ������Ӧ�ٶ�����Ũ���أ������Ӧֱ����ȫ������֮ǰ����Ӧ�ٶȽ�ʹ������
2�� ����ʹ��Ӧ��һ����Ӧ���ɴ������ڷ�ӦҺ����ʱӦ����ʲô�ֶΣ�
д��ʵ�鷽����
��
3��Ӱ�챾ʵ������ȷ�ȵ���Ҫ��������Щ��
���¶Ⱥ�Ũ�ȡ�
����ˮ�ⷴӦ���ʳ����IJⶨ
1��Ϊʲô�ڱ�ʵ����û�ж������ǵ�������У�������������������
������������������Ϊ�����ݴ�����������k��Ҫ���Ǧ�t -���� �����������У�����Ե�����
2������������Һʱ��������ȷ���Բ����������Ӱ�죿
����Ӱ�졣��Ϊ������Һ���������Ũ�ȳ��ϸ�����ȣ��������ָʾŨ�ȡ�
3�� �ڻ��������Һ��������Һʱ�����ǽ�����ӵ�������Һ��ȥ���ɷ�
��������Һ�ӵ�������Һ��ȥ��
�������Ǵ������ڼ���һ��ʱ��ʱ����ʱȷ�����ҷ�Ӧ���ʳ�����������Ũ��Ϊ���ģ������Ǽӵ������У����ǵ�Ũ�ȱ㲻�̶�������ʱ������ʵ��ԭ����
��Һ���������IJⶨ
1�� ���ݵ��ݳ��ٶȶ�ʵ�����к�Ӱ�죿ëϸ�ܲ�����������Һ����
�ж�ʵ��������ʲôӰ�죿
��ëϸ���е�����Ҫ���ȶ��Ҽ�ϣ����������ڱ�����������ڱ��������ƽ�⣬���ɼ���������Ӽ����������ڵ�Ħ���������ܻ��ƽ��ʱ�ı��������������ٶ�̫�죬��������ƫ�ߡ�ëϸ���ڵĿ���ѹ����ܿڴ���Һ���������ƽ�⣬����һ����Ⱥ����ӿ���ѹ�����ܵ�����һ�����ɵ�ѹ����ʹʵ���õı�������ֵƫ�ߡ�
2�������Ҵ�ˮ��Һ�ı�������ʱ��Ϊ��������ϴëϸ�ܺ�֧�Թܣ��ⶨ�۹���Ӧ�ںδ�ȡ����
�𣺲ⶨʱ��ϡ��Ũ�ⶨ��������Һ�ľ�ȷ��������۹��ʶ����ͼ��õġ�ȡ����֧�Թ�ȡ����
������������綯��λ�IJⶨ
1�� �ܽ����ӵĵ�Ӿ�ٶ�����Щ�����йأ�ʵ������ο�����Щ���أ�
����ӵ����ݶ�Խ��������Խ�࣬����ԽС�����ʵ���ԽС�����Ӿ�ٶ�Խ��
2�� ��Ӿ�и���Һ��ѡ������������Щ������
�𣺦Ƶ�λ�Ը���Һ�ijɷ�ʮ�����У����ѡ�øý�����Һ�ij���Һ��1-1�͵���ʵĸ���Һ��ѡ��KCl��Һ����ΪK Cl Ǩ���ʻ�����ͬ�����⣬����Һ�ĵ絼���ܽ�һ�£���������洦�糡ǿ��ͻ��������۽����ƶ��ٶȲ��Ȳ�������ģ����
�߾�����Է������IJⶨ
1�� �߾�����������봿�ܼ�����Ϊʲô����ȣ�
�𣺴��ܼ����ȷ�Ӧ���ܼ�����֮�����Ħ����ЧӦ���߾���������ȷ�Ӧ��������ϡ����Һ�У��ܼ�������߷���֮�����Ħ��ЧӦ��
2�� ���ȷ���߾������Է�������ʱ���߾�����Һ����ëϸ�ܵ�ʱ��
ΪʲôҪ����100�룿
�𣺶���һ������ëϸ���ȼƣ�ֻ����t>100ʱ����Һ���Ȳ�����Һ��ëϸ���е�����ʱ������ȣ����ݴ����ķ����ŷ��ϡ�
ԭ��ص綯�ƵIJⶨ
1�� ��λ��Ʋ����綯�ƹ����У��������ƹ�����dz�һ������ƫת����
��ʹʲôԭ��
�𣺱�����Ƹ��ڵ�λ��Ƶ����ޣ��������û�е綯���������
����ص��Ƶ��ڹ涨ֵ��������·���ж�·�������أ�����أ�������ؼ��Խӷ���
2�� ���ŵ�ѡ��Ӧ��ע��ʲô���⣿
�����ŵ���ʲ��������˵缫��Һ������ѧ��Ӧ�����ŵ������Һ����������Ǩ����Ӧ����ȣ����ŵ������Һ��Ũ��ͨ���ܸߣ������ﱥ��״̬��
�ڶ�ƪ��������ѧʵ��(�Ͼ���ѧ������)�κ�˼�����ܽ�
������ѧʵ�飨�Ͼ���ѧ�����磩�κ�˼�����ܽᡪ�������ռ������ο�
Һ�履������ѹ�IJⶨ----��̬��
����˼���⣺
1�𣺷�������ⶨ�������ܼ��ӷ���Һ��Ũ�ȷ����仯�����ܲ�;���Ƕ���������ı�����Һ���ߺ����ȿ���ʹ�ñ������ⶨ��
2�������¶�Խ��
��ԵIJ��������¶�ͬ��������
�Ӷ��ı�������ߵ���������
ʹ���������ڲ�����Ӳ�Ƚ��� ��չ�����ӵȵȴӶ�ʹ����ֵ�ı�
ȼ���ȵIJⶨ
1ʵ������Щ����ϵ����Щ�ǻ�����ʵ���������������ģ���Щ����Ķ�ʵ��������Ӱ�죿
����Ͱ��������Ϊ��ϵ������Ͱ��Ϊ������ʵ�������������ģ���������������Ͱ������Ͱ��ʹ����Ͱˮ�±�����ֵ�ͣ���ʹ��ȼ����ƫ�͡�
2ˮͰ�е�ˮ��ΪʲôҪѡ�����Ͳˮ�µͣ��Ͷ��ٺ��ʣ�Ϊʲô�� �𰸣�Ϊ�˼�������ģ���Ӧ����
ϵ���Ȼ�ʹ��Ͳ���¶����ߣ�ʹ��ϵ�뻷�����¶Ȳ�ֽ�С�̶ȣ���ϵ�������Ҳ�����١���1�����Һ��ʣ��������������Ʒȼ�պ���ϵ���Ȼ�ʹ��Ͳ���¶����ߴ��2�����ң�������Ӧǰ��ϵ�Ȼ�����1 �ȣ���Ӧ����ϵ�Ȼ�����1 �ȣ�ʹ���²���С���������С��
3�����ܻ��С���1�� ʵ������н���̫����̫�죻��2������˿��ҩƬ֮��ľ���; (3)ҩƬû�и����4������ʱ��Ħ������5��ѹƬʱ���ɻ��
Ӧ�����Ϸ��濼�ǣ�ʵ����������ٽ��裬����˿��ҩƬ֮��ľ���ҪС��5mm��Ӵ�������������ȼ����סҩƬһ��Ҫ�����֤ȼ����ȫ������ʽ������Ħ��������ѹƬʱ��ѹ��Ҫ���еȵȡ�
T----Xͼ
1���������ռ���������Һ�Ĵ�״���Ĵ�С�Խ���к�Ӱ�죿
�����������·��İ���������������������������������Һ������������������ƽ��ԭ������Ӧ��������������ɲ��ٶ�Ӧƽ���������ɣ���˱�Ȼ����ͼ�Ļ��Ʋ���Ӱ�졣
2��ʵ���У��ⶨ��������ʱ�����ǵĺ����¶����
����Ʒʱ�����ǵĺ����¶��Ƿ���Ҫ����һ�£�Ϊ
ʲô��
������Һ�����������¶ȵĺ������¶Ȳ�ͬ�������ʲ�ͬ����ˣ����ߵ��¶ȱ���һ�¡�
3���������ʵ�����ʲôӰ�죿�����ʵ���о����ܱ��⣿
�����������������ʹҺ�������ƣ�������խ����ͨ��
�����ʯ�ķ�������������ʱ��Ӧ������Σ���ֹ��ʯʧЧ��
�ɡ����⣬�����Һ��ȡ�����϶࣬ҲӰ����Һ����ɡ�
4��ʵ��������Ҫ��Դ����Щ��
����ɲ�����(1)�������ߣ�(2)����������ЧӦ��(3)ȡ������
�¶Ȳ�����(1)�����ٶȣ�(2)�¶ȼ�У����
����ˮ�����ʳ����IJⶨ
1���ǵ�ת�����ʳ���k ����Щ�����йأ�
���¶ȡ�����Ũ�ȡ�
2�ڲ�������ת�����ʳ����ģ�ѡ�ó�������ܺã����Ƕ̵�����ܺã�
��ѡ�ýϳ�������ܺá����ݹ�ʽ����������×1000/Lc��������������������£�LԽ������Խ���������Բ������ԽС��
3��θ������ǡ������Ǻ���ı�����ȼ����0�ͦ���?
�𣺦�0������������Dt��L[����]0/100
������������������Dt��L[������]��/100������������Dt��L[����]��/100

ʽ�У�[�� ����] D t ����[�� ������] D t ����[�� ����] D t ���ֱ��ʾ���ƻƹ�����Դ��t��ʱ���ǡ������Ǻ��ǵı�����ȣ�L(��dm��ʾ)Ϊ����ܵij��ȣ�[����] 0Ϊ��ӦҺ�����ǵij�ʼŨ�ȣ�[������] ����[����] ����ʾ�����Ǻ����ڷ�Ӧ���ʱ��Ũ�ȡ�
��t��20�� L=2 dm [����]0=10g/100mL ��
��0��66.6×2×10/100��13.32°��
�� ��������×2×10/100×��52.2-91.9������3.94°
4���Է�����ʵ�������Դ����������ʵ����
���¶ȡ���Դ������㶨��������ҺҪ�������䡣
1��ʵ���У�Ϊʲô������ˮ��У�������ǵ���㣿��
����ת����Ӧ�����У����������Ȧ�t �Ƿ���Ҫ��
��У����Ϊʲô��
��(1)��ˮ���ܼ���Ϊ�����������ʡ�
(2)���裬����lg(��t-����)��t ͼ���������У�����Լ��㷴Ӧ�ٶȳ�����Ӱ�졣
2��������ҺΪʲô�ɴ������ƣ�
����÷�ӦΪ()һ����Ӧ����һ����Ӧ�����ʳ�������˥������ʼŨ���أ�ֻ����dC/dt ���ɡ�
4���Է�����ʵ�������Դ����������ʵ����
���¶ȡ���Դ������㶨��������ҺҪ�������䡣
BZ��
1��Ӱ���յ��ڵ���Ҫ��������Щ��
��Ӱ���յ��ڵ���Ҫ�����з�Ӧ�¶ȡ���Ⱥͷ�Ӧ���Ũ�ȡ��¶ȡ���ȡ����������ӻ��ԡ������ӵ�Ũ��
2����ʵ���¼�ĵ�����Ҫ����ʲô��˼����Nernst������õĵ�λ�кβ�ͬ��
�𣺱�ʵ���¼�ĵ�����Pt˿�缫��αȵ缫����ʵ���Ǹʹ��缫����ĵ���,��Nernst������õĵ�λ�ǵ缫����ڱ��缫�ĵ��ƣ�����ӳ�˷DZ��缫���ƺͱ��缫���ƵĹ�ϵ��
��������
1����������ݷ��ⶨ��������ʱΪʲôҪ�����ѹ����?
�𣺷���ëϸ�ܿ����ݵ��γ������ѵĹ����У����ݵİ뾶������Ĥ���������Ĺ�ϵ�У�
�� ʱ�����ݵ�
ʱ�����ݵ�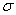 �ﵽ���ʱ����
�ﵽ���ʱ���� ����
����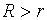 ʱ��
ʱ��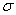 ��С��������������ʹѹ��������������������ѡ��ʶ�ȡ���ѹ�ʹ����
��С��������������ʹѹ��������������������ѡ��ʶ�ȡ���ѹ�ʹ����
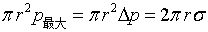 ���Ӷ��������������
���Ӷ��������������
2����Щ����Ӱ����������ⶨ�������μ�С����������Щ���ض�ʵ���Ӱ�죿
��Ӱ��ⶨ����������У�����ϵͳ���������Ƿ����ã��ⶨ�õ�ëϸ���Ƿ�ɾ���ʵ���������Ƿ�ƽ��������ëϸ�ܶ˿��Ƿ�ֱ����Һ�棻ëϸ�ܿ������ѳ��ٶȣ������¶ȡ�
��������Ҫ��֤����ϵͳ�������ԣ��ⶨ�õ�ëϸ�ܽྻ��ʵ��������ƽ��������ëϸ�ܶ˿�һ��Ҫ�պô�ֱ����Һ�棬�����뿪Һ�棬�������壻��ëϸ�ܿ��ѳ�����ÿ��ӦΪһ����������ѳ��������������¶��йأ�Ҫ����Һ���º��ٲ�����
3����Һ©����ˮ�ٶȹ����ʵ������û��Ӱ�죿Ϊʲô��
������ˮ�ٶ�̫�죬��ʹ�����ٶ�̫�죬���ݵ��γ����ݳ��ٶȿ�����ȶ�����ʹ�������ȶ������۲������ߵ���ϴ����
ճ�ȷ���߾���



�Ż��ʵIJⶨ
1����ͬ���ŵ����²�õ���ƷĦ���Ż����Ƿ���ͬ?
����ͬ��Ħ���Ż����������������������ʣ�������Ϊ���ŵ����IJ�ͬ���䡣�����ڲ�ͬ���ŵ����²�õ�cM���в�ͬ������Ҫԭ��������ƽ�ⶨ�ۺܳ���Լ50cm��������Dw�ı仯��ɵģ���Ȼ�¶ȵı仯Ҳ��һ��Ӱ�졣
2���ùŰ�����ƽ�ⶨ�Ż��ʵľ��ܶ�����Щ�����й�?
�𣺣�1����Ʒ�ܵ�����λ�ã����������ż�֮�䣬�ײ���ż���������ƽ��������Ʒ�ܵ����������κ�������Ӵ���
��2��Ħ��̽ͷ�Ƿ��������ֹ��Ƿ��ɶ������ɶ������̣�
��3���¶ȹ��գ��¶Ȳ��˸���60�棬����ǿ�����䣬�����ڸ�ʴ�����峡����ʹ�ã�
��4��Ħ��̽ͷƽ����ų�����Ҫ��ֱ��
��5������Ʒ�������ྻ��ÿ��װ���߶ȣ����ȶ���һ������������ľ��ܲŸߡ�
�綯�ƵIJⶨ
1��������綯�Ƶ�װ���У���λ��ơ�����ء������Ƽ�������ظ���ʲô���ã�
��ԭ�����ϸ���Ƶ����ڽӽ������������ⶨ��صĵ綯�ơ��ڴ������ϲ���һ����С��ȣ������෴����ӵ��Ʋ������������û�е���ͨ������ӵ��Ʋ�Ĵ�С�����ڴ����صĵ綯�ơ�
��λ��ƣ����ڵ�ص綯�ƺ͵缫���ƵIJ�����
�����ƣ�����ƽ��ֱ������������������Ϊʾ��װ�á�
����أ��ṩ�綯�Ƶı��ο��������Ա궨��λ��ơ�
������أ��ṩ������ص綯�Ʒ����෴����ֵ������ȵ���ӵ綯�ƣ����Զ��������صĵ綯�ơ�
2���αȵ缫Ӧ�߱�ʲô����������ʲô���ã�
�𣺾߱����������ȶ��ԡ������ԡ������ԡ�
���ã��������缫��
3��������ʲô���ã�ѡ�������ŵ�����Ӧ��ʲôԭ
��
�����ã���СҺ�ӵ�λ(���š���Һ���)��
ԭ��(1)������ҺӦ��������Һ������ѧ��Ӧ��(2)������Һ���������ӵ�Ǩ����Ӧ������ȡ�
4��UJ��25 �͵�λ��Ʋⶨ�綯�ƹ����У���ʱ������
��һ������ƫת������ԭ��
�𣺵�ؼ��Խӷ��������ص綯��̫��
5��ص綯���������Ȼ��ص�Ũ�ȵĹ�ϵ��
������Ũ�ȴ��ݾʹ�����ƶ���ɾʹ綯��ҲԽ��
7.��������ֵ��ʵ����ֵ��������������ԭ��
��ԭ��ص綯�Ʋⶨ����������Դ�кࣺܶ����ع���ʱ���������ʱ���е���ͨ�������綯��ƫ�룻��������Ⱦ�����ʹ��缫���Ʋ��ȶ���δ�ܽ���λ�����ť�趨�ڴ����ص綯��Ӧ�еĴ���λ�ã�ʹ���������е���ͨ���ȵȡ�
����������������Ӧ
1.Ϊʲôʵ����NaOH����������Ӧ��������?
������������Һ�����տ����ж�����̼�����ʣ������������ӷ��ͷ���ˮ�ⷴӦ��ʹŨ�ȸı䡣
2.Ϊ�α�ʵ��Ҫ�ں��������½��У�����CH3COOC2H5��NaOH��Һ�ڻ��ǰ��ҪԤ�Ⱥ��£����ʱ�ܷ�����������Һ����NaOH��Һ��һ��ʱ��ʼ��ʱ��
�𣺣�1����Ϊ�¶ȶԵ絼��Ӱ�졣��2�����ܣ�Ӧ�ջ���꿪ʼ��ʱ��
3.������Һ�ĵ絼������Щ���ӵĹ���?��Ӧ��������Һ�ĵ絼��Ϊ�η�������?
�𣺲��뵼��������С��͡��ڷ�Ӧǰ��Ũ�Ȳ��䣬��Ǩ���ʱȵ�Ǩ���ʴ�öࡣ����ʱ������ӣ����ϼ��٣��������ӣ����ԣ���ϵ�ĵ絼��ֵ�����½���
��β�K
4 CH3COOC2H5��NaOH = CH3OONa��C2H5OH
t=0 C0 C0 0 0
t=t Ct Ct C0 - Ct C0 -Ct
t=�� 0 0 C0 C0
���ʷ���ʽ �����ֲ����������ʳ���k�ı���ʽΪ��
�ٶ��˷�Ӧ��ϡ��Һ�н��У���CH3COONaȫ�����롣��μӵ���������Na����OH����CH3COO��,��Na����Ӧǰ�䣬OH����Ǩ����ԶԶ����CH3COO�������ŷ�Ӧ�Ľ��У�
OH�� ���ϼ�С��CH3COO���������ӣ�������ϵ�ĵ絼�ʲ����½�������ϵ�絼�ʣ��ʣ�
���½��Ͳ���CH3COO����Ũ�ȳ����ȡ�
�� ���ͷֱ�Ϊ0��t�͡�ʱ�̵ĵ絼�ʣ���
t=tʱ��C0 �CCt=K�� - �� KΪ��������
t����ʱ��C0= K�� - ��
��������ʽ�ӣ������ã�
�ɼ�������֪��ʼŨ��C0���ں��������£���ú� ������ �� ��ͼ���ɵ�һֱ�ߣ���ֱ��б�� ���Ӷ���ô��¶��µķ�Ӧ���ʳ���k��
