实验十四 胶体制备和电泳
1. 摘要
胶体中电泳现象及其实验装置的研究相对来说起步较晚。有文献可查的实验装置是
1937年,A.Tselius设计的一套较精密的界面移动法电泳装置[1],主要用于蛋白质的研究,对于肉眼不能观察的界面移动,他采用条纹摄影技术跟踪,其工作为界面移动法奠定了基础,关于界面移动法的详细讨论,可参见L.G.Longsworth编辑的专著[2]。
测量溶胶的z 电位是通过测定在两铂电极间外加一定直流电场(约100V左右),胶体溶液与辅助溶液间可见界面在单位时间内的移动距离。据公式
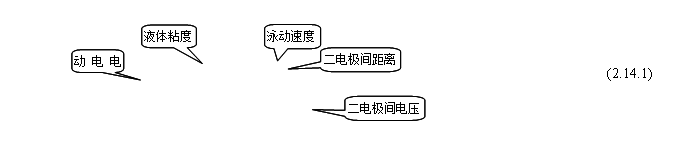


通过观察时间t内电泳仪中溶胶与辅助液的界面在电场作用下移动距离即泳动速度u求z。
实验进行时,两电极上有气泡析出(发生电解),会导致辅助溶液电导率发生变化和扰动界面,影响实验结果。可以将辅助溶液与电极用盐桥隔开或将铂电极改用电化学上的可逆电极[2][3]。
关键词:电泳 动电电位 Fe(OH)3溶胶 半透膜
2. 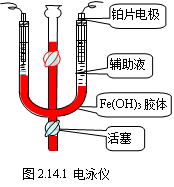
 装置
装置
3. 预习提问
(1) 什么叫胶体的电泳现象?与电渗有何异同处?
(2) 溶胶盍电电位是什么含义?能否直接测得?有哪些方法可测?
(3) 胶体聚沉有哪些条件?
(4) 电泳公式各量含义及其单位?电泳仪能否测反离子移动速度?
(5) 影响胶体电泳测定的因素有哪些?
4. 操作
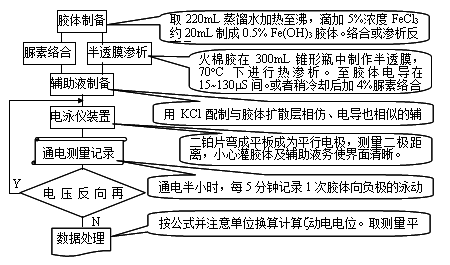
5.数据处理
(1)将实验数据填入下表
室温 大气压 e= h= E= l = G胶= G辅=
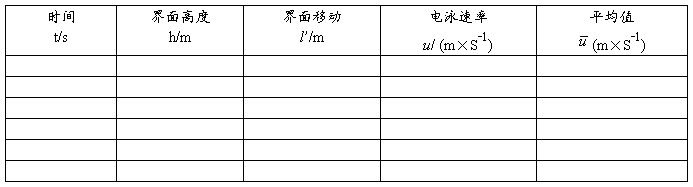
①按公式计算电们梯度及电泳速度。
②由液体的介电常数(0~45°C):lnet=4.474268-4.54420´10-3t,粘度等计算z 电位。
(2)文献值:氢氧化铁溶胶z= +0.044V,
硫化亚砷溶胶z= -0.032V,学生测值误差要求:±0.005V
6.点评
(1) 实验关键
①用2~5%FeCl3溶液水解制备Fe(OH)3溶胶时,FeCl3溶液应逐滴加入到沸腾的蒸馏水中并不断搅拌,加完后根据情况可适当延长煮沸时间,制得的溶胶不能长时间存放,若底部有沉淀物应除去。用火棉胶制作半透膜,渗析1~2天,其间需经常换蒸馏水。热渗析可加快渗析过程。还可配合加脲素,缩短渗析时间。不过,渗析也宜适当,渗析过分,没有足够量的反离子保障胶体的电学稳定性,溶胶反而易聚沉。
②电泳仪应洗净,避免因杂质混入电解质溶液而影响溶胶的z 电位 ,甚至使溶胶凝聚。
③辅助液的选择和配制对结果的准确性也有较大影响。如辅助液(本实验为稀NaCl溶液)的电导率与溶胶的电导不一致,电泳时溶胶部分与辅助液部分的电位梯度就不同,z电位的计算公式就不能适用。理论分析和经验均表明:若辅助液与溶胶电导不同,在界面处的电场强度发生突变,实验时就产生界面在一管中上升的距离不等于在另一管中下降的距离的现象,如辅助液电导过大,会使界面处溶胶发生聚沉。有报道[3],用NaCl稀溶液配制的辅助液远比用HCl的好。
④实验过程中,施于二极的电压的稳定性必须随时检查,予以保证。
(2) 界面移动法的困难之一是与溶胶形成界面的辅助溶液的选择。溶胶的z 电位对介
质成分十分敏感,从正负离子迁移速率要求相近来说,KCl比KNO3好,总是想到还是原配溶液好,可以想象用超离心方法取出由溶胶中分离出来的分散介质作为辅助液,称为“超滤液”。
(3) 本实验中采用两铂电极施加外界电场,电压达到100V以上,两电极上有气泡析
出(发生电解),致辅助液电导发生变化和扰动界面,影响实验。改善的办法是将辅助液与电极用盐桥隔开,或用电化学上的可逆电极替换铂电极[4]。
(4) 计算z 电位时,h、e 值采用同温度下纯水的数据,会引入一定误差。
(5) 在一般的物理化学教科书或实验教材中推导了电位与胶粒淌度的关系式。是在进
行了一系列的简化的情况下得到的,在更详细的电泳运动理论中,还必须考虑许多因素[5][6][7],例如:在外加电场中扩散层中的反离子向着与胶粒移动相反的方向运动。因此,胶体粒子是在运动着的液体中泳动,其结果是使电泳速度变慢,称为延时(retardation)效应。另一需要考虑校正的是滞后效应。由于胶体质点与扩散层中的反离子向相反方向运动,质点周围原来对称的扩散层发生变化,正负电荷中心不再重合。传导和扩散都会使双电层恢复原来的对称形状,这需要时间。因而,双电层的扩散部分总是落后于运动着的带电质点,形成一个与外加电场反方向的附加电场,带电质点的电泳速度也因此减小,有时还必须考虑表面电导的校正问题。
(6) 关于z 电位与胶休质点的电泳淌度的关系式,有的人认为能适用于各种不同形状
的粒子[8],P. Debye和E. Hückel[9]等认为与粒子的形状有关,后者已为多数人接受。
(7) 长时间通电会使溶胶及辅助液发热,接近电泳池管壁的溶胶或辅助液散热较管中
间部分的溶液快,管子中间部分的溶胶或辅助液就较管壁附近溶液具有较高的温度,溶液因密度差引起对流使界面不清晰。
(8) 本实验装置还可用来测定一些其它溶胶的z 电位和研究电解质浓度对溶胶z 电位
的影响,测定溶胶的等电点等。如果界面不能用肉眼看出,有时可使它在紫外光下发萤光而观察到,在此情况下仪器应用石英玻璃制作。
(9)溶胶电导大,说明杂质离子(多余Cl-1和FeO+)多,反离子多则扩散层被压缩,z 电位就相应减少,扩散层压缩到底,即z 电位=0,当z <20mV时胶体都是不稳定而要发生聚沉的,这主要是还有胶体的布朗运动,其强度足以克服胶粒之间所剩的较小的静电斥力作用而聚沉。
(10)Fe(OH)3是憎液溶胶,然而它已经具备某些亲液溶胶的性质,其亲液性方面比通常的憎液溶胶在聚沉值这一点上要大,但在达到一个相当大的浓度时却没有引起聚沉的危险,特别是其缓慢聚沉的阶段比典型憎液溶胶宽限得多。
7.解题研判
(1)电泳实验中辅助液的选择根据哪些条件?
解a 与胶体颜色反差要大,便于区分;
b 较胶体比重要轻,界面容易清晰;
c 辅助液正负离子迁移的速度要相近,克服两臂中上升和下降速度不等的困难。
d 辅助液电导要近于溶胶,以消除其间的电位梯度,否则,电泳公式不得不进行
修正,若电泳公式如一般实验教材所写: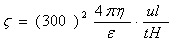 ,则电位梯度修正为
,则电位梯度修正为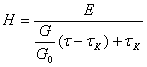 ,其中G 0为辅助液电导值,t K为两界面间距离。
,其中G 0为辅助液电导值,t K为两界面间距离。
(2)电泳速度的快慢与哪些因素有关?
解a 外加电场强度影响大,外加电压大,速度快
b 与胶体净化后所测电导值有关,电导大,电泳速度快;
c 与两极间距离有关,距离短,速度快;
d 与温度有关,温度高,介质的粘度降低,有利于电泳速度的提高;
e 与胶体的z 本性相关;
f 与辅助液的性质相关。
(3)加入脲素的作用?
解 a. 增加溶胶的比重,使与辅助液间的界面清晰。
b. 能络合一部分多余反离子Cl-,促进胶体稳定。

溶胶中加入脲素,电导迅速降低,在加至40%左右时发生转折,而后曲线斜率变小,说明络合了部分HCl。加脲素后的实验现象和结果与半透膜净化的结果无多大区别。
(4)用公式 计算时,各量采用哪些需要注意的单位?
计算时,各量采用哪些需要注意的单位?
解 计算z 电位时各物理量所使用的单位容易混乱。用公式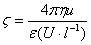 计算,并
计算,并
采用SI制,电位梯度(U×l-1)的单位是U×m-1,u的单位是m×s-1`。溶胶的h(粘度)和e(介电常数)应近似采用纯水的值,在室温下h=0.001Pa×s-1,e =8.89´10-9C×V×m-1(F×m-1法拉每米,则所得z 电位的单位为V,电渗实验中的计算相似。
(5) 为什么长时间渗析对溶胶有不利影响?如何理解z 是个阈值范围?
解 长时期渗析可以使带正电荷的氢氧化铁溶胶失掉电荷而聚沉。由于Fe(OH)3晶格上的FeO+的离子与Fe(OH)3晶核结合是不牢固的它们间的力场是十分不对称的,所以,一方面有被核表面所吸附的FeO+离子,另一方面在分散介质中有同种离子与前者处于吸附平衡的状态。渗析时不是从核表面上,而是主要从溶液中,也就是从分散介质中洗去起稳定作用的电解质,对Fe(OH)3溶胶来说,透过薄膜的就是Cl-1和FeO+离子,这个过程破坏了吸附平衡,并引起FeO+离子从核表面上解吸出来,核表面便被“裸露”,终于导致溶胶聚沉。因为胶团业已破坏,即或算得z 值,已不能代表稳定的Fe(OH)3溶胶的动电电位了。
既然溶胶的动电电位与核表面所吸附的FeO+离子数量的变化有关,也与胶体溶液中所含杂质离子的浓度有关,也就不能期望通过渗析作用仅仅洗去胶体表面多余部分的反离子,所以有理由认为溶胶的z 电位不应该是一个确定值,而是有个阈值范围。所以前人说,测z验,不同的实验者有不同的结果。电导值较小时测得的z 电位较大些,稳定的Fe(OH)3胶体,z =30~44mV。
(6) 293K时测得两电极间电势为75V,20分钟内Fe(OH)3胶体泳动距离为10.0mm,电极距离为30.0mm,已知水的相对介电常数为81.0,粘度为1.00´10-3Pa×s,试求氢氧化铁溶胶的z 电势。
解:电位梯度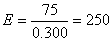 V×m-1
V×m-1
电泳速率 m×s-1
m×s-1
介电常数e =Dre 0=81.0´8.85´10-12=7.17´10-10F×m-1
其中1F=1C×V-1。得
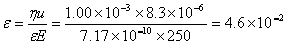 V
V
[参考文献]
[1]A.Tiselius. Trans. Faraday Soc. 33. 524(1937)
[2]L.G.Longsworth, “Electrophoresis”(M. Bier ed. ), Chap. 3 and 4. Academic(1959)
[3]и. H. 普季洛娃著《胶体化学实验作业指南》,第6章.高等教育出版社(1955)
[4]北京大学化学系物理化学教研室实验课教学组.《物理化学实验》. 北京大学出版社. 112(1981)
[5]张五昌. “电泳”,《物理化学实验指导书》.东北师大文库,330(1995)
[6]A. W. 亚当森著,顾惕人译,《表面的物理化学》. 科学出版社. 219(1984)
[7]周祖康等编著,《胶体化学基础》,北京大学出版社. 258(1984)
[8]H.A.Abramson,J.Phys. Chem. 35, 289(1931)
[9]P. Debye, E. Huchel, Physik, Z. 25, 49(1924)
第二篇:胶体的制备和电泳


四、仪器药品
1.仪器
直流稳压电源1台;万用电炉1台;电泳管1只;电导率仪1台;直流电压表1台;秒表1块;铂电极2只;锥形瓶(250mL)1只;烧杯(800、250、100mL)各1个,超级恒温槽1台;容量瓶(100mL)1只。
2.药品
火棉胶;FeCl3(10%)溶液;KCNS(1%)溶液;AgNO3(1%)溶液;稀HCl溶液。
五、实验步骤
1.Fe(OH)3溶胶的制备及纯化
(1)半透膜的制备
在一个内壁洁净、干燥的250mL锥形瓶中,加入约10mL火棉胶液,小心转动锥形瓶,使火棉胶液粘附在锥形瓶内壁上形成均匀薄层,倾出多余的火棉胶于回收瓶中。此时锥形瓶仍需倒置,并不断旋转,待剩余的火棉胶流尽,使瓶中的乙醚蒸发至已闻不出气味为止(此时用手轻触火棉胶膜,已不粘手)。然后再往瓶中注满水,(若乙醚未蒸发完全,加水过早,则半透膜发白)浸泡10min。倒出瓶中的水,小心用手分开膜与瓶壁之间隙。慢慢注水于夹层中,使膜脱离瓶壁,轻轻取出,在膜袋中注入水,观察有否漏洞,如有小漏洞,可将此洞周围擦干,用玻璃棒蘸沾火棉胶补之。制好的半透膜不用时,要浸放在蒸馏水中。
(2)用水解法制备Fe(OH)3溶胶
在250mL烧杯中,加入100mL蒸馏水,加热至沸,慢慢滴入5mL(10%)FeCl3溶液,并不断搅拌,加毕继续保持沸腾5min,即可得到红棕色的Fe(OH)3溶胶,其结构式可表示为{m[Fe(OH)3]nFeO(n-x)Cl}xCl。在胶体体系中存在过量的H、Cl等离子需要除去。
(3)用热渗析法纯化Fe(OH)3溶胶
将制得的40mLFe(OH)3溶胶,注入半透膜内用线拴住袋口,置于800mL的清洁烧杯中,杯中加蒸馏水约300mL,维持温度在60℃左右,进行渗析。每30min换一次蒸馏水,2h后取出1mL渗析水,分别用1%AgNO3及1%KCNS溶液检查是否存在Cl及Fe,如果仍存在,应继续换水渗析,直到检查不出为止,将纯化过的Fe(OH)3溶胶移入一清洁干燥的100mL小烧杯中待用。
2.配制HCl溶液
调节恒温槽温度为(25.0±0.1)℃,用电导率仪测定Fe(OH)3溶胶在25℃时的电导率,然后配制与之相同电导率的HCl溶液。方法是根据附录二所给出的25℃时HCl电导率—浓度关系,用内插法求算与该电导率对应的HCl浓度,并在100mL容量瓶中配制该浓度的HCl溶液。
3.装置仪器和连接线路
用蒸馏水洗净电泳管后,再用少量溶胶洗一次,将渗析好的Fe(OH)3溶胶倒入电泳管中,使液面超过活塞(2)、(3)
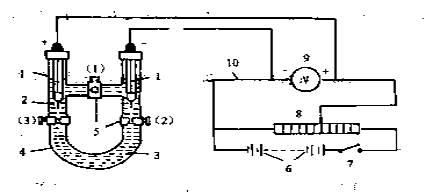
。关闭这两个活塞,把电泳管倒置,将多余的溶胶倒净,并用蒸馏水-3++-x+-+-
洗净活塞(2)、(3)以上的管壁。打开活塞(1),用自己配制的HCl溶液冲洗一次后,再加入该溶液,并超过活塞(1)少许。插入铂电极按装置图-1连接好线路。
图-1 电泳仪器装置图
1.Pt电极;2.HCl溶液;3.Fe(OH)3溶胶;4.电泳管;5.活塞;6.直流电源;7.电键;8.滑线电阻;9.直流电压表;10.电源线路。
4.测定溶胶电泳速度
同时打开活塞(2)和(3),关闭活塞(1),打开电键7,经教师检查后,接通直流稳压电源6,调节电压为100V。接通电键7,迅速调节电压为100V,并同时记时和准确记下溶胶在电泳管中液面位置,约1h后断开电源,记下准确的通电时间t和溶胶面上升的距离d,从伏特计上读取电压E,并且量取两极之间的距离L。
实验结束后,折除线路。用自来水洗电泳管多次,最后用蒸馏水洗一次。
六、注意事项
1.利用公式(3)求算ζ时,各物理量的单位都需用c.g.s制,有关数值从附录中有关表中查得。如果改用SI制,相应的数值也应改换。对于水的介电常数,应考虑温度校正,由以下公式求得:
lnDt=4.474226-4.54426×10t
式中,t为温度℃。
2.在制备半透膜时,一定要使整个锥形瓶的内壁上均匀地附着一层火棉胶液,在取出半透膜时,一定要借助水的浮力将膜托出。
3.制备Fe(OH)3溶胶时,FeCl3一定要逐滴加入,并不断搅拌。
4.纯化Fe(OH)3溶胶时,换水后要渗析一段时间再检查Fe及Cl的存在。
5.量取两电极的距离时,要沿电泳管的中心线量取。 3+--3
七、数据处理
室温:t=23℃ 电压:U=200V 电极距离L:=0.103m
d0(cm) d(cm)
9.3
9.4 9.2
9.1
查表知23℃时水的黏度为:0.9358×10Pa·s 介电常数:D=79.02F/m
∴Fe(OH)3溶胶的电位ζ=4π·η·L·u·300?/D·E
=4×3.14×0.9358×10×0.103×300?/79.02/200
=6.9×10V
六.思考题
1.决定电泳速度快慢的因素是什么?
电泳速度的快慢与带电粒子的大小、形状、粒表面的电荷数目、溶剂电解质的种类、离子强度、以及PH值、温度和所加的电压等有关。
2.电泳中电解质液的选择是根据哪些条件?
1.辅助液和溶胶的电导率要尽量一致
2.辅助液与溶胶的颜色要有较大区别,以便形成清晰界面;
3.辅助液与溶胶不发生反应。
3.连续通电溶液发热的后果是什么?
电导率升高,胶体定向移动困难。
-3-3-3t(min) 10min 20min 30min
