物理化学实验报告
院系 化学与环境工程学院
班级 0409403
学号 040940302
姓名 徐 杰
实验名称 BZ振荡反应
日期 20##-12-6
同组者姓名 王保森
室温 10.2℃
气压 978.0mmHg
成绩
一、实验目的
1.了解BZ振荡反应的基本原理;体会自催化过程是产生振荡反应的必要条件。
2.初步理解耗散结构系统远离平衡的非线性动力学机制。
3.掌握测定反应系统中电势变化的方法;了解溶液配制要求及反应物投放顺序。
二、实验原理
自然界存在大量远离平衡的敞开系统,它们的变化规律不同于通常研究的平衡或近平衡的封闭系统,与之相反,它们是趋于更加有秩序、更加有组织。由于这类系统在其变化过程中与外部环境进行了物质和能量的交换,并且采用了适当的有序结构来耗散环境传来的物质和能量,这样的过程称为耗散过程。受非线性动力学控制,系统变化显示了时间、空间的周期性规律。
目前研究的较多、较清楚的典型耗散结构系统为BZ振荡反应系统,即有机物在酸性介质中被催化溴氧化的一类反应,如丙二酸在Ce4+的催化作用下,自酸性介质中溴氧化的反应。BZ振荡反应是用首先发现这类反应的前苏联科学家Belousov及Zhabotinsky的名字而命名的,其化学反应方程式为:
 (1)
(1)
真实反应过程是比较复杂的,该反应系统中HBrO2中间物是至关重要的,它导致反应系统自催化过程发生,从而引起反应振荡。为简洁的解释反应中有关现象,对反应过程适当简化如下:
当Br-浓度不高时,产生的HBrO2中间物能自催化下列过程:
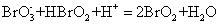 (2)
(2)
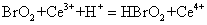 (3)
(3)
在反应(3)中快速积累的Ce4+又加速了下列氧化反应:
 (4)
(4)
通过反应(4),当达到临界浓度值 后,反应系统中下列反应成为主导反应:
后,反应系统中下列反应成为主导反应:
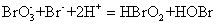 (5)
(5)
 (6)
(6)
反应(6)与反应(2)对HBrO2竞争,使得反应(2)、(3)几乎不发生。Br-不断消耗,当Br-消耗到临界值以下,则反应(2)、(3)为主导作用,而反应(5)、(6)几乎不发生。由此可见,反应系统中Br-浓度的变化相当于一个“启动”开关,当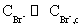 时,反应(2)、(3)起主导作用,通过反应(4)不断使Br-积累;当
时,反应(2)、(3)起主导作用,通过反应(4)不断使Br-积累;当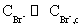 时,反应(5)、(6)起主导作用,Br-又被消耗。由于反应(2)、(3)中存在自催化过程,使动力学方程式中出现非线性关系,导致反应系统出现振荡现象。Br-在(5)、(6)中消耗,又在反应(4)中产生;Ce3+、Ce4+分别在(3)、(4)中消耗和产生,所以Br-、Ce3+、Ce4+在反应过程中浓度会出现周期性变化,而
时,反应(5)、(6)起主导作用,Br-又被消耗。由于反应(2)、(3)中存在自催化过程,使动力学方程式中出现非线性关系,导致反应系统出现振荡现象。Br-在(5)、(6)中消耗,又在反应(4)中产生;Ce3+、Ce4+分别在(3)、(4)中消耗和产生,所以Br-、Ce3+、Ce4+在反应过程中浓度会出现周期性变化,而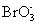 和
和 反应物,在反应过程中不断消耗,不会再生,因此,它们不会出现振荡现象。
反应物,在反应过程中不断消耗,不会再生,因此,它们不会出现振荡现象。
 值又反应(2)、(6)可求得
值又反应(2)、(6)可求得

所以 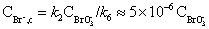
三、仪器与试剂:
NDM-1电压测量仪; SYC-15B超级恒温水浴;
磁力搅拌器; 反应器100ml;
217型甘汞电极; 213型铂电极;
数据采集接口装置; 计算机;
溴酸钾(GR); 硝酸铈铵(AR);
丙二酸(AR); 浓硫酸(AR)。
四、仪器装置连接图:
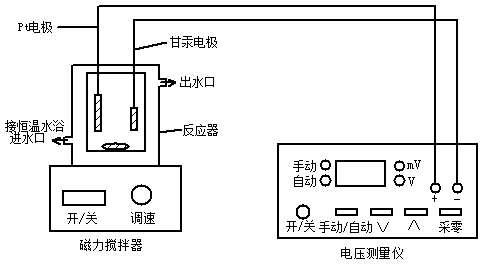
五、实验步骤:
1.用1.00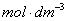 硫酸作217型甘汞电极液接;
硫酸作217型甘汞电极液接;
2.按图连接好仪器,打开超级恒温水浴,将温度调节至25.0±0.1℃;
3.配制0.45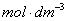 丙二酸250ml、0.25
丙二酸250ml、0.25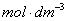 溴化钾250ml、3.00
溴化钾250ml、3.00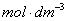 硫酸250ml;在0.20
硫酸250ml;在0.20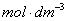 硫酸介质中配制
硫酸介质中配制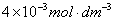 的硫酸铈铵250ml。
的硫酸铈铵250ml。
4.在反应器中加入已配好的丙二酸溶液、溴酸钾溶液、硫酸溶液各15ml;
5.打开磁力搅拌器,调节合适速度;
6.将精密数字电压测量仪置于分辨率为0.1mV档(即电压测量仪的2V档),且为“手动”状态,甘汞电极接负极,铂电极接正极;
7.恒温5min后,加入硫酸铈铵溶液15ml,观察溶液颜色的变化,同时开始计时并记录相应的变化电势;
8.电势变化首次到最低时,记下时间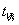 ;
;
9.用上述方法将温度设置为30℃、35℃、40℃、45℃、重复实验,并记下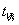 ;
;
10.根据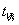 与温度数据
与温度数据 作图。
作图。
数据记录与分析
数据记录:
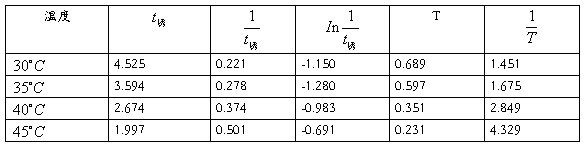
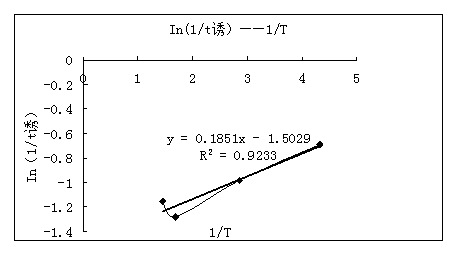
数据分析:作图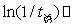
六、注意事项
1.实验中溴酸钾试剂要求纯度高,为GR级;其余为AR级。
2.配制硫酸铈铵溶液时,一定要在0.2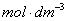 硫酸介质中配制,防止发生水解呈浑浊。
硫酸介质中配制,防止发生水解呈浑浊。
3.反应器应清洁干净,转子位置和速度都必须加以控制。
4.电压测量仪一定要置于0.1mV分辨率的手动状态下。
5.跟电脑连接时,要用专用通讯线将电压测量仪的串行口与电脑串行口相接,在相应软件下工作。
七、思考题
1.试述影响诱导期的主要因素。
解:中间体的生成速率。
2.初步说明BZ振荡反应的特征及本质。
解:BZ震荡反应的特征如下:(1)反应必须是敞开系统,且远离平衡态;(2):反应历程中应包含自催化的步骤;(3):系统具有双稳定性;
3.说明实验中测得的电势的含义。
解:说明离子的浓度随时间的周期化变化情况从而导致周期性的发生变化。
第二篇:化学振荡
化学震荡
一、目的要求
1、了解 、熟悉化学振荡反应的机理。
2、通过测定电位——时间曲线求得振荡反应的表观活化能。
二、基本原理
有些自催化反应有可能使反应体系中某些物质的浓度随时间(或空间)发生周期性的变化,这类反应称为化学振荡反应。
最著名的化学振荡反应是1959年首先由别诺索夫(Belousov)观察发现,随后柴波廷斯基(Zhabotinsky)继续了该反应的研究。他们报道了以金属铈离子作催化剂时,柠檬酸被HBrO3氧化可发生化学振荡现象,后来又发现了一批溴酸盐的类似反应,人们把这类反应称为BZ振荡反应。例如丙二酸在溶有硫酸铈的酸性溶液中被溴酸钾氧化的反应就是一个典型的BZ振荡反应。典型的BZ系统中,铈离子和溴离子浓度的振荡曲线如图1所示。
对于以BZ反应为代表的化学振荡现象,目前被普遍认同的是Field,Körös和Noyes在1972年提出的FKN机理。FKN机理提出反应由三个主过程组成:
过程A (1) Br-+BrO3-+2H+→HBrO2+HBrO
(2) Br-+HBrO2+H+→2HBrO
过程B (3) HBrO2+BrO3-+H+→2BrO2+H2O
(4) BrO2+Ce3++H+→HBrO2+Ce4+
(5) 2HBrO2→BrO3-+H++HBrO
过程C (6) 4Ce4++BrCH(COOH)2+H2O+HBrO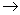 2Br-+4Ce3++3CO2+6H+
2Br-+4Ce3++3CO2+6H+
过程A是消耗Br-,产生能进一步反应的HBrO2,HBrO为中间产物。
过程B是一个自催化过程,在Br-消耗到一定程度后,HBrO2才按式(3)、(4)进行反应,并使反应不断加速,与此同时,Ce3+被氧化为Ce4+。HBrO2的累积还受到式(5)的制约。
过程C为丙二酸溴化为BrCH(COOH)2与Ce4+反应生成Br-使Ce4+还原为Ce3+。
过程C对化学振荡非常重要,如果只有A 和B,就是一般的自催化反应,进行一次就完成了,正是C的存在,以丙二酸的消耗为代价,重新得到Br-和Ce3+,反应得以再启动,形成周期性的振荡。
该体系的总反应为:
2H++2 BrO3-+3CH2(COOH)2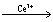 2BrCH(COOH)2+3CO2+4H2O
2BrCH(COOH)2+3CO2+4H2O
振荡的控制离子是Br-。
由上述可见,产生化学振荡需满足三个条件:
1.反应必须远离平衡态。化学振荡只有在远离平衡态,具有很大的不可逆程度时才能发生。在封闭体系中振荡是衰减的,在敞开体系中,可以长期持续振荡。
2.反应历程中应包含有自催化的步骤。产物之所以能加速反应,因为是自催化反应,如过程A中的产物HBrO2同时又是反应物。
3.体系必须有两个稳态存在,即具有双稳定性。
化学振荡体系的振荡现象可以通过多种方法观察到,如观察溶液颜色的变化,测定吸光度随时间的变化,测定电势随时间的变化等。
按在FKN机理基础上建立的俄勒冈模型,推导可得振荡周期t与过程C即反应步骤(6)的速率系数及有机物浓度呈反比关系,比例常数还与其它步骤的速率系数有关。如测定不同温度下的振荡周期,并近似地忽略比例常数随温度的变化,则可应用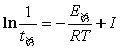 及
及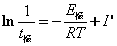 可估算过程C即反应步骤(6)的表观活化能E诱,E振。另一方面,随着反应的进行,有机物浓度逐渐减少,振荡周期将逐渐增大,并最终停止振荡,反应终止。
可估算过程C即反应步骤(6)的表观活化能E诱,E振。另一方面,随着反应的进行,有机物浓度逐渐减少,振荡周期将逐渐增大,并最终停止振荡,反应终止。
本实验采用电动势法测量反应过程中离子浓度的变化。以甘汞电极作为参比电极,用铂电极测定不同价位铈离子浓度的变化,用离子选择性溴电极测定溴离子浓度的变化。本实验通过测定离子选择性电极上的电势(U)随时间(t)变化的U-t曲线来观察BZ反应的振荡现象(见图1),同时测定不同温度对振荡反应的影响。根据U-t曲线,得到诱导期(t诱)和振荡周期(t1振,t2振,…)。

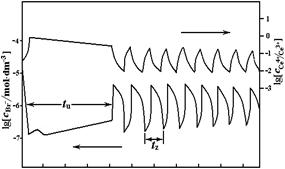
图1.振荡反应装置 图2. 振荡曲线
三、 仪器与试剂
仪器: 2D-BZ振荡实验装置,100ml电解池,光亮铂丝电极,217型双盐桥甘汞电极(用 H2SO4作液接盐桥),SYC-15B超级恒温槽,移液管,洗耳球。
试剂:0.05mol·L-1硫酸铈铵溶液(在0.2mol·L-1硫酸介质中配制)。
0.2mol·L-1溴酸钾溶液,0.4mol·L-1丙二酸溶液,3mol·L-1硫酸溶液
四、实验步骤
按图17-1连接好仪器装置,开启电脑,打开超级恒温槽,将温度恒定在25.0±0.1℃。在100mL的反应器中加入浓度为0.4mol·L-1的丙二酸、浓度为 0.2mol·L-1的KBrO3、浓度为 3mol·L-1的硫酸各10 mL混合,开启电磁搅拌使溶液在设定温度下恒温至少10min(调节调速旋钮约3圈半)。打开BZ振荡2.0软件,设置纵坐标0-1.5V,横坐标0-30min。待电压稳定后,开始绘图,绘图约5min后加入10mL浓度为 硫酸铈铵溶液,观察溶液颜色变化,
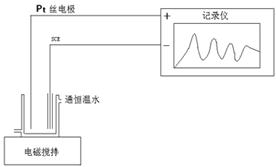
图18-1 B-Z反应实验装置示意图
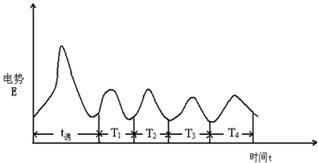
图18-2 B-Z反应的电势振荡曲线
经过一段时间后,此后的曲线呈现有规律性周期变化。图像出现10个周期以后,停止绘图。
获取振荡曲线数据和图像。
取出电极洗净电解池和所用电极,在20-50℃之间选择5-8个合适的温度(如20.0℃,25.0℃,30.0℃,···),在每个温度下重复上述步骤,绘制在不同温度下的曲线。
五、数据记录和处理
室温: 始:31.3℃ 末:31.7℃
大气压: 始:100.68kPa 末:101.60kPa
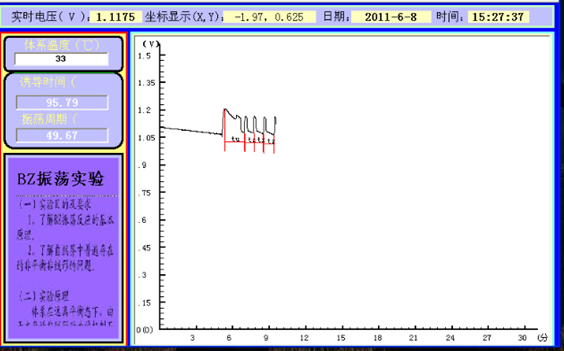
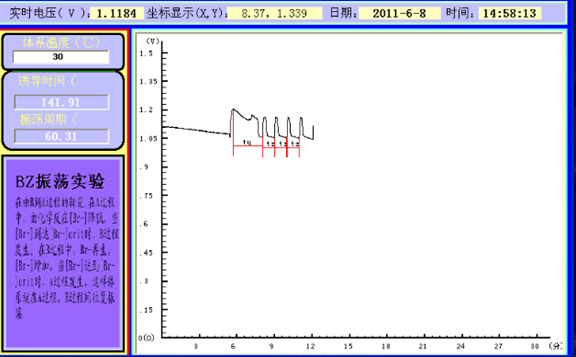

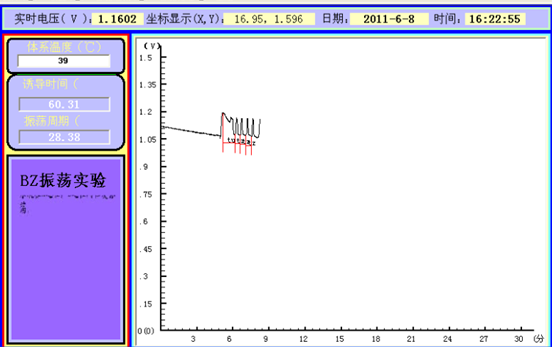
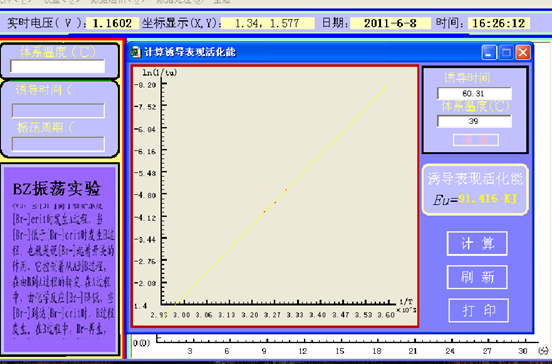

数据分析:根据上述图可得,诱导时间(tu)=60.31s,震荡周期(tz)=28.38s。
由图中直线的斜率可以求得诱导表观活化能(Eu)=91.416kJ,震荡表观活化能(Ez)=45.946kJ.
六、注意事项
(1)各个组分的混合顺序对体系的振荡行为有影响。应在丙二酸、溴酸钾、硫酸混合均匀 后,且当记录仪的基线走稳后,再加入硝酸铈铵溶液。
(2)反应温度可明显地改变诱导期和振荡周期,故应严格控制温度恒定。
(3)实验中溴酸钾试剂纯度要求高。
(4)配制硝酸铈铵溶液时候,一定要在硫酸介质中配制,防止发生水解呈浑浊。
(5)所使用的反应容器一定要冲洗干净,转子位置及速度都必须加以控制。
七、思考题
1、影响诱导期、周期、及振荡寿命的主要因素有哪些?
答:主要因素有:反应体系的温度、反应物的浓度、离子的活性、催化剂的性质。
2、为什么在实验过程中应尽量使搅拌子的位置和转速保持一致?
答:因为化学振荡反应发生的3个条件之一为:体系必须具有双稳态性,即可在两态间来回振荡。所以应尽量使搅拌子的位置和转速保持一致是体系在一个相对稳定的状态下反应。
