第六单元碳和碳的氧化物知识结构图

碳和碳的化合物专题复习
【复习目标】
知识和能力目标:
1、二氧化碳和碳酸钠的化学性质及应用。
2、构建以二氧化碳为核心的物质转化图。
3、提升学生对知识的整合能力、应用能力。
过程与方法:通过练习复习知识、整合知识、应用知识。
情感目标:渗透元素化合物知识学习的构建观、整合观。
【教学重点】二氧化碳和碳酸钠化学性质和应用;知识网络的构建。
【教学难点】二氧化碳和碳酸钠化学性质的综合应用。
【复习方法】归纳法
【教学准备】PPT课件、学案
【教学环节】
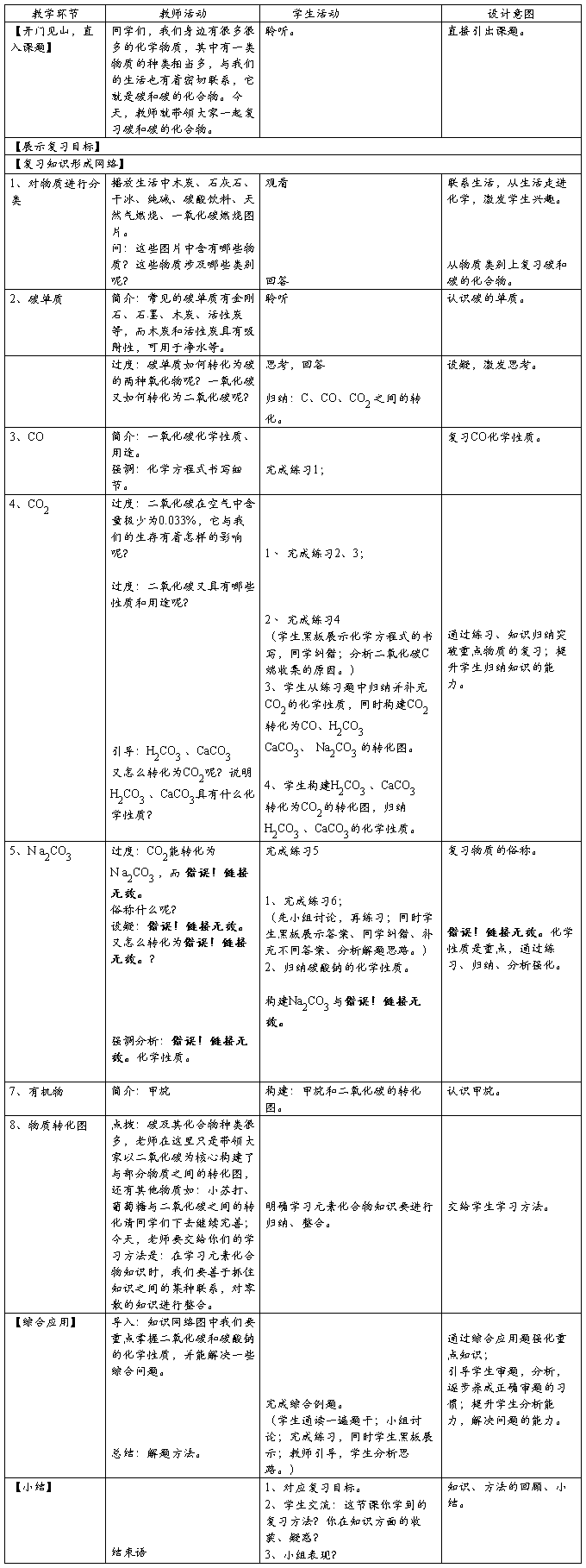
【板书设计】知识网络图。
【教学反思】
【基础练习】
1、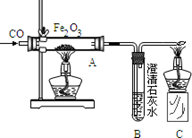 用CO气体来还原氧化铁实验装置如下,请根据题目要求回答下列问题:
用CO气体来还原氧化铁实验装置如下,请根据题目要求回答下列问题:
(1)A装置玻璃管中的现象 反应方程式为_ _____。
(2)C装置是对尾气进行处理,因为尾气中含有有毒气体 。
2、世博“零碳馆”是中国第一座零碳排放的公共建筑,“零碳”中的“碳”主要指( )
A CO B CO2 C CH4 D C
3、空气成分中导致全球气候变暖的主要气体是 ,自然界消耗二氧化碳的主要途径是植物的 作用
4、下图是实验室用碳酸钙与稀盐酸反应制取二氧化碳并验证其性质的实验装置图,试根据题目要求回答下列问题:
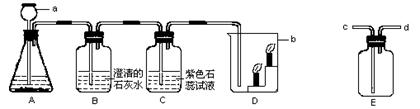
(1)仪器a的名称是 ;装置A中发生的方程式为 ,装置B常用来检验二氧化碳气体,可以观察到澄清石灰水变浑浊,发生的反应方程式 。
装置C中可观察到的现象 反应方程式
(2)装置D中观察到下层蜡烛先熄灭,上层蜡烛后熄灭,说明二氧化碳密度比空气大,它不能燃烧,也不能支持燃烧。由此可知,二氧化碳在生活中可用于 。
(3)实验室用装置E来收集二氧化碳时,二氧化碳应从 (填“c端”或“d端”)通入。
5、下列俗称与化学式不相符的是( )
A 干冰H2O B 烧碱 NaOH C 纯碱Na2CO3 D小苏打 NaHCO3
6、把下列化学方程式补充完整
①加入一种酸
Na2CO3+ = CO2↑+ +
②加入一种碱溶液
Na2CO3+ = CaCO3↓+
③加入一种盐溶液
Na2CO3+ = CaCO3↓+
【综合应用】7、为了通过一些现象说明CO2与NaOH发生了反应,某班同学分两组作了如下探究实验:
(1)把一支收集有CO2的试管倒立在装有饱和NaOH溶液的烧杯中(如图),看到试管内液面上升。这种现象是因为试管内外产生( )
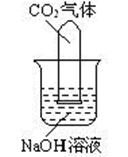
A.温度差 B.重力差 C.压强差 D.浮力差
(2)同学们经过分析讨论,认为实验中产生液面上升现象的原因可能有两种。一种是因为CO2与溶液中的NaOH反应,消耗了CO2,你认为另一种原因是 。
(3)为了进一步证实CO2与NaOH溶液已经发生了反应,他们设计了如下方案:取上述实验后的溶液,第一组同学滴加 ,现象为 ;第二组同学滴加 ,现象为 。他们虽然看到的现象不同,但都可以证CO2与NaOH溶液已经发生了反应。
第二篇:第六单元 碳和碳的氧化物知识盘点
第六单元 碳和碳的氧化物
一、碳的单质
1. 同一种元素可能组成多种单质,__、__和__都是碳元素组成的单质。碳单质的物理性质有差异,是因为 。
2. (1)纯净的金刚石是天然存在的最______的物质。金刚石可以用来做装饰品和__。
⑵石墨很__,有滑腻感,有优良的__。石墨可以用来做____________、电车的“电刷”和___________________。
木炭和___________等主要是由石墨的微小晶体构成的____结构,具有_________能力,食品工业用活性炭制白糖和制作防毒面具都是应用了该能力。
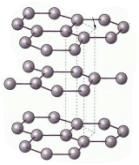
3.(1)下列结构图中,对应的碳单质是(写名称):
① ② ③
———————— ———————— ——————
(2)我国古代书、画家用墨书写或绘制的字画能保存至今,是因
为 。
(3)石墨在一定条件下可转变为金刚石,该变化属于 变化。
(4)构成C60 的微粒是 。构成金刚石和石墨的微粒是 。
二、碳的化学性质
常温下,碳的化学性质很 。
1.碳与氧气
当碳在氧气中充分燃烧,化学方程式是__
当不充分燃烧时,化学方程式是__。
2.碳与金属氧化物(碳具有__________性,用于________工业)
碳与氧化铜:化学方程式是___________________,实验现象:
___________________
碳与氧化铁:化学方程式是
___________________
碳与二氧化碳:化学方程式是___________________,此反应为______反应
课题二 二氧化碳制取的研究
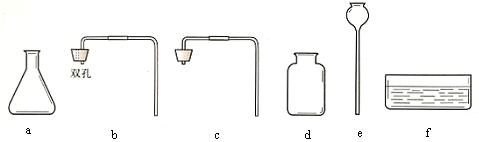
1.实验室里制取气体的装置的确定
发生装置由反应物的________和_________决定,收集装置由气体的_________和__________决定。实验室制取二氧化碳的发生装置选用__________________,这是因为反应物的状态为________,并且反应______加热。收集时选用________原因是二氧化碳密度 _________,_____溶于水。
最后要通过实验来验证制得的气体。例如:如果产生的气体能________________,则证明产生的气体为氧气。如果产生的气体能 ________________,则证明产生的气体为二氧化碳。
2.实验室制取二氧化碳

课题三 一氧化碳和二氧化碳
1.二氧化碳和一氧化碳______________不同,所以_____________不同
2. 二氧化碳 物理性质:一氧化碳 物理性质:
3.二氧化碳的重要性质
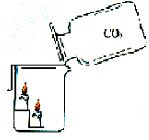
实验①实验现象: ,
此实验说明了
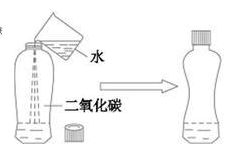
实验②实验现象: ,
此实验说明了
实验③将一个充满二氧化碳的试管倒插在有澄清石灰水的烧杯里,可观察到的现象是 .
实验④向盛放有紫色石蕊试液的试管中通入足量的二氧化碳,溶液变为 色,原因是 (用化学方程式解释);将变色后的溶液加热,溶液颜色 ,其原因(用化学方程式解释) ,说明 .
实验⑤水和干燥的二氧化碳 使紫色石蕊小花变色,而二氧化碳溶于水后 使紫色石蕊小花变色,因为二氧化碳与水反应生成 ,反应方程式
为: . 实验验证:准备一瓶CO2气体,紫色石蕊试纸,水,醋酸。①取适量醋酸滴在紫色石蕊试纸上②将干燥的石蕊试纸放入CO2气体中

③将干燥的石蕊试纸润湿后,再放入CO2气体中。操作顺序是: 在此实验原理的验证中,醋酸使紫色石蕊变红的小实验说明 。
4. 利用二氧化碳____________和____________的性质,可以灭火;绿色植物的
光合作用吸收二氧化碳,二氧化碳在农业上用作___________;在工业上还可用作化工的原料;固体二氧化碳叫__________,__________时吸热,可用作__________和____________。
5. 一氧化碳能______并放出大量的________,火焰呈______色,反应方程式为
________________________;由于一氧化碳是_____味、_____色的气体,并且有________性,为防止煤气泄漏是被及时发现,因此掺入微量难闻的气体。
6. CO表现出___________。一氧化碳和木炭一样能使氧化铜还原成______,同
时生成__________,反应的方程式为____________________,实验现象是
________________________________________,可用于冶金工业中炼铁.
7. 大气中的__________像温室的玻璃或塑料薄膜那样,使地面吸收的太阳光
的热量不易散失,从而使全球变暖,这种现象叫做_____________。为了防止该现象的发生,人类应减少使用________燃料,更多利用清洁能源;大力植树造林,严禁乱砍滥伐森林等。
