有机化学实验报告
姓名: 陈威 学号:PB07206240
实验三 三苯甲醇
一、 目的与要求
1. 了解利用格氏试剂制备三苯甲醇的原理 2. 掌握水蒸气蒸馏的实验方法 二、

实验原理(反应方程式)
1.溴苯、镁和苯甲酸乙酯制三苯甲醇的反应
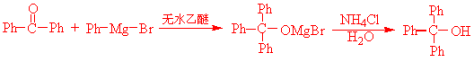
_
PhMg_Br+Ph__C2H5
Ph__OC2HC2H5
Ph__Ph+C2H5MgBr
2.水蒸气蒸馏的原理
由Henry定律可得混合溶液中的组分A的蒸汽压为:
PA=PA×XA (其中PA为纯物质A的蒸汽压)
※
※
由上可知:高沸点的组分在混合溶液中的蒸汽压降低于其纯物质状态下的蒸汽压,使其在较低的温度下就可以沸腾蒸出。
再由Dalton分压定律:P=PA+PB 可知:混合物的沸点低于任意组分的沸点。
由理想气体状态方程:PV=nRT,其中n=m/M.代入得PM=mnRT/V,即物质在混合溶液中的相对质量与它们的蒸汽压和相对分子质量成正比。在实验中,水具有低的相对分子质量和较大的蒸汽压,因此在本实验中正是利用这一原理在常压下将高沸点的组分和水蒸气一起蒸出来。 三、 试剂规格及用量
0.4g镁,2ml溴苯,1ml苯甲酸乙酯,(7+2)ml乙醚(无水),2g氯化铵,1-2粒碘片,1g湿品+5-6ml95%乙醇重结晶
四、 主要试剂及产物的物理常数
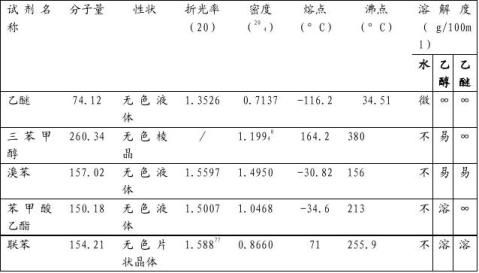
五、 实验装置图
3
有机化学实验报告
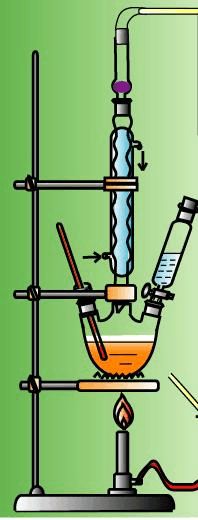
装置一 装置二
六、 实验步骤及现象
1 格氏试剂的制备

2 三苯甲醇的制备
3 水蒸气蒸馏 3

有机化学实验报告
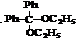
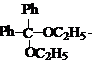

4 物理常数的测定
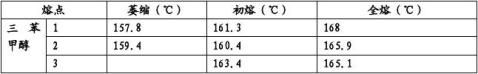
5 三苯甲醇的熔点测定数据记录
七、 实验步骤的图示
三口瓶中放入0.4g镁,一粒碘,磁石→将1/3的混合液倒入→开启搅拌器→将温度保持在32℃逐滴滴加→待加完溶液之后保持温度在34℃,待回流0.5h→从加热套中取出三口瓶让其自然冷却→在滴液漏斗中装入1ml苯甲酸乙酯和2ml无水乙醚→开动搅拌器滴加混合液→滴加完成后在将温度保持在34℃回流0.5h→从加热套中取出三口瓶让其自然冷却→在滴液漏斗中装入2g氯化铵和7-8ml水配成的混合溶液,并逐滴滴入三口瓶中→放置一周→安装蒸馏装置→加热待直型冷凝管口的溶液出现的油状物质较少时停止蒸馏在空气中进行冷却,抽滤的粗样品→将粗产品研碎之后装入三口瓶中,向粗产品中加入8.5ml的95%乙醇,加热搅拌溶解→加入活性碳→趁热进行过滤,放置在空气中让其自然结晶→待结晶完成之后进行过滤→取少量的晶体放到玻片上加热并记录晶体坍塌,初熔和全熔时的温度 八、 实验结果的计算
1三苯甲醇的产率 以粗产品为参考,实验的产率=0.364∕1.223×100%=29.76% 2 三苯甲醇的熔点 熔程=(168-161.3+165.9-160.4+165.1-163.4)/3=4.63℃ 熔点在161.7℃到166.3℃之间 九、 讨论
1 红色的中间产物应为 。此为推断的结果。因为在反应过程中中间产物只有两种:
与 ,显见前者的稳定性远不及后者酮。因为同一个碳原子上连有四个较大的基团空间位阻很大,不稳定。
2 本实验得到的产品的产率不是很高,主要原因有:
Ⅰ)最终抽滤的溶液呈黄色,用水滴加之后发现出现大量白色的物质,这些均是溶解在乙醇溶液中的三苯甲醇这是带来较大偏差的主要原因(三苯甲醇易溶于乙醇); Ⅱ)活性碳的吸附作用
3 由上的分析可知,晶体的析出宜让乙醇慢慢挥发,让其中的三苯甲醇全都析出来以提高产率。 4 至于三苯甲醇熔点的测量,其误差较大。第三组测量时就没有觉察到晶体的坍塌。仪器加热过快带来的直接后果就是显示的温度与实际温度的差距很大。还有在测量时发现加入的固体较多最后发现只有其全熔状态可以比较准确的测量出来,坍塌与初熔的温度较难观测出来。 十、 思考题
1 实验在讲Grignard试剂加成物水解前的各步中,为什么使用的药品仪器均要绝对干燥?采取了什么措施?
答:1)格氏试剂极易水解,因而在制备过程要保证环境的绝对干燥。
3

有机化学实验报告
2)采取的措施:
Ⅰ)在实验之前将制取格氏试剂的仪器进行烘干;
Ⅱ)实验过程中装上干燥器以保证实验过程中空气中水汽不会进入装置内。
2 本实验中溴苯加入太快或一次加入,有什么不好?
答:Grignard反应是一个放热反应,过快加入会造成暴沸的现象。反应开时,调节滴加速度使溶液始终保持的微沸状态。
3 如苯甲酸乙酯和乙醚中含有乙醇,对反应有何影响?
答:乙醇分子中有活泼的羟基,不利于格氏试剂的生成。
4 用混合溶剂进行重结晶时,何时加入活性碳脱色?能否加入大量的不良溶剂,使产物全部析出?抽滤后的结晶应该用什么溶剂洗涤?
答:1)待溶质完全溶解时,加入补充的乙醇后再加活性炭,这样既可以避免溶质未完全溶解时,活性炭会大量吸附,又可以避免活性炭引起暴沸;
2)是可以加入不良溶剂。本实验中是加入水,但是这样做会破坏晶体的晶形。
3)抽滤之后应仍用乙醇溶液进行洗涤。
3
第二篇:三苯甲醇(方法二)
实验三 三苯甲醇(方法二)
实验目的:
1. 了解Grignard试剂的制备、应用和进行Grignard反应的条件; 2. 巩固搅拌,回流,蒸馏(包括低沸物蒸馏)等操作; 实验原理:
Br
+
Mg
MgBr
MgBr
+
无水乙醚
COMgBr
OMgBr
COH
实验仪器:(磨口仪器需预先干燥)
50mL三颈烧瓶,恒压滴液漏斗,回流冷凝管,量筒(10mL , 50mL),磁力搅拌器,CaCl2干燥管,抽滤瓶,布氏漏斗,烧杯,玻棒. 实验药品:
0.5g(0.02mol)镁屑,2.2mL(0.02mol , 3.2g )溴苯(要求新蒸),3.7g(0.02mol)二苯甲酮,30mL无水乙醚,4gNH4Cl,一小粒I2 实验装置:
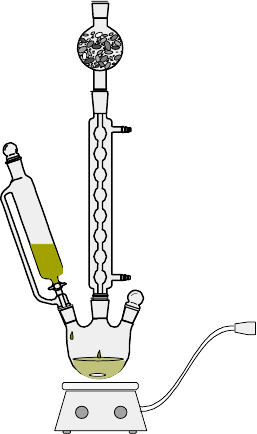
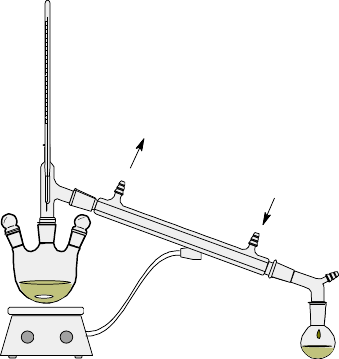
实验步骤:
(一) 苯基溴化镁的制备(所有的仪器都必须干燥)
1. 在50mL三颈烧瓶中装上磁力搅拌器,回流冷凝管(回流冷凝管上端装上CaCl2干燥管),恒压滴液
漏斗(活塞涂凡士林,但不能多涂,以免堵住小孔);
2. 向三颈烧瓶加入0.5g(0.02mol)剪细的镁屑(注意:一定要剪细,大约1~2mm宽一段,否则反
应速度很慢,而且要刮去镁表面的氧化层,否则反应不能进行)和一小粒I2(大约半粒米大小),向恒压滴液漏斗中加入2.2mL溴苯和10mL无水乙醚的混合液,(先放入1/3左右的混合液,用手温热三口瓶,待I2的黄色消失后,开动磁力搅拌器,不要打开其加热开关);
3. 将恒压滴液漏斗中的混合液慢慢滴加到三颈烧瓶中,保持三口瓶中的乙醚呈微沸状态。加完后,
用50~60℃的热水加热回流(同时进行适度的加热)30min(镁条差不多消失),这样制成了Grignard试剂(溶液呈暗褐色,让其冷却,同时用水浴锅装一些冷水冷却磁力搅拌器的加热盘);
4. 往制备好的Grignard试剂中加入10mL无水乙醚;
(二) 三苯甲醇的制备
1. 在干燥的小锥形瓶中加入3.7g二苯甲酮,10mL无水乙醚,盖上塞子,轻轻摇动使其溶解,再将
该溶液转移到恒压滴液漏斗中;
2. 在冷水浴冷却下和搅拌下滴加二苯甲酮的乙醚溶液(可能会出现固体,实验照常进行),加完后,
用50~60℃的热水加热回流(同时进行适度的加热)0.5h;
3. 在冰浴下加入4gNH4Cl和15mL水配成的饱和溶液,搅拌使固体全溶(将溶液转移到250mL的三口
瓶中,改成水蒸气蒸馏);
4. 常压蒸掉乙醚(同时用酒精灯加热水蒸气发生器),(乙醚蒸完后,夹上弹簧夹)进行水蒸汽蒸馏
(除去未反应的溴苯,联苯等副产物);
5. 冷却,抽滤固体,晾干,称重,计算产率。

