实验十一 肉桂酸的制备
一、实验目的:
1.了解肉桂酸的制备原理和方法
2.掌握回流、热过滤及水蒸汽蒸馏等操作
二、实验原理:
芳香醛与含有α-氢的脂肪族酸酐在碱性催化剂的作用下加热,发生缩合反应,生成芳基取代的α,β不饱和酸。这种缩合反应称为Perkin 反应。本实验将芳醛与酸酐混合后在相应的无水羧酸盐存在下加热,可以制得α,β不饱和酸。
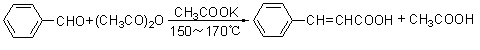 按照Kalnin所提出的方法,用碳酸钾代替Perkin反应中的醋酸钾,反应时间短,产率高。
按照Kalnin所提出的方法,用碳酸钾代替Perkin反应中的醋酸钾,反应时间短,产率高。
三、实验药品:
苯甲醛3mL(3.15g,0.03mol),碳酸钾4.2g(0.03mol),乙酐8mL(8.64g,0.084mol),饱和碳酸钠溶液,活性碳,浓盐酸。
四、实验仪器:
三口瓶,温度计,空气冷凝管,瓶塞,滴管,水蒸汽蒸馏装置,直形冷凝管,蒸馏头,接引管,锥形瓶,烧杯,玻璃棒,pH试纸,布氏漏斗,抽滤瓶。
五、实验步骤:
在250mL三口瓶中放入3mL(3.15g,0.03mol)新蒸馏过的苯甲醛[1]、8mL(8.64g,0.084mol)新蒸馏过的醋酐[2]以及研细的4.2g无水碳酸钾[3]。三口瓶,一口装温度计,一口装回流冷凝管,一口用塞子塞上,上加热[4]回流30min。由于有二氧化碳放出,初期有泡沫产生。
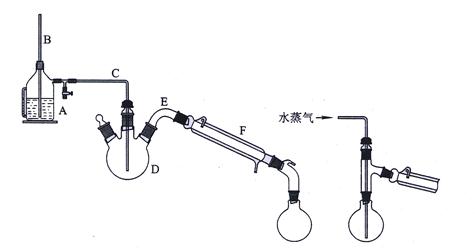
反应结束后,待反应液稍冷向反应液中加入20mL冷水,振荡下慢慢加入饱和碳酸钠溶液[5](注意有大量的CO2气体产生,不要冲料),调节反应液呈弱碱性pH=9~10。用二口瓶作为水蒸汽发生器,如图安装水蒸汽蒸馏装置,进行水蒸汽蒸馏,蒸出未反应的苯甲醛,直至馏出液无油珠澄清为止。
待三口烧瓶内的剩余液稍冷,加入半匙活性碳,在石棉网上煮沸2~3分钟,趁热进行抽滤,滤液转移到烧杯中。将滤液用浓盐酸酸化(不易过快,否则晶型过细),使呈明显酸性(pH=3)[6],用冷水浴充分冷却,待结晶完全析出后进行抽滤,用少量冷水洗涤晶体,挤压除去水份。
产品在水中或30%乙醇中重结晶[7]。产品包在方形滤纸中,自然晾干,下次实验称重,计算产率。
肉桂酸为无色晶体,有顺反异构体,通常以反式异构体形式存在,熔点135~136℃,沸点300℃,d 1.245 。
附注
[1] 苯甲醛久置会氧化为苯甲酸,这不但影响反应的进行,而且苯甲酸混在产品中不易除干净,将影响产品的质量。故实验前要重新蒸馏,收集170~180℃馏分供使用。
[2] 乙酸酐久置会吸水和水解为乙酸。故实验前要重新蒸馏,收集137~140℃馏分。
[3] 碱性催化剂通常用相应酸酐的羧酸钠或钾盐,由于催化剂的碱性较弱,因此反应时间较长,反应温度较高。使用无水碳酸钾反应时间短产率高。
[4] 开始加热不要过猛,以防醋酸酐受热分解而挥发,白色烟雾不要超过空气冷凝管高度的1/3。反应温度不易过高,如反应温度过高(200℃左右),会生成树脂状物质。
[5] 此时不能用氢氧化钠代替碳酸钠,否则会发生坎尼扎罗反应,使未反应的苯甲醛变为苯甲酸,影响产品质量。
[6] 刚果红试纸变蓝。
[7]也可用其它溶剂进行重结晶,参见下表:

思考题
1.苯甲醛和丙酸酐在无水丙酸钾存在下相互作用得到什么产物?写出反应式?
2.为什么不能用氢氧化钠代替碳酸钠溶液来中和水溶液?
3.水蒸汽蒸馏的目的是什么?
第二篇:实验四 肉桂酸的制备及水蒸气蒸馏
实验四 肉桂酸的制备及水蒸气蒸馏(6学时)
[实验目的] 1.了解肉桂酸的制备原理和方法。
2.掌握回流,水蒸汽蒸馏等操作。
[实验药品]新蒸馏过的苯甲醛1ml,新蒸馏过的醋酐2.7ml,研细的无水碳酸钾1.4克,10%NaOH溶液6.7ml,浓盐酸,刚果红试纸。
[仪器设备] 普通抽滤装置、水蒸气蒸馏装置、标准磨口仪
[实验原理] 1.水蒸气蒸馏原理:当有机物与水一起共热时,整个系统的蒸汽压根据分压定律,各组分蒸汽压之和, 即P=P(H2O)+PA当总蒸汽压(P)与大气压力相等时,则液体沸腾。显然,混合物的沸点低于任何一个组分的沸点。有机物可以在比其正常沸点低得多的温度,而且在低于100℃的温度下随蒸汽一起蒸馏出来。
2. 肉桂酸的制备原理:
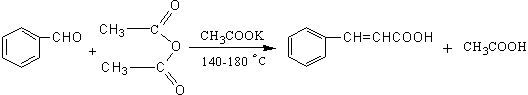
[实验步骤] 按图安装装置
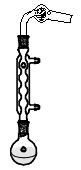
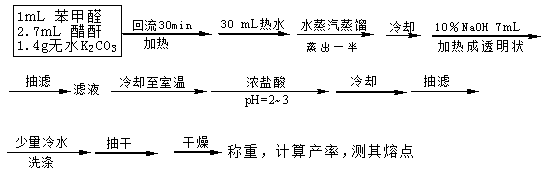
[注意事项]
1.苯甲醛,醋酐使用前重新蒸馏。
2.回流所需的仪器必须干燥。
3.回流完毕后,不必冷却,且加热水,否则固体难以捣碎。
4.利用水蒸气蒸馏的物质必须以下条件:(1)不溶或难溶于水;(2)与水煮沸很久不发生化学反应;(3)在100℃时至少具有10mmHg压力.[习题] 课后第1,2 题。
