阿司匹林的制备
实验名称:
班 级:
姓 名:
实 验 报 告
第二篇:阿司匹林铜制备实验报告.doc
氢氧化钠对阿司匹林铜制备的影响
一、实验目的
1.了解阿司匹林铜的一般特性。
2.掌握水浴加热、结晶、减压过滤和晶体洗涤等基本操作。
3.掌握碘量法测定铜(Ⅱ)的方法和原理。
二、实验原理
阿司匹林铜为亮蓝色结晶粉末,无味,无吸湿、风化、挥发性,不溶于水、醇、醚及氯仿等溶剂中,微溶于二甲亚砜。受热不稳定,成一种浅绿色混合物。因能与氨水反应而溶于氨水,与强酸反应使阿司匹林和铜离子解离出来。
1.阿司匹林铜的制备
本实验采用阿司匹林、氢氧化钠、五水硫酸铜为原料合成阿司匹林铜,反应方程式如下:
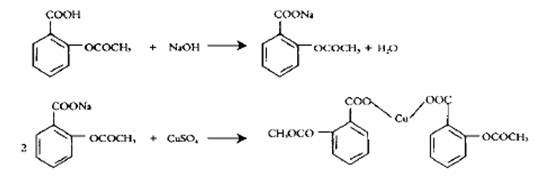 阿司匹林与硫酸铜的摩尔配比为2:1。配位方式属于桥式双齿配位。
阿司匹林与硫酸铜的摩尔配比为2:1。配位方式属于桥式双齿配位。
制备阿司匹林铜时,NaOH用量不同,阿司匹林铜的产率和纯度均不同。本次实验NaOH用量分别为:0.8、0.9、1.0、1.1。比较不同NaOH的用量时的反应现象及产品的产率和纯度,确定制备阿司匹林铜时合适的NaOH用量。
2.阿司匹林铜中铜含量的测定
阿司匹林铜中铜含量的测定可用碘量法测定。在酸性溶液中加热,阿司匹林铜解离出Cu2+。在微酸性溶液中(pH=3~4),Cu2+与过量I-作用,生成难溶性的CuI沉淀和I2,其反应式为: 2Cu2+ + 4I- = 2CuI ↓+ I2
生成的I2用Na2S2O3标准溶液滴定,以淀粉溶液为指示剂,滴定至溶液的蓝色刚好消失即为终点。反应式为: I2 十2S2O32- = 2 I- + S4O62-
由于CuI沉淀表面吸附I2致使分析结果偏低,为此,可在大部分I2被Na2S2O3溶液滴定后,溶液由棕色变为浅黄色时,加入KSCN,使CuI(Ksp=2.1´10-12 )沉淀转化为溶解度更小的CuSCN(Ksp=4.8×10-15 )沉淀,把吸附的碘释放出来,从而提高测定结果的准确度。
CuI + SCN- = CuSCN¯ + I-
根据Na2S2O3标准溶液的浓度及消耗的体积计算出试样中铜的含量。
Cu%=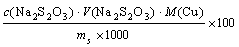
为了防止I-的氧化(Cu2+催化此反应),反应不能在强酸性溶液中进行。由于Cu2+的水解及I2易被碱分解,反应也不能在碱性溶液中进行。一般控制溶液pH3~4弱酸介质中进行。
三、主要仪器设备及试剂
仪器:电炉,烧杯,100ml容量瓶,胶头滴管,量筒,玻璃棒,表面皿,布氏漏斗,吸滤瓶,抽滤泵,分析天平,药匙,细口瓶,锥形瓶。
试剂:阿司匹林(s),NaOH(s),邻苯二甲酸氢钾(s),酚酞,无水乙醇,五水硫酸铜,硫代硫酸钠标准溶液,3mol/L硫酸溶液,6mol/L盐酸溶液,碘酸钾(s),碘化钾(s),硫氰化钾(s),0.5%淀粉溶液。
四、实验步骤
1.阿司匹林铜的制备
步骤一:称取阿司匹林4.50g  , 加入250mL的烧杯中
, 加入250mL的烧杯中 ------à加入95%乙醇25mL,此时不溶解------à 称取NaOH 固体1.00g,加入100mL烧杯中
------à加入95%乙醇25mL,此时不溶解------à 称取NaOH 固体1.00g,加入100mL烧杯中 ------à加20 mL蒸馏水溶解成溶液
------à加20 mL蒸馏水溶解成溶液 ,并冷却至室温------à
,并冷却至室温------à 将NaOH溶液加入到阿司匹林的乙醇溶液中,边加边搅拌,至阿司匹林全部溶解
将NaOH溶液加入到阿司匹林的乙醇溶液中,边加边搅拌,至阿司匹林全部溶解
步骤二:称取五水硫酸铜2.76g  ,加入另一250mL的烧杯中
,加入另一250mL的烧杯中 ------à加入100ml蒸馏水,搅拌溶解
------à加入100ml蒸馏水,搅拌溶解 ------à将硫酸铜溶液用滴管滴加到阿司匹林钠溶液中,
------à将硫酸铜溶液用滴管滴加到阿司匹林钠溶液中, ,边加边搅拌,加完持续搅拌10分钟,生成阿司匹林铜沉淀------à 水浴加热,控制温度15-20摄氏度,持续搅拌10min------à生成阿司匹林铜沉淀------à抽滤沉淀,先
,边加边搅拌,加完持续搅拌10分钟,生成阿司匹林铜沉淀------à 水浴加热,控制温度15-20摄氏度,持续搅拌10min------à生成阿司匹林铜沉淀------à抽滤沉淀,先
用蒸馏水洗3遍、再用10mL无水乙醇分3次洗沉淀
 ------à沉淀自然晾干,即得阿司匹林铜亮蓝色结晶粉末。
------à沉淀自然晾干,即得阿司匹林铜亮蓝色结晶粉末。

 2.阿司匹林铜中铜含量的测定
2.阿司匹林铜中铜含量的测定
步骤一:称取1.0g阿司匹林铜 ------à加入到250mL的锥形瓶中
------à加5mL 3mol/L H2SO4,蒸馏水30mL------à加热煮沸3min------à充分反应
后,加蒸馏水15mL,摇匀------à冷却到室温------à加入1.5 gKI ,摇匀
步骤二: 用0.1mol/L Na2S2O3标准溶液滴定至溶液变浅黄色------à加入100g/L KSCN试剂10mL,并加入2mL0.5%淀粉溶液------à
用0.1mol/L Na2S2O3标准溶液滴定至溶液变浅黄色------à加入100g/L KSCN试剂10mL,并加入2mL0.5%淀粉溶液------à 继续用0.1mol/L Na2S2O3标准溶液滴
继续用0.1mol/L Na2S2O3标准溶液滴
定至蓝色刚好消失为终点(10 S内不返回蓝色)------à记录消耗的Na2S2O3溶液体积------à
平行滴定三次,计算产品中铜的含量。
五、实验数据及处理
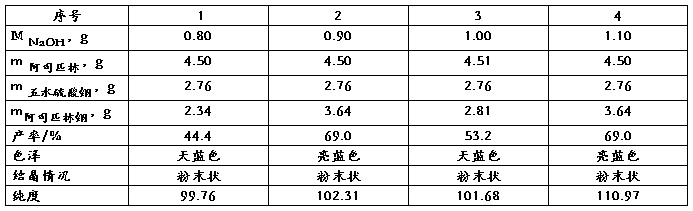
表格 1 NaOH用量对阿司匹林铜制备的影响(25.4 )
)
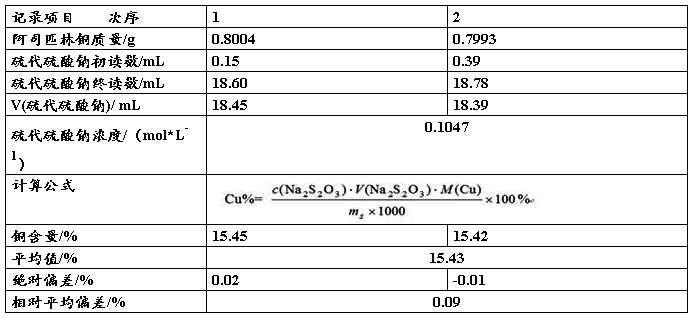
表格 2 阿司匹林铜中铜含量的测定
六、结论及分析
(1) 由实验数据得,阿司匹林铜的产率不高,可见有机反应不同于无机,反应复杂,副反应较多,严重影响产率。
(2) 氢氧化钠用量会影响阿司匹林铜的产量和纯度。NaOH用量为0.90g和1.10g的产率比较高,但1.0g产率反而不高。一般来说,通过条件实验,可确定NaOH用量对阿司匹林铜的产量和纯度的影响应类似一条钟形曲线,存在最适NaOH用量。可能用量为1.00g的同学存在操作失误导致结果偏低,也可能0.90g和1.10g同学操作失误导致结果偏高,但可以肯定氢氧化钠用量确实会影响阿司匹林铜产率,这说明NaOH的量并非越多越好。乙酰水杨酸在氢氧化钠的介质中很易水解成水杨酸,温度高,水解更快,反应液放置的时间越长,水解程度越大,因而NaOH用量增加反而会造成产率的下降。
(3) 阿司匹林铜含量的测定结果显示纯度大于100%,存在明显错误。经过分析实验过程和实验原理,可能的原因有以下几个方面:一、硫酸铜过量导致结晶时,晶体表面或内部附着了少量硫酸铜,洗涤时没有完全洗净带入了铜,导致最后铜含量测定结果偏大; 二、阿司匹林铜中铜含量测定实验时,滴定终点很难把握好,导致滴定过量,出现误差;三、反应可能形成了Cu一配位产物
七、实验改进与建议
(1) 在搅拌过程中溶液中的碘易被空气中的氧气反应导致硫代硫酸钠滴定用量偏少,进而导致滴定结果偏低,可在实验时使用碘量瓶
(2) 酸化时使用硫酸而不用盐酸,是由于Cl-1与Cu2+易形成配离子形成实验干扰。
(3) 试剂称取时可以使用分析天平,并且使用差减法,减少试剂在称量过程中与空气的反应,减小试剂变质引起的误差。
(4) 碘量法适合在低温中(<25摄氏度)进行
(5) 作为探究性实验,应更加注重学生在实验过程中对实验中误差及反常现象的思考,而不是实验是否符合常理。
八、思考题
1、阿司匹林与氢氧化钠反应时为什么在较低温度下进行,且过程快点更好?
答:乙酰水杨酸在氢氧化钠的介质中很易水解成水杨酸,温度高,水解更快,反应液放置的时间越长,水解程度越大。
2、那些原因引起产率的差异,怎样提高产率?
答:乙酰水杨酸在氢氧化钠的介质中很易水解成水杨酸,温度高,水解更快,反应液放置的时间越长,水解程度越大。阿司匹林的中和反应尽量在低温下快速进行。
阿司匹林铜的形成时,反应的时间太短,转化不好,产率低,杂质含量高,所以阿司匹林铜生成时搅拌的时间要适当长。
3、测定铜含量时,采取了那些措施来提高测定的准确度?
答:(1)加入过量的KI(配位剂、沉淀剂、还原剂) ;
(2)由于CuI沉淀强烈地吸附I2,使测定结果偏低。加入KSCN,使CuI转化为溶解度更小的CuSCN沉淀:CuI+ SCN? CuSCN? + I-?
但KSCN只能在接近终点时加入,否则SCN一可直接还原 Cu2+而使结果偏低;
5. 为防止Cu2+水解,必须在H2SO4溶液中进行(pH值在3~4之间),不能用HCl,Cu2+ 易与Cl-形成配位化合物
4、间接碘量法误差的主要来源及减免方法?
答:(1)主要来源: I2的挥发和I-的氧化。
(2)减免的方法: 防止碘的挥发: a. 加入过量的KI, 使用碘量瓶;b. 滴定时不要剧烈的摇动。 防止碘离子的氧化: 由于光照和酸度的提高会加快氧化的速度,因而:a. 反应时避光 b. 滴定前控制好酸度。
5. 间接碘量法滴定时,溶液必须控制在中性或弱酸性进行,为什么?
答:必须控制在中性或弱酸性溶液中进行的原因:
在碱性溶液中:S2O3- + 4I- +10OH-  2SO4- +8I- + 5H2O
2SO4- +8I- + 5H2O
在强酸性溶液中:S2O3- + 4H- 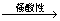 SO2 + S↓+ H2O
SO2 + S↓+ H2O
九、学生感言
