HPV操作步骤详细
一、 试剂配制区、样品处理区、核酸扩增区。
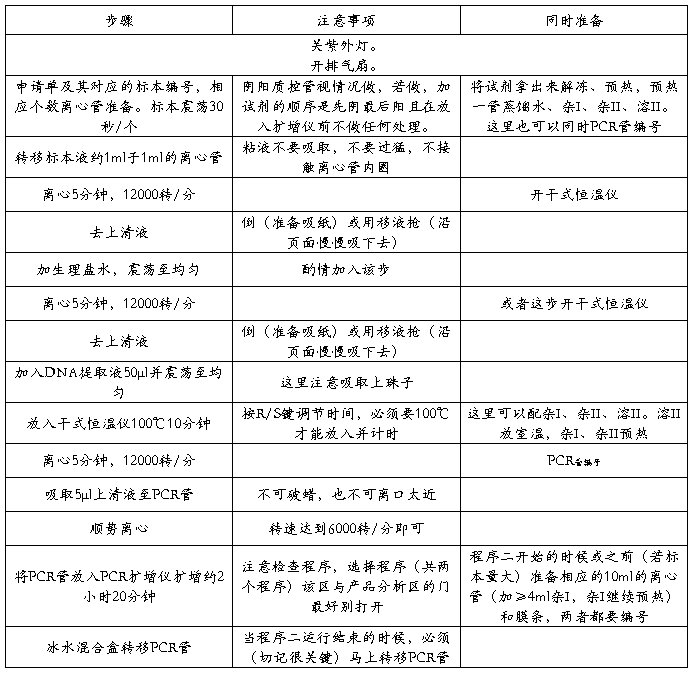
二、 产物分析区。
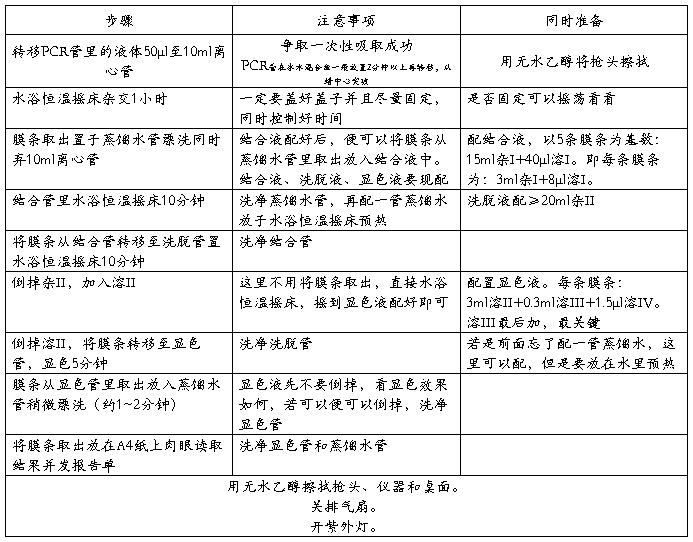
第二篇:PCR HPV-DNA荧光定量检测标准操作程序

1.目的:明确高危型人乳头瘤病毒核酸定量检测的操作规程,指导检验人员正确进行巨细胞病毒核酸定量的检测。
2.适用范围:
2.1适用于进行高危型人乳头瘤病毒核酸定量检测的检验人员。
2.2适合仪器:LightCycler480型核酸扩增荧光检测仪
2.3方法原理:采用PCR方法结合荧光探针的扩增技术
2.4样品要求:宫颈脱落细胞
3.职责:实验操作人员应严格按操作规程进行实验。
4.试剂来源:潮州凯普生物化学有限公司高危型人乳头瘤病毒核酸定量检测试剂盒。
5.质控物:阴性、阳性对照及阳性参控品系列均来源于试剂盒
6.标准操作:
6.1 试剂准备(在试剂准备区操作)
6.1.1将试剂盒及其它所需试剂置室温解冻(临用前取出,用后立即放回冰箱,反复冻融不可超过三次),取出PCR MIX,室温下避光解冻,上下颠倒混匀后,8000转/分钟10s从试剂盒中取出DVA聚合酶,8000转/分钟lOs。
6.1.2根据当次实验标本量,取出相应试剂(1管=17.5ulPCR MIX +0.5ul DVA聚合酶)总的需求量于一管中(其余随即放回原温度保存),如所需要的管数为n (n=标本数+1空白管对照+1管阳性对照) 取PCR反应管转移至样本制备区。
6.2样本处理(在样本处理区进行)
6.2.1.取宫颈脱落细胞样本0. 5ml~1ml(如果细胞数量少可以加大体积到2m1)
6.2.2. 13000转/分钟离心1分钟
6.2.3.弃上清,加入0.5m1细胞保存液重悬细胞
6.2.4. 13000转/分钟离心1分钟,尽量弃干净上清
6.2.5.每样本加入50ul细胞裂解液,充分振荡重悬细胞,煮沸10分钟。
6.2.6. 13000转/分钟离心10分钟,保留上清备用(上清中为释放的DNA)。
6.2.7取上清2.0ul作为PCR扩增的模板,其余保存于一20℃
6.2.8在对应的PCR反应管中分别加入2ul处理好的样本DVA,空白对照、阳性对照,盖
紧管盖,稍做离心(反应总体积为2o u 1/人份,每次反应需要设置一个阳性对照以及一个空白对照)。转移到检测区,放入相应的荧光PCR检测仪内,记录样本摆放顺序
6.3 PCR扩增(在扩增区操作)
6.3.1打开稳压器电源,再打开计算机电源。
6.3.2 打开扩增仪电源,按仪器操作规程进入扩增循环条件设定。
6.3.3设置四种荧光检测通道的报告荧光、淬灭荧光;Passive Reference选择none(见表1)

表1: 设置四种荧光检测通道

6.3.4将循环条件设定为
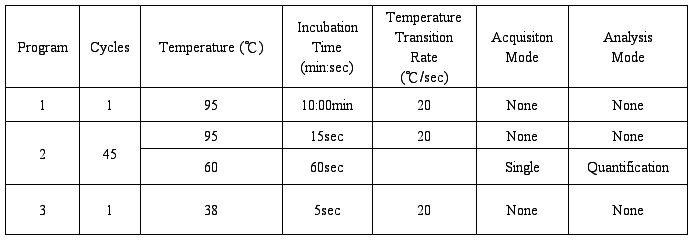
6.3.5检查反应管是否盖紧,以免荧光物质泄漏污染仪器。
6.3.6将待反应的PCR反应管放入扩增仪中,并根据实际情况和仪器操作规程在程序中设定好样孔位置。
6.3.7按仪器操作规程开始循环。
6.3.8扩增结束后取出PCR反应管,关闭扩增仪电源,反应管直接放入焚烧垃圾桶内。

6.3.9分析数据,在Analysis Notes窗口中注明检测基线值、试剂批号、阳参批号等相关信息,进行结果分析。
6.3.10关闭计算机。
6.4检验结果判断:
6.4.1基线,阂值的设定:基线的确定为:取3-15个循环的荧光信号:阈值设定:使阈值线超过正常阴性对照品扩增曲线(无规则的噪音线)的最高点,且Ct值为Under
6.4.2质控对照
1阴性对照Ct值均应显示为Undet
2阳性对照Ct值≤36
3内对照β-globin在Cy5通道Ct值≤40
符合以上三个条件,此反应是为有效
6.4.3结果判断
1样本在FAM、HEX、ROX通道Ct值显示为Undet,内对照β-globin在Cy5通道Ct值≤40,判断为阴性
2样本在FAM、HEX、ROX通道Ct值≤40, 内对照β-globin在Cy5通道Ct值≤40判断为阳性
3若样本在FAM、HEX、ROX通道40<Ct值<45的样本建议重做,重做结果Ct值<40者为阳性,否则为阴性
7.支持性文件:
7.1 《高危型人乳头状瘤病毒核酸检测试剂盒(PCR一荧光探针法)》说明书(潮州凯普生物化学有限公司)
7.2 检测结果报告程序。
7.3 LightCycler480型核酸扩增荧光检测仪说明书
8.此标准操作变更程序:如果本操作程序使用者在实际工作中发现其存在问题,则应向科室负责人提出,科室负责人则召集所有与本程序有关的人员讨论,以决定是否需要变更本程序
