第十二章 血液毒理学 (以简答题为主)
1、对红细胞生成的影响
 :红细胞的生成依赖于血红蛋白的高速合成;
:红细胞的生成依赖于血红蛋白的高速合成;
 血红蛋白的合成依赖于珠蛋白链和血红素两部分协调生成;
血红蛋白的合成依赖于珠蛋白链和血红素两部分协调生成;
 外源毒物通过影响珠蛋白链合成和血红素合成,导致血红蛋白合成减少引起贫血。
外源毒物通过影响珠蛋白链合成和血红素合成,导致血红蛋白合成减少引起贫血。
主要有铁粒幼细胞性贫血、巨幼细胞性贫血、再生障碍性贫血、纯红细胞再生障碍性贫血、继发性贫血……
2、铁粒幼细胞性贫血:
l 是由血红素合成障碍引起的不同程度小细胞低色素性贫血;
l 红细胞铁利用障碍性贫血。
特点:1、血清铁蛋白↑、骨髓外铁及内铁↑,出现环形铁粒幼细胞;
2、乙醇、氯霉素、异烟肼、锌中毒、铅中毒等可干扰血红素合成过程而导致铁粒幼细胞性贫血。
3、巨幼细胞性贫血
l 叶酸或维生素B12缺乏导致;
l 维生素B12缺乏:如秋水仙碱、新霉素、乙醇…
l 叶酸缺乏:如苯妥英、苯巴比妥、磺胺嘧啶、卡马西平…
4、再生障碍性贫血(Aplasia Anemia
 定义 :由于各种原因引起的造血干细胞数量和功能异常,以致全血细胞(红细胞、血水板、白细胞)减少而引起的一种综合征。
定义 :由于各种原因引起的造血干细胞数量和功能异常,以致全血细胞(红细胞、血水板、白细胞)减少而引起的一种综合征。
 各种病因→造血干细胞损伤 →骨髓增生不良 →外周血全血细胞减少(Pancytopenia),
各种病因→造血干细胞损伤 →骨髓增生不良 →外周血全血细胞减少(Pancytopenia),
 临床表现为贫血,出血和感染发热。
临床表现为贫血,出血和感染发热。
5、毒性高铁血红蛋白血症
Ì 正常人血红蛋白分子含二价铁 (Fe2+),与氧结合为氧合血红蛋白。当血红蛋白中铁丧失一个电子,被氧化为三价铁 (Fe3+) 时,即称为高铁血红蛋白 (简称Met Hb)。
Ì 正常人血Met Hb仅占血红蛋白总量的0.5%~2%,并且较为恒定。当血中Met Hb量超过这个数值时,称为高铁血红蛋白血症 (methemoglobinemia)。
Ì 症状为呼吸困难,发绀 ;严重时可致器官缺氧受损, 智力受影响等后遗症 。
6监测内容:
Ì 红细胞参数:红细胞、血红蛋白、血细胞压积、平均血细胞容积、平均血红蛋白浓度;
Ì 白细胞参数:白细胞绝对数、分类计数;
Ì 血小板计数、凝血实验、外周血细胞形态、骨髓细胞学、组织学检查;
Ì 潜在血液毒性检查:网织红细胞计数、海因茨体制备、红细胞渗透脆性试验等。
第十三章 免疫毒理学
1、外源性化学物质对免疫系统的影响:
外源性化学物质对免疫系统的影响表现在三个方面,即免疫抑制、超敏反应和自身免疫反应。
2、免疫抑制
外源化学物免疫抑制的主要表现:外源化学物免疫抑制的结果是宿主抵抗力降低,主要表现为抗感染能力降低和肿瘤易感性增加。
3、超敏反应(hypersensitivity)
亦称变态反应(allergy)指已致敏的机体再次接触相同抗原后,发生的一种以生理功能紊乱或组织细胞病理损伤为主的异常特异性免疫应答。
4、(三)自身免疫
自身免疫是指机体免疫系统对自身成分发生免疫应答的现象,自身免疫性疾病是因机体免疫系统对自身成分发生免疫应答而导致的疾病。
第十四章 生殖毒理学
1、外源化学物对生殖发育的影响
Ø 干扰生殖发育的任何环节,并造成损害作用。(铅、镍、镉中毒,农药、有机化合物与香烟等)
Ø 可以通过对内分泌系统,特别是对性腺的作用,发生间接的影响。
Ø 神经系统对内分泌功能也有调节作用,通过下丘脑-垂体-睾丸轴(下丘脑-垂体-卵巢轴)两条途径作用于生殖发育过程 。
2、生殖毒理学(reproductive toxicology)主要研究外源化学物对生殖细胞发生、卵细胞受精、胚胎形成、妊娠、分娩和哺乳过程的损害作用及其评定,评定方法即为生殖毒性试验。
发育毒理学(developmental toxicology)主要研究外源化学物对胚胎发育、胎仔发育以及出生幼仔发育的影响及其评定,评定方法称为发育毒性试验,其中主要为致畸试验。
3、生殖毒性的评价
v 观察指标:
Ö 受孕率(%):反映雌性动物生育能力以及雌性动物受孕情况
Ö 正常分娩率(%):反映雌性动物妊娠过程是否受到影响
Ö 幼仔出生存活率(%):反映雌性动物分娩过程是否正常
Ö 幼仔哺育成活率(%):反映雌性动物授乳哺育幼仔的能力
Ö 除上述4个指标外,还应该注意出生幼仔是否有畸形存在,对死亡的幼仔应进行畸形检查,可为下一步致畸试验提供参考
第十五章,神经与行为毒理学
(一)神经递质代谢的改变
可卡因:抑制突触前膜摄取单胺类神经递质的酶,增加突触间隙多巴胺/去甲肾上腺素的浓度引起中毒。
有机磷:抑制乙酰胆碱酯酶活性,造成突触间隙乙酰胆碱的大量蓄积引起中毒。
(二)干扰神经递质的储存和/或释放
| 利血平:干扰储存→递质耗竭
| 麻黄碱:促进儿茶酚胺类递质释放
| 肉毒杆菌毒素:抑制神经肌肉接头处突触前膜释放乙酰胆碱,引起迟缓性瘫痪。
| 破伤风毒素:阻断抑制性神经元释放氨基酸递质,导致肌肉强直。
毒物可与受体分子发生相互作用,产生不同的生物学效应:
(1)毒物分子可模拟内源性配体,激活相应的受体,引起激动剂样的作用;
(2)毒物分子可能结合于受体,但并不引起激活效应,而是阻断内源性配体的作用(拮抗作用);
(3)毒物可能对受体产生变构效应。结合与受体大分子的相邻部位,引起构象变化而影响复合体与神经的结合。
第十六章 呼吸毒理学
1、外源毒物对呼吸系统损害的类型:
急性:表现为呼吸道粘膜的刺激作用和急性肺炎、肺水肿
慢性:表现为肺气肿、肺纤维化、哮喘、肺肿瘤等
2、一、急性损伤
(一)呼吸道损伤
急性刺激:刺激性气体如甲醛、氨、氯气等水溶性气体导致;
急性炎症:水溶性化学物易引起上呼吸道炎症;脂溶性毒物可引起支气管和细支气管炎症;某些过敏原、有毒颗粒以及感染性微生物可进入到肺泡引起肺泡炎或肺炎。
(二)坏死:吸入毒性强的毒物或吸入的毒物量大,引起气管组织的坏死。
(三)肺水肿(肺急性损伤的标志)
部位:呼吸膜 机制:肺泡-毛细血管屏障通透性增加
后果:肺结构和功能的急性损伤;水肿消退后遗留的异常。评价指标:肺含水量的测定
3、二、慢性损伤
(一)肺纤维化
| 病理特征:肺泡壁(包括呼吸性细支气管)弥漫性慢性炎症和间质纤维化
| 部位:肺泡间质;小气道
(二)肺气肿
病理特征:肺气肿是指终末细支气管 (呼吸细支气管、肺泡管、肺泡囊和肺泡)的管腔异常增大,弹性减退,过度膨胀,并伴有腔壁的破坏性改变而无明显纤维化的一种病理状态。
部位:终末细支气管 ;管腔
多见于吸烟引起
(三)哮喘:气管、支气管对刺激因子高度敏感,导致反复发作的气短、呼吸困难、哮鸣等气道梗阻的表现。
(四)肺癌
| 可能机制:1)活化的致癌剂或其代谢产物引起DNA损害;
2)活性氧引起DNA损害
| 研究手段:吸烟、氡气;石棉纤维、砷、镉等;硅、人造纤维、甲醛
4、代表性肺毒性药物和毒物
(1)博来霉素
l 肿瘤化疗药;可引起急性化学性肺炎和慢性肺纤维化,甚至呼吸衰竭
l 损害结果:毛细血管内皮细胞和Ⅰ型肺泡细胞的坏死,形成水肿和出血,迟延性Ⅱ型肺泡上皮细胞的增殖,最后肺纤维化使肺泡壁增厚
l 可能机制:肺缺少使博来霉素灭活的酶
(2)环磷酰胺
l 抗癌药和免疫抑制剂;可引起出血性膀胱炎和肺纤维化
l 可能机制:由细胞色素P450代谢成丙烯醛等活性代谢物,启动脂质过氧化作用
(4)百草枯
ü 除草剂;
ü 肺脏蓄积作用强;
ü 被Ⅰ型和Ⅱ型肺上皮细胞摄取、活化,通过肺氧化性毒性机制引起肺损害;急性作用呈肺水肿,慢性作用呈肺纤维化;
ü 特征:弥散性间质和肺泡内纤维化
5、支气管肺泡灌洗(bronchoalveolar lavage, BAL)用等渗的盐溶液冲洗和灌注气管和肺泡区表面的过程,是一种采集支气管和肺泡表面脱落细胞和液体的方法。
第十七章 肝脏毒理学
1、肝脏毒理学:利用毒理学的基本原理和方法,研究外源毒物对肝脏的损害作用及其机制的学科;
n 是靶器官毒理学的主要研究领域;
n 在毒理学研究领域,为了区别于病毒性肝炎,近年来将化学物引起的各种急性和慢性肝脏损害统称为“化学性肝损害”(chemically induced liver injury):
M 短期暴露:肝细胞内脂质蓄积、肝细胞坏死、肝胆功能障碍等
M 长期暴露:肝硬化、瘤样改变等
2、(二)脂肪肝(fatty liver)
| 概念:脂质积聚含量超过总重量5%的肝脏;
| 特点:肝急性中毒的常见反应;可逆;不引起肝细胞坏死
3、(五)肝纤维化与肝硬化
Ø 概念:
慢性肝损伤晚期,纤维组织逐渐增多,肝脏微循环变形引起细胞缺氧并重建,最终肝脏结构由纤维组织壁包绕互连成为重建肝细胞结节
4、对乙酰氨基酚的肝毒性机制(图5)
细胞色素P450将其活化为N-乙酰-对苯醌(NAPOI),后者可耗竭谷胱甘肽或与肝蛋白结合,最终导致肝细胞死亡。
5、实验性肝损伤的体内检测:
血清酶学检测(谷丙转氨酶、谷草转氨酶较简便敏感,是应用最广的肝损害检测指标)
肝脏排泄功能检测
肝脏化学组成成分改变的检测
肝脏组织病理学检查
第十八章 肾脏毒理学
1、功能性指标:
(1)肾小球滤过率(glomerular filtration ratio, GFR):单位时间内(每分钟)两肾生成的超滤液量。 正常值:125ml/min
测定方法:菊粉、内生肌酐
意义:不仅反映肾小球的功能,而且还反映肾浓缩能力。
2、(一)急性肾功能衰竭( acute renal failure,ARF):一种可逆的肾小球和肾小管排泄功能不全。其特征为GFR突然减少引起氮质血症。是肾脏对药物毒性最常见的反应。
例如:乙酰氨基酚、阿司匹林、布洛芬
3、(四)汞
l 环境中存在的元素汞(汞蒸气)、无机汞盐、有机汞化合物;
l 肾脏的近曲小管是无机汞蓄积的主要靶器官;
l 汞所致急性肾毒性主要特征:接触24~48h内,出现近曲小管坏死和急性肾衰竭,伴随肾小球滤过率降低。
第二十章 药物临床安全性评价概述
药品:是指用于预防、治疗、诊断人体疾病的,有目的地调节人体生理机能并规定有适应证或者功能主治、用法和用量的物质,包括中药与天然药、化学药和生物制品。
新药临床前安全性评价意义与局限性
(一)意义
提供新药对人类健康危害程度的科学依据,预测上市新药对人体健康的有害程度,权衡药物对人体的危险性,保证上市的药物在临床剂量下无毒或毒性很小,即安全、有效。
(二)局限性
根据临床前安全性评价来预测临床的安全性是有一定风险的,一些新药上市之后出现毒副作用的而被淘汰。
原因: 一方面是新药本身,另一方面来自现有的毒理学评价手段。
(1)实验动物和人对药物反应的种属差异。 甲醇对人眼毒性比强,而对动物眼睛比较轻
(2)常规毒性实验所用的动物多系实验室培育的品种,反应较单一,而临床病人很广泛,对药物的敏感性各不相同。
(3)毒性实验所用的动物多是健康的,而临床用药的病人则可能同时患有多种疾病,而某种疾病的存在往往会成为发生某种毒性反应的必须条件。
(4)动物毒性试验中采用大剂量的方法与临床给药相差太大,容易造成假象。
(5)实验动物数量有限,那些发生率低的毒性反应,在少量动物实验中难以发现。一种苯噁洛芬的非甾体抗炎药,以万分之一的发生率使61人死亡。
药物非临床安全性研究质量管理规范 (Good Laboratory Practice for Nonclinical Safety Studies,GLP)
国内一般称为“药物非临床安全性研究质量管理规范”,或者“优良实验室规范”。系指严格实验室管理的一整套规范化的规章制度。是一种法规性文件,是阐述保证所做的总结报告全部资料质量及完整性的最低要求的方法和步骤。
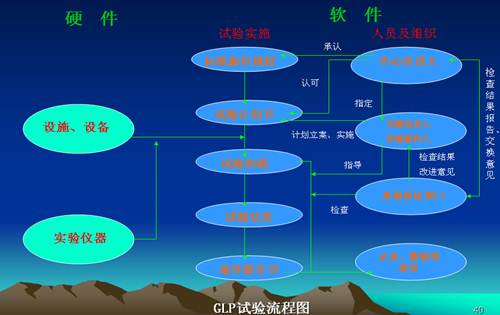
GLP规范的主要内容
硬件:实验动物室和从事研究用的实验室,必须按照GLP标准涉及施工和维护,保证空气洁净,减少各种微生物、灰尘对实验室的影响。
软件:从事安全性研究人员的素质和根据GLP规范指南制定的SOP及严格执行SOP的要求。如:仪器设备使用前检验校正,用后做好记录;实验记录不得涂改;实验报告要有实验者、专题负责人姓名和日期;实验试剂和实验动物要有品名来源等等。
GLP实验室人员和组织机构
1. 人员分类
中心负责人、专题负责人、实验操作人员、质量保证人员、其他人员
2. 组织机构
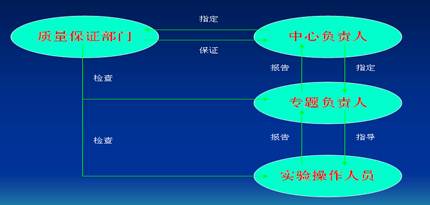
GLP实验室运行方式
第二十一章药物临床安全性评价基本内容
(新药物临床前毒理研究)
第一节 新药物临床前毒理研究的内容

第二节 毒理学实验的基本原则
一、实验设计的三原则
(一)重复:相同的实验条件下实验结果相同
1. 原则与含义:重现性;重复数
2. 重现性与重复数的辨正关系:在保证有统计学意义的重现性的前提下尽量减少重复数 。
3.实验重复数的数量与质量的辨证关系 :同时、同地、同条件、同种、同批、同病情。
4.实验条件的严密性和代表性的关系条件越严密,结论越确切,但实验的代表性就可能越差。
(二)随机:使每个实验对象都有相等的机会接受处理
1. 随机不是随便。2. 均衡随机(分层随机)优于绝对随机。
(三)对照:没有对照就没有比较,也没有鉴别
1. 对照应复合齐同可比原则 除了处理因素外,其他所有的条件都一致。
2. 对照能产生监控条件变化的作用 阳性对照、阴性对照 。
二、主要影响外推的因素
(一)种属差异及外推
1.致畸作用的种属差异(反应停)
2.毒物致癌作用的种属差异
(1)自发肿瘤发病率的种属差异
(2)对致癌剂的敏感程度的种属差异
家兔和小鼠对煤焦油敏感 大鼠和豚鼠不敏感
(3)致癌剂作用的靶器官的种属差异 芳香胺
(二)高剂量效应与低剂量效应的差异与外推
1、高剂量和低剂量下效应性质可能不同
CS2,高浓度导致末梢神经炎,低浓度危害血脂和心血管系统
长期高剂量乳糖引起的钙性肾病
2、高剂量向低剂量外推的线形关系的不确定性很多新的物质的剂量-效应关系或剂量反应关系不是很明确。
新 药 药 理 学 研 究
概述
药理学研究,是指利用生物(整体动物、麻醉动物、离体器官、组织、细胞或微生物培养等)在严格控制的试验条件下,观察药物的疗效及药动学等,包括主要药效学研究、一般药理学研究、药代动力学研究三方面。
第一节 主要药效学
概念:药物效应动力学简称药效学,是研究药物的生化、生理效应及机制以及剂量与效应之间的关系。
药理学实验设计的基本原则
1、随机2、对照3、重复
第二节 一般药理学研究
一、概述
广义的一般药理学(General Pharmacology)是指对主要药效学作用以外进行的广泛的药理学研究,包括安全药理学(Safety Pharmacology)和次要药效学(Secondary Pharmacodynamic)研究。
安全药理学
主要是研究药物在治疗范围内或治疗范围以上的剂量时,潜在的不期望出现的对生理功能的不良影响,即观察药物对中枢神经系统、心血管系统和呼吸系统的影响。
第二十二章生物技术药物临床安全性评价
一、非临床安全性评价的差异

二、生物技术药物非临床安全性评价中应注意的问题(自己适当简化)
1、安全性问题
◇药理作用的放大或延伸。 如胰岛素引起的低血糖休克。
◇免疫毒性,包括免疫原性、免疫抑制和刺激反应及过敏反应。
免疫毒性与超敏性、细胞转化及中和抗体的产生有关。
◇杂质或污染物引起的毒性。
宿主细胞的污染 过敏反应及其它免疫病理效应
核酸污染物 整合入宿主基因组
2、受试物的质量
用于药理和毒理试验的药物应与拟用于临床试验的药物具有可比性。
表达蛋白宿主细胞(如细菌、酵母、哺乳动物细胞等)的污染(残留蛋白、核酸)可能会导致潜在的危险,这些由杂质或污染物引起的安全性问题应尽可能地通过纯化等质量控制手段来解决。
3、组织交叉反应
◇在首次进入临床试验前,所有抗体类药品都应该完成体外组织交叉反应试验
◇用于组织交叉反应的人体和动物组织
FDA推荐的组织(如肾上腺、膀胱、骨髓、脾脏、肺、肝脏等)。
◇阳性和阴性对照对结果的解释非常重要
缺乏对照组,无法判定抗体的特异性结合。
4、相关动物种属的选择
所谓相关种属,是指受试品在该类动物上,由于表达有受试物作用的受体或抗原决定簇(对单抗而言),能产生药理活性。
例如 细胞因子在安全性评价使用中的动物种属上可与相应细胞因子受体结合,其亲和力应与其在人相应受体上的表现相似,并且产生与预期人体反应相似的药理反应。
体外亲合力试验、竞争结合试验及细胞功能试验等方法是筛选相关动物的常用方法。
安全评价方案常包括二种相关动物种属,但是在非相关种属动物中的毒性试验结果可能会误导,所以在证明合理的情况下,一种相关动物即可。
即使短期毒性试验必须应用两种动物,但随后的长期毒性试验也可能使用一种动物。
若不存在相关动物,可以考虑应用表达人源受体的转基因动物或使用同系蛋白进行安全性研究。
5、给药途径与剂量
尽可能与临床拟用的给药途径与频率相同,如果在受试动物体内药物的活性成分清除较快或溶解度偏低,可适当增加给药次数或给药容量。
如受到生物利用度、给药途径或动物生理状态等限制,也可以采用与临床不同的给药途径。
给药剂量应包括中毒剂量和未观察到不良反应的剂量(NOAEL),以反应剂量效应关系。
对某些毒性很小或无毒的生物技术药物,需根据药物预期的药理或生理作用、受试物的易得程度以及临床适应症选择合理的给药剂量。
目前国外通常采用的为预期最大人体暴露量的5-10倍以上。
6、免疫原性
? 生物技术药物通常对动物具有免疫原性,产品的很多特性会影响免疫原性:一级结构、糖基化、杂质、宿主细胞、纯化、制剂和储藏。
? 在重复给药的毒性实验中要对免疫原性进行评价,抗体反应特征(如抗体滴度、出现抗体的动物数、中和或非中和抗体)应予以鉴别。
? 除非在多数动物中抗体中和了生物技术药物的药理学和/或毒理学效应,否则抗体的检出不能作为提前终止临床前安全性评价或调整试验设定观察时间的唯一标准。
? 动物身上出现的免疫原性,并不能推测在人体是否会产生抗体。
? 人体也可能产生抗人源蛋白的血清抗体,但往往在抗体出现后仍存在治疗作用。
7、药代动力学(pharmacokinetics )
? 蛋白质在生物体内会很快降解为小肽和氨基酸,其药代动力学研究具有相当的难度,因此传统的生物转化试验对生物技术药物不是必要的。
? 放射性标记是生物技术药物药代动力学研究中经常使用的方法,但要保证放射标记的受试物保持了与非标记物相当的生物学活性。
? 由免疫介导的清除机制也可能影响生物技术药物在动物体内的药代动力学行为。
第二十三章 新药临床前安全性评价的统计学基础
一、数据类型:
1. 计量资料:用仪器、工具等测量(measure) 方法获得的数据,即为(measurment data)。也叫定量数据(Quantitative data)
特点:有计量单位,如患者的身高(cm)、体重(kg)血压(mmHg)、脉搏(次/分)、红细胞计数(5×1012/L)
2. 计数资料:按某种属性分类,然后清点每类的数据,称计数资料(count data)。也叫定性数据(Qualitative data)
特点:无固有计量单位,如肤色(黑、白)、血型(ABO)、职业(工农兵)、性别(男女)
3. 等级资料Rank data
半定性或半定量的观察结果。有大小顺序,所以也叫有序分类资料(ordinal category data)。
①癌症分期:早、中、晚。 ②药物疗效:治愈、好转、无效、死亡。 ③尿蛋白: -,±,+,++,+++及以上
二、总体与样本 population and sample
总体:根据研究目的确定的同质研究对象的全体(集合)。分有限总体与无限总体。
样本:从总体中随机抽取的部分观察单位。
