
实验报告
固相反应动力学实验
院(系) 材料科学与工程学院
专 业 材料类
班 级 2010级创新班
学生姓名 李智豪
2013 年 5 月 13 日
一、 实验目的
1、研究扩散控制固相反应机理,过程动力学。
2、学习研究Na2CO3-SiO2系统的固相反应。
3、验证金斯特林方程,研究转化率和时间的关系。
二、实验方法
1、研究系统
Na2CO3-SiO2系统(均为分析纯),在加热保温至700℃时,系统发生反应Na2CO3(s) + SiO2(s) → Na2O·SiO2(s) + CO2(g)↑。在此恒温下通过测量不同时间t时失去的CO2的重量,可计算出Na2CO3的反应量,进而计算出其对应的转化率G,来验证金斯特林格方程:[1-(2G/3)-(1-G)2/3]=KG*t的正确性。
2、实验仪器
热重同步热分析仪,电子分析天平,研钵,250目筛,烘箱。
3、实验过程
3.1 样品制备
将Na2CO3(AR)和SiO2(AR)分别在玛瑙研钵中研细,过250目筛。SiO2的筛下料在空气中加热至800℃,保温5h,Na2CO3筛下料在200℃烘箱中保温4h。把上述处理好的原料按Na2CO3:SiO2=1:1摩尔比配料,混合均匀,烘干,放入干燥器内备用。
3.2 样品测试
3.2.1检查周围环境及仪器状态:要求室内环境温度为23±5℃,熟悉控制器的操作。
3.2.2 开机预热,设定所需的SDT模式及要保存的信号(热流、重量、△T)等。
3.2.3 称量样品,将其装入测试坩埚中,放入仪器中,等待约5min,在其系统稳定后开始测量。
3.2.4 根据不同时间测出的重量填写表格。
三、实验数据及处理
1、数据记录
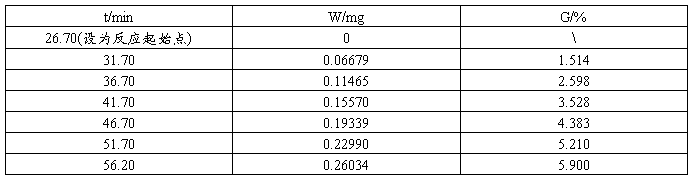
其中,
t/min:反应时间;
W/mg:CO2累计失重量;
G:Na2CO3转化率;
G=(W*106)/(44*10.6306)。
2、曲线绘制(origin)

由曲线可知,反应速率常数K接近于一个定值,即说明该系统固相反应满足某一个扩散控制速率模型。
由D4=1-2G/3-(1-G)2/3=KG*t计算D4值,做D4-t曲线。

由图可知,D4-t曲线的回归直线相关度为0.976,实验满足金斯特林格方程。
四、实验结论与误差分析
1、Na2CO3-SiO2系统的固相反应机理满足金斯特林格方程。
2、实验误差主要有三个方面:
2.1仪器因素影响:加热方式、炉子形状和尺寸的影响,样品支持器的影响,坩埚作为样品支持器的一个部件,对实验结果也有影响。
2.2 实验条件的影响:实验过程的气氛,升温速率,压力等对结果也有影响。
2.3 试样本身因素:式样用量、粒度尺寸、干燥程度还有混合程度等都会对结果产生影响。
第二篇:实验报告3—固相反应
 南昌大学实验报告
南昌大学实验报告
学生姓名: 学 号: 专业班级:
实验类型:■ 演示 □ 验证 □ 综合 □ 设计 □ 创新 实验日期: 实验成绩:
实验三 固相反应
一、实验目的
1. 掌握TG法的原理,采用TG法研究固相反应的方法。
2. 通过Na2CO3-SiO2系统的反应验证固相反应的动力学规律—金斯特林格方程。
3. 通过作图计算出反应的速度常数和反应的表观活化能。
二、实验原理
固体材料在高温下加热时,因其中的某些组分分解逸出或固体与周围介质中的某些物质作用使固体物系的重量发生变化,如盐类的分解、含水矿物的脱水、有机质的燃烧等会使物系重量减轻,高温氧化、反应烧结等则会使物系重量增加。
现代热重分析仪常与微分装置联用,可同时得到TG-DTG曲线。通过测量物系质量随温度或时间的变化来揭示或间接揭示固体物系反应的机理或反应动力学规律。
固体物质中的质点,在高于绝对零度的温度下总是在其平衡位置附近作谐振动。温度升高时,振幅增大。当温度足够高时,晶格中的质点就会脱离晶格平衡位置,与周围其它质点产生换位作用,在单元系统中表现为烧结,在二元或多元系统则可能有新的化合物出现。这种没有液相或气相参与,由固体物质之间直接作用所发生的反应称为纯固相反应。实际生产过程中所发生的固相反应,往往有液相或气相参与,这就是所谓的广义固相反应,即由固体反应物出发,在高温下经过一系列物理化学变化而生成固体产物的过程。
固相反应属于非均相反应,描述其动力学规律的方程,通常采用转化率G(已反应的反应物量与反应物原始重量的比值)与反应时间t之间的积分或微分关系来表示。
测量固相反应速率,可以通过TG法(适应于反应中有重量变化的系统)、量气法(适应于有气体产物逸出的系统)等方法来实现。本实验通过失重法来考察Na2CO3-SiO2系统的固相反应,并对其动力学规律进行验证。Na2CO3-SiO2系统固相反应按下式进行:
Na2CO3+SiO2—→Na2SiO3+CO2↑
恒温下通过测量不同时间t时失去的CO2的重量,可计算出Na2CO3的反应量,进而计算出其对应的转化率G,来验证金斯特林格方程:[1-(2G/3)-(1-G)2/3]=Kkt的正确性。
式中,Kk=Aexp(-Q/RT)为金斯特林格方程的速度常数,Q为反应的表观活化能。改变反应温度,则可通过金斯特林格方程计算出不同温度下的Kk和Q。
三、主要仪器设备及耗材
仪 器:Q600-SDT 差示扫描量热/热重(DSC/TGA)同步热分析仪 美国(TA)公司
实验材料:铂金坩埚1只,不锈钢镊子两把,Na2CO3 1瓶,SiO2 1瓶(均为A·R级)。
四、实验步骤 (同热重分析实验,可考虑略去)
1.样品制备
将Na2CO3(A·R)和SiO2(99.9%)分别在玛瑙研钵中研细,过250目筛。SiO2的筛下料在空气中加热至800℃,保温5h,Na2CO3筛下料在200℃烘箱中保温4h。把上述处理好的原料按Na2CO3:SiO2=1:1摩尔比配料,混合均匀,烘干,放入干燥器内备用。
2.测试步骤:
1).检查周围环境及仪器状态:要求室内环境温度为23±5℃。在SDT和控制器之间进行所有必要的电缆连接,连接所有气体线路,检查并接通各个装置的电源,将控制器连接到仪器,熟悉控制器的操作,如果有必要,请校准SDT。
2).设置净化气体:主净化气体应该限制为常用的、最好是N2、Ar等惰性气体。推荐的流量设置为100ml/min。辅助净化气体主要为引入更具反应性的气体,其流速通常低于主净化气体,推荐的流量设置为20ml/min。
3).设定所需的SDT模式及要保存的信号(热流、重量或Delta/T)等。
4).选择并准备样品。包括准备一个适当大小的样品并将其放到测杯中。
表1 Na2CO3~SiO2系统固相反应实验数据记录
反应时间:t(min);坩埚与样品重量W1(g);CO2累计失重量W2(g);
Na2CO3转化率G:[1-(2G/3)-(1-G)2/3]=Kk
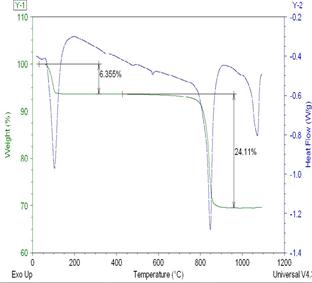
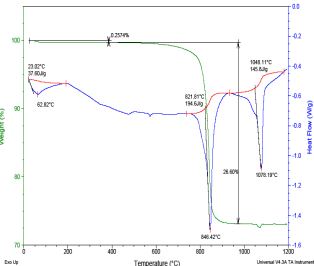
图1 Na2CO3-SiO2系统DSC/TGA曲线 图2 Na2CO3-SiO2系统DSC/TGA曲线
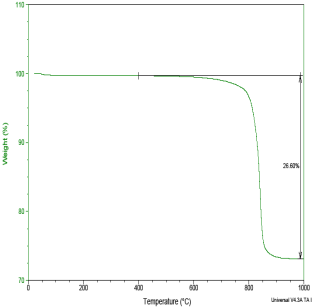
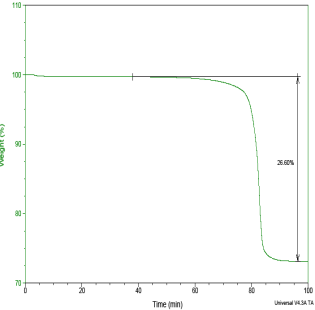
图3 Na2CO3-SiO2系统TGA/T曲线 图4 Na2CO3-SiO2系统TGA/t曲线
五、思考题
1.要使一个多步分解反应过程在热重曲线上明晰可辨,应选择什么样的实验条件?
2.温度对固相反应速率有何影响?其它影响因素有哪些?
3.本实验中失重规律怎样?请给予解释。
4.影响本实验准确性的因素有哪些?
