实验九植物细胞质膜透性的检测
一、实验目的
了解高温对植物细胞膜的伤害作用;学会使用电导率仪
二、实验原理
植物细胞膜是分隔细胞质和胞外成分的屏障,也是细胞和坏境发生物质交换的主要通道以及细胞感受坏境胁迫最敏感的部位。细胞膜的选择透性是最重要的功能之一。逆境伤害会造成膜选择透性的改变和丧失,使细胞内的物质(尤其是电解质)大量外渗,引起组织浸泡液的电导率值发生变化,就可知质膜的伤害程度和所测材料的抗逆性大小。
三、实验器材和试剂
1、 实验仪器和用具
DDS-11A型数显电导率仪、温箱、烧杯、量筒、镊子
2、 实验试剂
蒸馏水
3、 实验材料
小棠菜、橙子
四、实验步骤
1、 用打孔器取出20片小棠菜,20片橙子皮,用蒸馏水漂洗数次,以除伤口上的物质,减少伤口外渗的影响。然后用吸水纸吸干小棠菜和橙子皮的外附水,将每种材料分为两组,每组10片,分别放在盛有20ml蒸馏水的两个小烧杯中,将一杯放在45度温箱中,另一杯放在室温20到30度的条件下。
2、 30分钟后,小心取出实验材料,冷却至室温,用电导仪测量每一杯中溶液的电导率。
3、 重新将刚才取出的材料放入烧杯中,用沸水煮沸10分钟,取出幼苗,冷却至室温后再次测定电导率值。
五、注意事项
1、电导法对水和容器的洁净度要求严格,水的电导值要求1-2s(西门子),所用容器必须清洗后,再用蒸馏水冲净,倒置于洗净且垫有洁净滤纸的瓷盆中,干燥后备用。
2、在电导率测定中要用离子水,若制备困难可用蒸馏水代替,但需要设一空白试管(蒸馏水作空白)。测定样品时同时测定空白电导率值,按以下公式计算相对电导率,即
相对电导率=(浸泡率电导率值—空白电导率值)/(煮沸后电导率值—空白电导率值)*100
六、实验结果

1、空白电导率值=219*20u
2、小棠菜在常温下再经沸水处理后的
相对电导率值=(764*20u—219*20u)/(835*2000u—219*20u)*100%=8.76%
小棠菜经45度和沸水处理后的
相对电导率值=(1159*2000u—219*20u)/(1967*2000u—219*20u) *100%=58.85%
3、橙子在常温下再经沸水处理后的
相对电导率值=(333*200u—219*20u)/(263*2000u—219*20u)*100%=11.46%
橙子经45度和沸水处理后的
相对电导率值=(1273*200u—219*20u)/(244*2000u—219*20u)*100%=51.46%
七、结果分析
根据实验结果所得可知,高温胁迫条件下,植物细胞膜的透性会增加,而且温度越高,膜透性就越大,细胞内渗出的物质就越多,组织浸泡液的电导率值就越高。具体表现如下:
① 煮沸前的组织浸泡液在室温下所测得的电导率比在45℃高温处理后所测得的电导率要小几十到一百倍,说明了高温会造成膜透性的改变或缺失。
② 在45℃高温处理后所测得的电导率比煮沸后的组织浸泡液所测得的电导率只小几倍,造成原因可能是45℃高温处理后植物细胞膜的透性已缺失了大部分。
③ 在室温或45℃高温处理后再煮沸的组织浸泡液所测得的电导率相差不大,可能是因为煮沸后植物细胞膜的透性已完全丧失,细胞内物质全部外渗。
八、作业
书上的实验设计为什么将电导率的测量和糖的显色反应一并考虑?这种测量方法有何实践意义?
答:高温胁迫会使原生质膜的半透性消失,使胞内物质大量外渗,而电解质和糖是细胞内容物的主要成分之一。温度越高,渗出的物质越多,外渗液中所含离子和可溶性糖也越多。将电导率的测量和糖一并考虑,可以更肯定高温胁迫下植物细胞膜透性增大,且透性与温度成正比,当温度高到一定程度时,膜透性丧失。外渗液的电导率与可溶性糖浓度也呈一定的正比关系,而温度高到一定程度时,两者之比趋于稳定。
第二篇:细胞膜的渗透性实验报告.doc
姓名:高超 学号:201300140020 同组者:樊晓航,王昊明,余敬洋
实验名称:细胞的渗透性实验
一, 实验目的:
1. 了解细胞膜的渗透性
2 .了解各种小分子物质跨膜进入红细胞的速度
二, 实验原理:
细胞膜具有对物质选择透过的生理功能。脂溶性越高通透性越大,水溶性越高通透性越小;非极性分子比极性容易透过,小分子比大分子容易透过。水分子可通过由膜脂运动而产生的间隙。非极性的小分子如O2、CO2、N2可以很快透过脂双层,不带电荷的极性小分子,如尿素、甘油等也可以透过人工脂双层,尽管速度较慢,分子量略大一点的葡萄糖、蔗糖则很难透过,而膜对带电荷的物质如:H+、Na+、K+、Cl–、HCO3 –是高度不通透的。
将红细胞放入数种等渗溶液中,由于红细胞对各种溶质的透性不同,
有的溶质可以渗入,有的溶质不能渗入,深入的溶质可以提高红细胞
的渗透压,所以促进水分进入细胞,引起细胞溶血。由于溶质渗入的
速度互补相同,因此溶血时相同。
三, 实验器材:
鸡血,0.85%的氯化钠溶液,0.0085%的氯化钠溶液,0.8mol/L的甲醇,0.8mol/L的丙三醇,6%的葡萄糖溶液,2%的Triton X—100溶液,试管六支,离心机,滴管,载玻片,显微镜等
四, 实验步骤:
1、取鸡血2-3ml加入0.85%的氯化钠溶液4ml,在1000r/min条件下离心5分钟,(RBC压积量不少于0.3ml,否则应补加鸡血)
2、将上述离心的红细胞按沉淀量配成50%浓度的溶液(总体积量不少于0.6ml)
3、取六支试管,分别加入如下溶液个3ml
(1) 0.85%氯化钠溶液 (2) 0.0085%的氯化钠溶液
(3) 0.8mol/L的甲醇 (4) 0.85mol/L丙三醇
(5) 6%的葡萄糖溶液 (6) 2%的Triton X—100溶液
4、向上述六支试管中加入50%的红细胞悬液1滴,轻摇混匀,观察是否有溶血现象发生(观察时间1小时),记录溶血时间并于显微镜下观察 各种溶液中的细胞。
五,实验现象与结果:
实验结果:
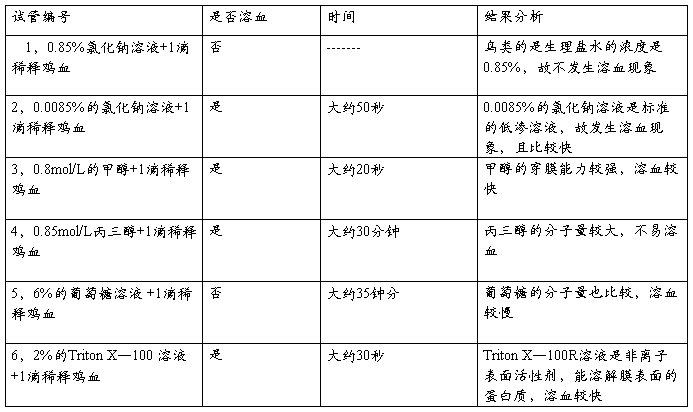
各组光度对比(全以0.85%氯化钠溶液为对照)



(1和2) (1和3) (1和4)


(1和5) (1和6)
溶血现象在显微镜下的图片:

3号管在10秒左右的溶血
五, 实验分析;
1, 由于甲醇和Triton X—100溶液渗透较快,所以观察时也要迅速,应事先做好准备,观察时也要快
2, 丙三醇和葡萄糖渗透的较慢,应每十分钟观察一次,才有现象
