附表一:
国家食品药品监督管理局监制
可疑医疗器械不良事件报告表
报告日期: 20xx年6 月 6 日
报告来源:? 生产企业 ?经营企业 ? 使用单位 单位名称:洋县长生堂药房
联系地址:洋县纸坊 邮编:723300 联系电话:0916——8216992 编码:? ? ? ? ? ? ? ? ? ? ?


第二篇:新可疑医疗器械不良事件报告表
济宁市第一人民医院西院区 可疑医疗器械不良事件报告表
报告日期: 年 月 日 编 码:? ? ? ? ? ? ? ? ? ? ? 报告来源:? 生产企业 ? 经营企业 ? 使用单位 单位名称:
联系地址: 邮 编: 联系电话:
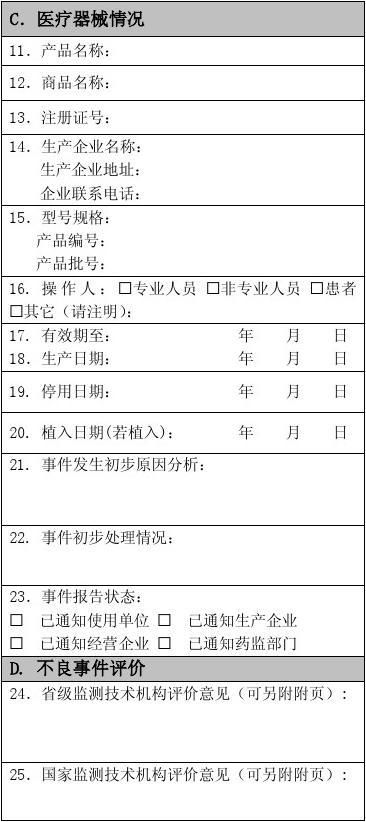
报告人: 医师? 技师? 护士? 其他? 报告人签名: 国家食品药品监督管理局制

医疗器械不良事件监测基础知识问答
1. 审批上市的医疗器械都是绝对安全的吗?
不是。任何医疗器械产品都具有一定的使用风险,都可能因为当时科技水平的制约、实验条件的限制等因素,而在临床应用过程中存在一定的风险。所谓批准上市,是指社会、技术、伦理和法令皆可接受的基础上的认可,而非绝对安全。被批准上市的医疗器械只是“效益大于风险”的“风险可接受”产品,即被批准上市产品在现有认识水平下,相对符合安全使用的要求。
2.什么是医疗器械不良事件?
医疗器械不良事件,是指获准上市的质量合格的医疗器械在正常使用情况下发生的,导致或者可能导致人体伤害的各种有害事件。
3.什么是医疗器械不良事件监测?
医疗器械不良事件监测,是指对医疗器械不良事件的发现、报告、评价和控制的过程。
4.医疗器械不良事件监测的目的是什么?
医疗器械不良事件监测旨在通过对医疗器械使用过程中出现的可疑不良事件进行收集、报告、分析和评价,对存在安全隐患的医疗器械采取有效的控制,防止医疗器械严重不良事件的重复发生和蔓延,保障公众用械安全。
5.如何正确认识医疗器械不良事件?
任何医疗器械在临床应用过程中,都可能因为当时科技水平的制约、实验条件的限制等因素,存在一些不可预见的缺陷。只有通过不
良事件的有效监测,对事件本身进行科学的分析和总结,才能及时采取适宜、有效的措施,保证医疗器械使用的安全有效,促进企业不断改进产品质量。
6. 如何区别医疗器械不良事件、医疗器械质量事故与医疗事故? 医疗器械不良事件主要是由于产品的设计缺陷、已经注册审核的使用说明书不准确或不充分等原因造成的,但其产品的质量是合格的。
医疗器械质量事故主要是指其质量不符合注册产品标准等规定造成的事故。
医疗事故是指医疗机构及其医务人员在医疗活动中,违反医疗卫生管理法律、行政法规、部门规章和诊疗护理规范、常规,过失造成患者人身损害的事故。
7.影响医疗器械不良事件报告的原因主要有哪些?
影响医疗器械不良事件报告的原因主要有:(1)医务人员害怕引起医患纠纷;(2)医疗器械生产企业对《医疗器械不良事件监测和再评价管理办法(试行)》的理解及执行不到位,缺乏主动开展监测工作的意识;(3)医疗器械生产企业、经营企业、使用单位等相关主体对不良事件概念及报告范围认识模糊,没有认识到医疗器械不良事件监测工作的重要性。
8.临床医务人员在医疗器械不良事件监测中应起到什么样的作用? 作为医疗器械不良事件的报告主体之一,医疗机构是大多数医疗器械的使用场所,也是医疗器械不良事件的主要发生地。同时,作为
医疗机构的工作人员,临床医务人员具有一定的专业背景和行业位置,能够掌握事件发生的第一手资料,并具有良好的鉴别能力。因此,临床医务人员在医疗器械不良事件监测中具有重要作用。医务人员及时报告、分析医疗器械不良事件,配合企业和相关部门的调查,是确保公众用械安全的重要保障。
9.医疗器械不良事件监测的报告范围是什么?
医疗器械不良事件监测的报告范围是医疗器械所发生的导致或者可能导致严重伤害或死亡的医疗器械不良事件。例如病人按照说明使用血糖试纸,由于试纸显示值错误导致使用了不当的胰岛素剂量,最终导致病人低血糖休克并入院。
其中,严重伤害事件是指有下列情况之一者:
(1)危及生命;
(2)导致机体功能的永久性伤害或者机体结构的永久性损伤;
(3)必须采取医疗措施才能避免上述永久性伤害或损伤。
10. 报告医疗器械不良事件应遵循什么原则?
报告医疗器械不良事件应当遵循可疑即报的原则。
11.什么是可疑即报原则?
可疑即报告原则,是指在不清楚是否属于医疗器械不良事件时,按可疑医疗器械不良事件报告。对于一部分医疗器械未达到预期使用效果的也属安全性问题,这些事件可以是与使用医疗器械有关的,也可以是不能除外与医疗器械有关的事件。
12.医疗器械生产企业、经营企业和使用单位发现或者知悉应报告的医疗器械不良事件后,应在几个工作日内进行报告?
对于导致死亡的医疗器械不良事件,医疗器械生产企业、经营企业和使用单位应在发现或者知悉之日起5个工作日内报告。
对于导致严重伤害、可能导致严重伤害或死亡的医疗器械不良事件,医疗器械生产企业、经营企业和使用单位应在发现或知悉之日起15个工作日内报告。
13. 医疗器械不良事件报告的内容和统计资料能够作为诉讼的依据吗?
医疗器械不良事件报告的内容和统计资料是加强医疗器械监督管理,指导开展医疗器械再评价工作的依据,不作为医疗纠纷、医疗诉讼和处理医疗器械质量事故的依据。
14.血压计在使用中可能会发生哪些可疑不良事件?
血压计是测量血压的仪器,主要分为水银柱式血压计和电子(无液)血压计两大类。血压计在使用中可能会发生导致或者可能导致人体伤害的可疑不良事件,主要表现为测量结果不准确、间断性黑屏、不显示血压值等。
15.体温计在使用中可能会发生哪些可疑不良事件?
体温计是测量体温的仪器,主要形式有玻璃体温计、电子体温计和红外体温计。体温计在使用中可能会发生导致或者可能导致人体伤害的可疑不良事件,主要表现为测量结果不准确、水银柱不上升/下降、不能计数等。
16.血糖仪在使用中可能会发生哪些可疑不良事件?
血糖仪是糖尿病患者自我血糖监测而使用的仪器,其在使用中可能会发生导致或者可能导致人体伤害的可疑不良事件,主要表现为血糖测量值不准确、血糖值显示不清晰、屏幕不显示等。
17.胰岛素注射笔在使用中可能会发生哪些可疑不良事件?
胰岛素注射笔是糖尿病患者胰岛素治疗中理想的注射用具,其前端是注射针头,后面的套筒则装有胰岛素,套筒容积大小根据胰岛素的种类而不同。胰岛素注射笔在使用中可能会发生导致或者可能导致人体伤害的可疑不良事件,主要表现为注射部位疼痛、注射针头漏液、推动困难、笔芯密封不严、笔芯变色等。
18.血管内支架在使用中可能会发生哪些可疑不良事件?
血管内支架主要用于大动脉瘤性血管狭窄、闭塞,外压性动静脉狭窄、闭塞,动脉瘤,动脉夹层、器官移植术后的血管狭窄,动脉粥样硬化性狭窄、闭塞等疾病的治疗。血管内支架在使用中可能会发生导致或者可能导致人体伤害的可疑不良事件,主要表现为支架脱载、无再流、支架内血栓形成、再狭窄等。
19.骨科植入物在使用中可能会发生哪些可疑不良事件? 骨科植入物主要包括骨接合植入物及骨与关节植入物。
骨接合植入物主要包括接骨板、接骨螺钉、髓内针、矫形用棒、矫形用钉、带锁髓内针、脊柱内固定植入物等。
骨与关节植入物主要包括人工髋关节、人工膝关节、人工肘关节等。
骨科植入物在使用过程中可能会发生导致或者可能导致人体伤害的可疑不良事件,主要表现为植入物变形、折弯、断裂、松动、脱落、磨损等。
20.人工心脏瓣膜在使用中可能会发生哪些可疑不良事件?
人工心脏瓣膜用于瓣膜损坏,适用于严重影响循环系统功能的疾病,如风湿性心脏病、先天性畸形、遗传性疾病、外伤等,其在使用中可能会发生导致或者可能导致人体伤害的可疑不良事件,主要表现为开放性卡瓣、瓣叶脱落、碟片被卡、瓣膜狭窄、血栓栓塞等。
21.宫内节育器在使用中可能会发生哪些可疑不良事件?
宫内节育器是置入人体进行妊娠控制的医疗器械,其在使用中可能会发生导致或者可能导致人体伤害的可疑不良事件,主要表现为意外妊娠、异位妊娠、严重贫血、盆腔炎、节育器异位、子宫穿孔等。
22.心脏起搏器在使用中可能会发生哪些可疑不良事件?
心脏起搏器是治疗心律失常等疾病的一种有效手段,其在使用中可能会发生导致或者可能导致人体伤害的可疑不良事件,主要表现为电极移位、心外肌肉收缩、静脉血栓/狭窄、电池提前耗竭、电极导线感染等。
23.透析机在使用中可能会发生哪些可疑不良事件?
透析机是用来进行血液透析或滤过的医疗设备,临床主要用于治疗急性或慢性肾衰竭、尿毒症。透析机在使用中可能会发生导致或者可能导致人体伤害的可疑不良事件,主要表现为空气监测不报警、头晕、心率下降等。
24. B型超声诊断仪在使用中可能会发生哪些可疑不良事件? B型超声诊断仪在临床上主要用于心脏、腹部、妇产科的检查,适用于心、肝、胆、肾、脾、胰腺、甲状腺、乳腺、子宫、膀胱等脏器的诊断检查。B型超声诊断仪在使用中可能会发生导致或者可能导致人体伤害的可疑不良事件,主要表现为显影模糊、突然死机、探头出现阴影、图像与检查部位不符等。
25. 医用监护仪在使用中可能会发生哪些可疑不良事件?
监护仪是用于精确了解患者身体情况变化,以减轻医院护士工作量的仪器,按照临床应用的地方不同,监护仪一般分为麻醉监护仪、肺功能监护仪、心电监护仪、脑电监护仪。监护仪在使用中可能会发生导致或者可能导致人体伤害的可疑不良事件,主要表现为监测数据不准确或不显示、黑屏、死机等。
26. 呼吸机在使用中可能会发生哪些可疑不良事件?
呼吸机是当前大、中型医院必备的抢救设备,是呼吸衰竭治疗、危重患者抢救以及麻醉呼吸管理的必需设备,是延长患者生命从而为进一步治疗争取宝贵时间的重要工具。呼吸机其在使用中可能会发生导致或者可能导致人体伤害的可疑不良事件,主要表现为潮气量过大、通气量不足、氧流量不稳定、管路漏气等。
27. 婴儿培养箱在使用中可能会发生哪些可疑不良事件?
婴儿培养箱是一种用已加热空气来控制婴儿所处环境温度的婴儿舱,主要用于对低体重婴儿、病危儿、新生儿的恒温培养、体温复苏、输液、输氧、抢救、住院观察等。婴儿培养箱在使用中可能会发
生导致或者可能导致人体伤害的可疑不良事件,主要表现为温度失控、报警失灵等。
28. 助听器在使用中可能会发生哪些可疑不良事件?
助听器是用放大了的声音来帮助失聪人士补偿听力的一种医疗器械,其在使用中可能会发生导致或者可能导致人体伤害的可疑不良事件,主要表现为噪音大、听不清,声音小、不能放大,声音过响,断音,耳鸣,耳道肿痛,头痛等。
29. 高压氧舱在使用中可能会发生哪些可疑不良事件?
高压氧舱是进行高压氧疗法的专用医疗设备,临床主要用于厌氧菌感染、CO中毒、气栓病、减压病、缺血缺氧性脑病、脑外伤、脑血管疾病等的治疗,其在使用中可能会发生导致或者可能导致人体伤害的可疑不良事件,主要表现为氧舱起火、氧气加湿罐破裂、测氧仪示值偏差大、主舱加压阀失灵、对讲系统失灵、氧舱开门受阻等。
30. 输液泵在使用中可能会发生哪些可疑不良事件?
输液泵是以控制药液的流速或流量,通过外加的压力将药液输入患者体内,达到治疗目的的仪器。输液泵在使用中可能会发生导致或者可能导致人体伤害的可疑不良事件,主要表现为为滴速失控、滴量不准、漏液、报警失灵等。
31. 心电图机在使用中可能会发生哪些可疑不良事件?
心电图机是提供诊断用的心电图图谱的医用电气设备及其电极,有单道心电图机、多到心电图机等。心电图机在使用中可能会发生导
致或者可能导致人体伤害的可疑不良事件,主要表现为结果不准确、走纸不正常、信号干扰、接触不良、黑屏、不显示心电图谱等。
32. 温热治疗床在使用中可能会发生哪些可疑不良事件?
温热理疗床是利用电热原理和远红外光波技术,集脊椎矫正、热灸、推拿、指压、温热效应等为一体的理疗设备,临床主要用于对高血压(颈源性)、腰椎间盘突出症、慢性胃炎、风湿性关节炎、失眠症、便秘、颈椎病、妇女痛经、慢性前列腺炎(非细菌感染)、胃脘痛的辅助治疗及保健。温热理疗床在使用中可能会发生导致或者可能导致人体伤害的可疑不良事件,主要表现为烫伤、红疹、瘙痒、水疱;头晕、头疼、恶心、呕吐;神经麻木;腰椎间盘突出;心慌、胸闷、心跳加速;肋骨受伤;脾、胆、肾脏增大;脑溢血;白细胞数量异常增高;死亡;胃痛;腹泻;血压升高等。
33.经外周插入的中心静脉导管在使用中可能会发生哪些可疑不良事件?
经外周插入的中心静脉导管临床主要用于支持性静脉输液治疗及血液取样,其在使用中可能会发生导致或者可能导致人体伤害的可疑不良事件,主要表现为导管脱落、断裂滑入体内,静脉炎,感染,导管破裂后漏液等。(综文)
34. 导尿管在使用中可能会发生哪些可疑不良事件?
导尿管临床主要经由尿道插入膀胱以便引流尿液出来,其在使用中可能会发生导致或者可能导致人体伤害的可疑不良事件,主要表现
为尿道红肿、疼痛、分泌物、血尿、腰痛、导尿管堵塞、脱落、气囊破裂等。
35.人工晶体在使用中可能会发生哪些可疑不良事件?
人工晶体是一种植入眼内的人工透镜,以取代天然晶状体的作用,其在使用中可能会发生导致或者可能导致人体伤害的可疑不良事件,主要表现为角膜水肿、角膜损伤、前房出血、眼内炎、青光眼、瞳孔变形移位、人工晶体位置异常等。
36. 一次性使用输液器在使用中可能会发生哪些可疑不良事件? 一次性使用输液器主要用于临床重力输液,其在使用中可能会发生导致或者可能导致人体伤害的可疑不良事件,主要表现为寒颤、高热、恶心、呕吐、输液器漏液、有异物等。
37. 缝合线在使用中可能会发生哪些可疑不良事件?
缝合线临床上主要用于一般外科手术的缝合,其在使用中可能会发生导致或者可能导致人体伤害的可疑不良事件,主要表现为伤口红肿、疼痛、化脓、不愈合/愈合延迟、线断裂等。
38. 颈椎牵引器在使用中可能会发生哪些可疑不良事件?
颈椎牵引器是一种新型的家用医疗保健器械,主要是利用充气牵引原理,拉伸矫正颈椎,其在使用中可能会发生导致或者可能导致人体伤害的可疑不良事件,主要表现为头晕、头痛,恶心,眼花,颈部皮肤红肿、瘙痒,颈部酸胀疼痛,气囊漏气、破裂等。
39. 静脉留置针在使用中可能会发生哪些可疑不良事件?
静脉留置针又称套管针,外套管质地柔软可随血管形状弯曲,置于血管内不易刺破血管壁而造成液体外渗,可降低重复穿刺率,减少病人痛苦。静脉留置针在使用中可能会发生导致或者可能导致人体伤害的可疑不良事件,主要表现为留置针漏液(接口处、针尾),套管脱落,套管堵塞,套管断裂,穿刺部位红肿、疼痛,静脉炎等。
