病理生理学实验

动物实验则可人为地严格控制实验条件,在动物身上造病,并对动物进行观察,记录和分析,然后将在动物身上所获得的资料与临床的疾病表现进行比较、分析,从中引出疾病的发生、发展的规律。
病理生理实验目的:除验证课堂讲授的部分理论,加深理解外,更主要的是培养同学初步具有实验性研究疾病的技能,为今后临床医学研究打下基础。
实验要求:
1、养成正规的技能操作习惯,耐心细致地观察实验中出现的每个现象
2、不能主观臆造实验数据,做到准确、及时、客观地记录。
3、爱护实验器材,如有损坏要登记,按设备处规定酌情赔偿。
实验前核对器械、试剂、实验结束清洗,清点器械、试剂。
4、同学实验中分工明确,责任到人。轮流取送动物,打扫卫生。
5、按时交纳实验报告。
实验一 缺氧
一、几种类型缺氧
目的要求 1、在动物身上复制缺氧性、血液性缺氧,以了解各种类型缺氧对机体影响及其表现特点。
2、观察缺氧时动物的一般情况,呼吸和内脏血液颜色的变化。

二、实验步骤
1、 乏氧性缺氧
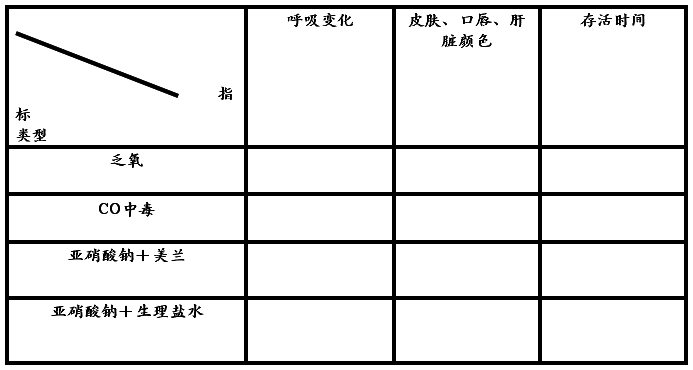
取钠石灰5g放入缺氧瓶内,观察瓶内小白鼠呼吸频率(次/分)、幅度、皮肤和口唇颜色,塞紧瓶塞,记录时间,每三分钟观察上述指标一次,记下动物死亡时间。
2、 CO中毒性缺氧
安装CO发生装置,用移液管向刻度试管中加入甲酸3ml,然后再加入浓硫酸2ml,塞紧橡皮塞,适当加热产生CO,随时观察上述指标。
3、 亚硝酸钠中毒性缺氧
取体重相近的两个小白鼠(甲、乙),观察正常指标。
甲鼠腹腔注射5%亚硝酸钠0.3ml+1%美兰0.3ml。
乙鼠腹腔注射5%亚硝酸钠0.3ml+1%生理盐水0.3ml
4、将各组死亡的小白鼠解剖腹腔,观察肝脏和皮肤粘膜、口唇颜色。
三、注意事项
1、按老鼠喜欢钻洞的习性让其进入瓶内
2、小白鼠腹腔注射,应头朝下,稍靠左下腹,注射器不能混用。
3、需密闭的缺氧瓶塞一定要塞紧,可用适量的水滴加在橡皮塞周围,以防漏气
4、每小组桌上都有浓硫酸与甲酸,在盘内使用,绝对不能打翻,因具有强腐蚀性,若滴在桌上、身上等,必须及时用自来水冲洗,用完后,试管立即用自来水冲洗干净(CO产生装置不一定密闭)
5、加热浓硫酸、甲酸时火焰不能过旺(防CO产生过多,致使小白鼠立即死亡,樱桃红色不明显),一般稍有冒泡即可,也不能煮沸后立即从火焰上移开,以防NaOH倒吸,加热时试管口绝不能对着人
6、美兰染料起到还原剂的作用,在专门注射盘中使用,防止美兰污染桌面,几个类型的缺氧死亡鼠要标记清楚
实验二 豚鼠高血钾症
实验步骤
1、豚鼠称重,用10%乌拉坦1ml/100g体重腹腔麻醉

3、设置打印正常心电图
4、腹腔注入10% kcl 1ml→5分钟→10%kcl 0.5ml→……
观察有变化时随时记录
5、观察到高血钾心电图后,自行选择抢救方案
4% NaHCO3 或10% CaCl2 或50%葡萄糖和胰岛素
6、继续注入kcl→室颤→开胸观察心脏停跳状态
实验注意事项
1、抓豚鼠时要小心,不要任意玩耍豚鼠,防被豚鼠抓伤。
2、腹腔麻醉 两人配合,头朝下,臀部朝上,左下腹注射麻药
插入踝部皮下,注意勿插进肌肉,因有肌电干扰。另外及时清除电极和电线周围的血和水迹,保持良好的导电状态
4、出现室颤开胸观察心脏停搏状态动作要迅速
典型的实验结果:
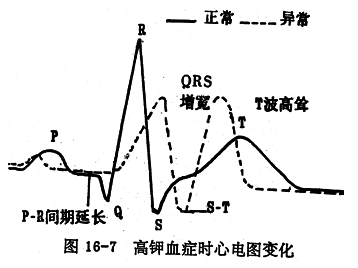
P波压低增宽, QRS波群压低增宽,T波高尖
Q-T间期缩短 传导阻滞,室颤

抢救方案:
4% NaHCO3 1、输入碱性溶液有利于钾从胞外移入胞内
2、注入高渗液后能使细胞外液容易迅速增加而起稀释作用,致血钾浓度相对下降。
3、钠离子具有对抗钾离子对心肌的作用,可以增加细胞的兴奋性,使心率加速。
10%氯化钙 钙对钾具有拮抗作用,但对血钾浓度无影响,应该注意的是注射氯化钙的速度过快会引起心律失常。
葡萄糖和胰岛素:由于细胞内合成糖原增多,钾离子由细胞外液转入细胞内(合成1g糖原时有0.5mmol的K+进入细胞内)所以可以降低血钾。
实验 呼吸功能不全
实验步骤
全麻下分离气管,插管,气管插管与呼吸传感器连接并记录正常呼吸曲线
复制窒息 完全窒息(不超过30秒钟) 观察皮肤颜色,窒息后记录呼吸曲线
解除窒息 10分钟左右呼吸恢复
复制气胸 兔右胸4~5肋间插入16号针头,5-10分钟记录呼吸曲线,抽尽胸腔内气体,封闭可能留下的通道。10分钟左右呼吸恢复。
复制肺水肿 抬高兔台,注射器针头插入气管插管分叉处,缓慢滴入10%葡萄糖液2ml,5-10分钟后,放平兔台,记录呼吸曲线
听诊器听到湿性罗音时,处死动物开胸,用线结扎两侧门, 肺取出肺称重
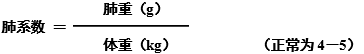
切开肺脏,观察有无泡沫液体流出。
注意事项:复制气胸的针头不能潮湿
复制气胸时针头钻入有一突破感,不能过深,否则损伤肺脏
50ml注射器抽吸空气后,针头和针筒一起拔出,封闭通道,滴入高渗葡萄糖时要缓慢,不要过快,防窒息。
处死动物时要结扎肺门,防水肿液流失
实验 肝性脑病
目的:采用肝大部分切除术,造成急性肝功能不全的动物模型,并以十二指肠插管灌注氯化铵溶液,观察血氨升高在肝性脑病机理中的作用。
步骤:
1、家兔称重全麻,仰卧固定于兔台上,腹部正中去毛
2、从胸骨剑突起,作上腹正中切口,切口长约8cm
3、打开腹腔,向下压肝,剪断肝与横膈之间的镰状韧带
4、再将肝叶向上翻,用手剥离肝胃韧带
5、用粗棉线在肝叶的根部结扎(仅留下二小叶),注意棉线不要剪去
6、用眼科小剪刀在十二指肠壁作一小切口,将导尿管插入肠腔约5cm,并固定导尿管防滑脱
7、 血管钳夹住腹壁切口,关闭腹腔
8、观察家兔角膜反射及对疼痛刺激反应
每隔5分钟向十二指肠插管中注入复方氯化铵溶液5ml,观察动物有无反应性增强,直至痉挛发作为止,记录所用的复方氯化铵溶液总量,并计算每公斤体重的用量。
分组:
1、实验组:
肝大部结扎,十二指肠插管注入氯化铵
2、对照组:
肝大部结扎,十二指肠插管注入生理盐水5ml/5分钟
3、假手术组:
分离肝脏(不结扎),十二指肠插管注入氯化铵5ml/5分钟
兔失血性休克
实验目的:
1. 复制失血性休克模型。
2. 观察动物失血前后的表现。
3. 探讨失血性休克的机理。
实验对象:家兔
实验用品:生物信号采集及分析系统(PowerLab)、压力换能器、呼吸换能器、心电导联线、体温计、注射器等。
实验步骤:
1. 家兔麻醉,固定。
2. 颈部手术:切开颈正中皮肤,分离气管和左侧颈总动脉,插入气管插管描记呼吸;插入颈动脉插管,接三通管,一侧记录血压,另一侧连注射器。
3. 放血前观察动物生理指标:一般情况,皮肤粘膜颜色,肛温、血压、心率、呼吸等。
4. 放血至血压为40mmHg止,血液置于与失血量等量的生理盐水中,混匀。放血速度适宜。放血量根据家兔大小确定,放血过程中观察血压变化。
[生理盐水和放血量计算方法:
放血量≈80ml/kg×体重(kg)×40%(ml)]
5. 维持血压在40mmHg 15-20分钟,观察失血期间动物生理指标改变。
6. 停止放血,回输血抢救。
注意事项:
1. 手术过程中尽量减少出血和休克。
2. 麻醉适度,过浅致动物疼痛可出现神经源性休克。
3. 动脉插管和回输血的注射器中事先加入肝素,以防凝血。
4. 放血前、后及回输血后,注意观察家兔的各项生理指标的变化。
