实验四水中碱度的测定(酸碱滴定法)
指导老师:张玉玲马哲
64080707 于澎
一、实验目的
通过实验掌握水中碱度测定的方法,进一步掌握滴定终点的判断。
二、实验原理
采用连续滴定法测定水中碱度。
三、实验仪器和药品
1. 酸式滴定管 25mL
2. 碱式滴定管 25mL
3. 锥形瓶 250mL
4. 移液管 25mL
5. 溴甲酚绿—甲基红指示剂
6. 酚酞指示剂
7. 标准浓度盐酸溶液 0.0511mol/L
8. 标准浓度的NaOH溶液 0.0507mol/L
四、实验步骤
1、实验前的准备工作 用HCl、Na2CO3、NaHCO3调节溶液pH,配制出pH=4,5,6,7,8,8.5,9,10,11,12等各种溶液。
2、实验步骤
分别吸取配制的各种pH的溶液,并按下列方法测定CO2(H2CO3*)、HCO3-、CO32-的摩尔浓度(mmol/L)。
⑴游离CO2的测定:用移液管吸取样品25mL,加二滴1%酚酞指示剂。用标准浓度的NaOH滴定至溶液呈淡红色不消失为终点,记下NaOH的用量V1mL。
计算式:
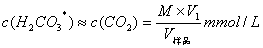
式中,M表示NaOH的毫摩尔浓度(mmol/L)。
在滴定过程中碳酸是由游离CO2转变而来,因此,c(H2CO3*)=c(CO2)。
⑵HCO3-的测定:吸取样品25mL,加4滴溴甲酚绿—甲基红指示剂,若溶液呈玫瑰红色,则此溶液无HCO3-;若此溶液呈绿色,则用标准浓度盐酸滴定至现玫瑰红色为终点,记下盐酸的用量V2mL。
计算式:
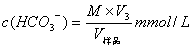
式中,M为盐酸的毫摩尔浓度(mmol/L)。
⑶HCO3-及CO32-的测定:吸取水样25mL,加入二滴酚酞,若深层呈红色时,用标准浓度的盐酸滴定至红色刚消失为止,记下盐酸的用量V1mL(若加酚酞后无色时则无CO32-);然后再加4滴溴甲酚绿—甲基红指示剂,用标准浓度的盐酸滴定绿色刚变成玫瑰红色为止,记下盐酸的用量V2mL。
五、实验数据

六、把数据输入Excel表格中并作图
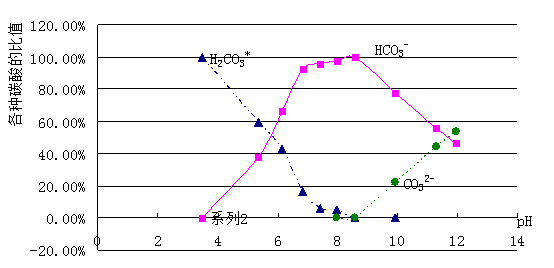
第二篇:水分析化学实验报告 - 副本
水中碱度的测定(酸碱滴定法)
一、实验目的
通过实验掌握水中碱度测定的方法,进一步掌握滴定终点的判断。
二、实验原理
采用连续滴定法测定水中碱度。用标准浓度的酸溶液滴定水样,用酚酞和甲基橙做指示剂,根据指示剂颜色的变化判断终点。根据滴定水样所消耗的标准浓度的酸的用量,即可计算出水样的碱度。
三、实验仪器和药品
1. 酸式滴定管 25mL
2. 碱式滴定管 25mL
3. 锥形瓶 250mL
4. 移液管 25mL
5. 溴甲酚绿—甲基红指示剂
6. 酚酞指示剂
7. 标准浓度盐酸溶液 0.0511mol/L
8. 标准浓度的NaOH溶液 0.0507mol/L
四、实验步骤
1、实验前的准备工作 用HCl、Na2CO3、NaHCO3调节溶液pH,配制出pH=4,5,6,7,8,8.5,9,10,11,12等各种溶液。
2、实验步骤
分别吸取配制的各种pH的溶液,并按下列方法测定CO2(H2CO3*)、HCO3-、CO32-的摩尔浓度(mmol/L)。
⑴游离CO2的测定:用移液管吸取样品25mL,加二滴1%酚酞指示剂。用标准浓度的NaOH滴定至溶液呈淡红色不消失为终点,记下NaOH的用量V1mL。
计算式:

式中,M表示NaOH的毫摩尔浓度(mmol/L)。
在滴定过程中碳酸是由游离CO2转变而来,因此,c(H2CO3*)=c(CO2)。
⑵HCO3-的测定:吸取样品25mL,加4滴溴甲酚绿—甲基红指示剂,若溶液呈玫瑰红色,则此溶液无HCO3-;若此溶液呈绿色,则用标准浓度盐酸滴定至现玫瑰红色为终点,记下盐酸的用量V2mL。
计算式:

式中,M为盐酸的毫摩尔浓度(mmol/L)。
⑶HCO3-及CO32-的测定:吸取水样25mL,加入二滴酚酞,若深层呈红色时,用标准浓度的盐酸滴定至红色刚消失为止,记下盐酸的用量V1mL(若加酚酞后无色时则无CO32-);然后再加4滴溴甲酚绿—甲基红指示剂,用标准浓度的盐酸滴定绿色刚变成玫瑰红色为止,记下盐酸的用量V2mL。
五、实验数据
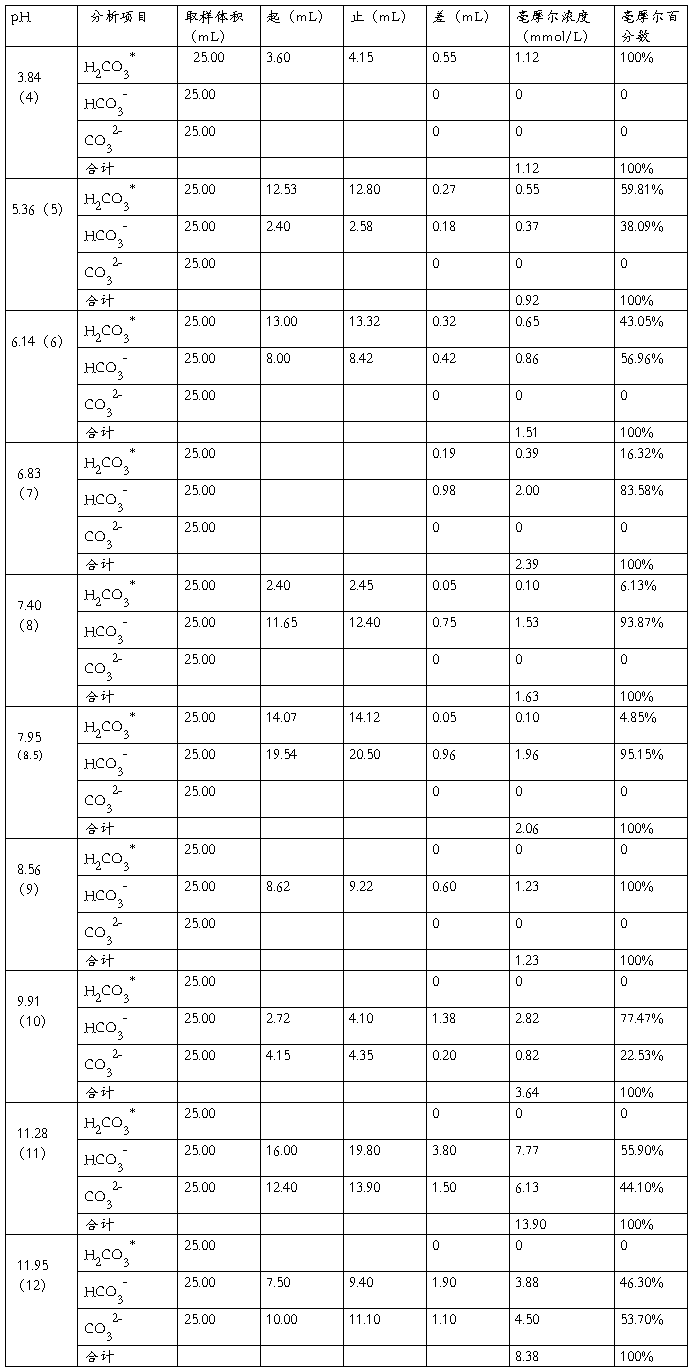
六、把数据输入Excel表格中并作图
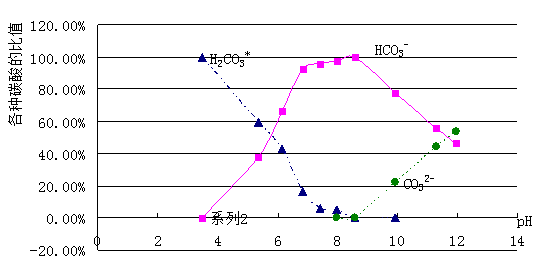
注意事项
1.水样中不能含有大量余氯及强氧化剂,不能有太大浊度、色度。
2.CO2含量高时影响测定,应事先加热煮沸除去。
3.碱度小的水样如蒸汽冷凝液,脱盐水和锅炉给水等应采用微量滴定管和低浓度的酸标准溶
