纸片法药敏试验
1)目的 本操作规程依据WS/T 125-1999,规定了临床抗菌药物敏感试验标准(纸片法)
内容做必要的细化和补充,规范纸片法药敏检测方法。
2)适用范围 本细则适用于适用于多种动物细菌病药物筛选。
3)职责
检测人员:负责按照本细则对被检样品进行检测。
复核人员:负责对检测操作是否符合规范以及检测结果是否准确进行复核。
4)方法原理 纸片法药敏试验由快速生长的致病菌标定,适合肠杆菌科、葡萄球菌、肠球菌、铜绿假单胞菌、不动杆菌。经适当改动可用来测定嗜血杆菌、淋病奈瑟菌和链球菌。对于使用培养基不同、孵育环境不同或生长率不同的菌类,不能用纸片法做药敏试验。
5)仪器设备 恒温培养箱、冰箱等。
6)试剂与材料 普通琼脂培养基、药敏片。
7)环境条件 操作环境温度22~28℃、湿度40~80%、电源220V。
8)检测步骤
8.1 制备接种菌液
8.1.1 增菌法
选琼脂平板上形态相同的菌落至少4~5个,用接种环挑其顶部,移至4~5ml肉汤或大豆酪蛋白消化液中。放置35℃培养至菌液浓度达到或超过比浊管浓度(一般需2~6h),浓度约1~2×108cfu/ml。用生理盐水或肉汤校正菌液浓度至与麦氏单位标准比浊管相同。可用光电比浊。
8.1.2 直接菌悬液法
可直接用过夜培养的菌落(必须用无选择性培养基,如血平板)在盐水或肉汤中制备接种菌液。菌液浓度调至0.5麦氏单位标准比浊管。此法亦适用于在肉汤培养基中生长不好的细菌如嗜血杆菌、淋病奈瑟菌及葡萄球菌的甲氧西林或苯唑西林的药敏试验。
8.2 接种平板
校正的菌液须在15 min内使用。用一无菌棉拭子蘸取菌液,并在上端管壁旋转挤压几次,去掉过多的菌液。用拭子涂布整个琼脂平板表面。Mueller-Hinton 琼脂平板用前应烘干。反复涂布几次,每次将平皿旋转60度,保证涂布均匀。
8.3 贴纸片
接种平板后,贴上药敏纸片。用镊子或针尖压一下纸片使其与培养基表面贴牢。纸片要贴得均匀,纸片与纸片中心距离不得小于24㎜。原则上,直径150㎜的平板贴12张纸片,直径100㎜平板贴6张纸片。贴上纸片15min内,须把平板倒放在35℃孵箱中。
8.4 测量抑菌环
经16~18h培养后,观察结果。菌液浓度合适且涂得好,抑菌环规则,细菌呈融合生长。手持平皿从背面目测检查每块平板,借反射光(黑色无反光背景),用卡尺、普通尺或特制的模板量取抑菌环直径,测量抑菌环直径须包含纸片直径,单位为毫米。培养基中如果加了血液,须打开平皿盖,借反射光,从正面量抑菌环。葡萄球菌和肠球菌,须培养24h后,经透射光检查苯唑西林和万古霉素的抑菌环内有无耐药菌株的生长。抑菌环内有任何生长都判断为耐药。
肉眼见不到细菌明显生长的区域为抑菌环边缘,有很难辨认的细小菌落者不算。如抑菌环内有大菌落长出,须再移种出来,重新鉴定,重新做敏感试验。变形菌在某些抗菌药物纸片周围可弥漫生长到抑菌的区域内,但抑菌环边缘清楚,弥漫生长不算。甲氧苄胺嘧啶和磺胺药的拮抗剂会支持细菌生长,因而测这类药时可忽略轻微生长(80%以上受抑制),以浓密生长的区域作为抑菌环的界限。
9)检测记录和数据处理
参照表1~表8的标准对抑菌环的大小作出解释,以敏感、中介或耐药的形式报告结果。
表1 肠杆菌科用的抑菌圈直径解释标准和相对应的最小抑菌浓度(MIC)折点
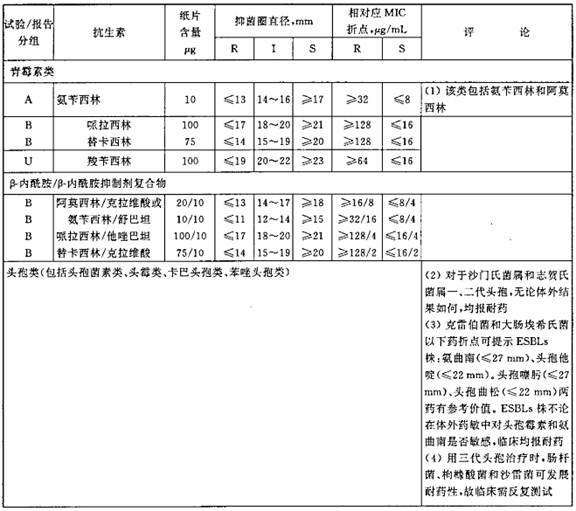
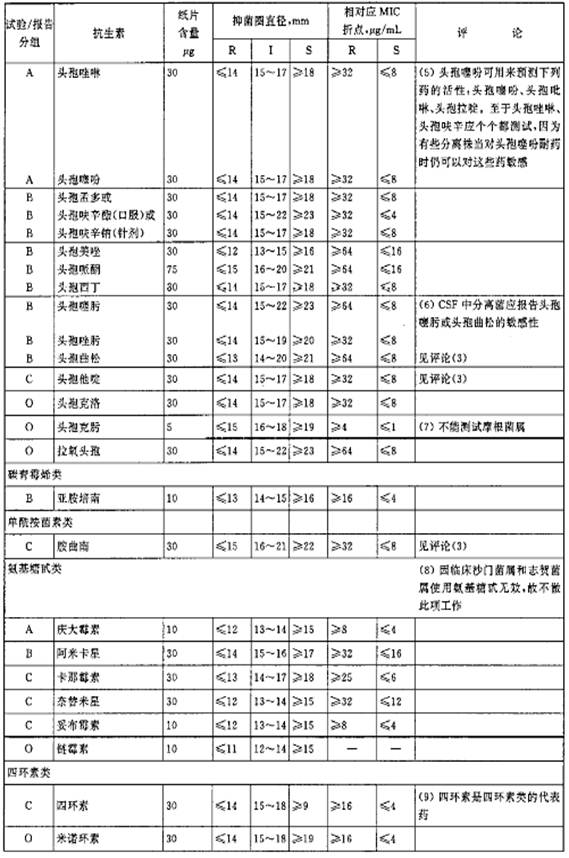
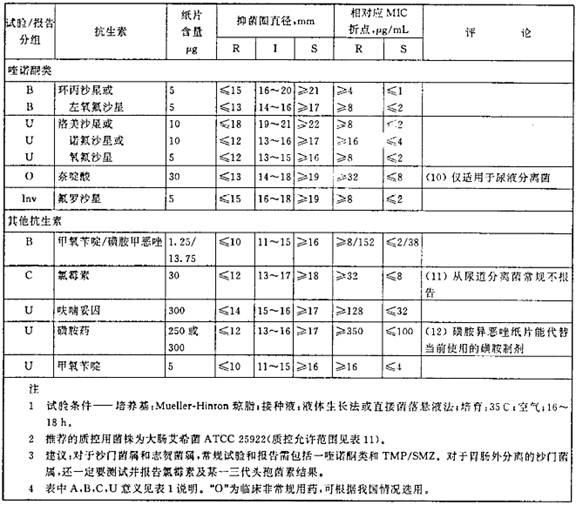
表2 铜绿假单胞菌和不动杆菌用的抑菌环直径解释标准和相对应的最小抑菌浓度(MIC)折点
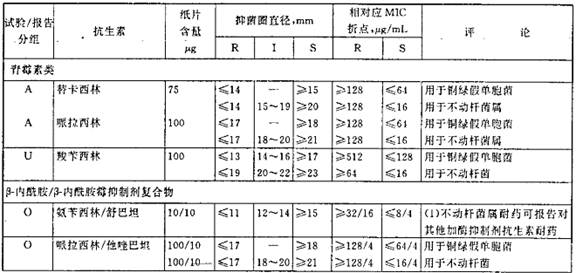
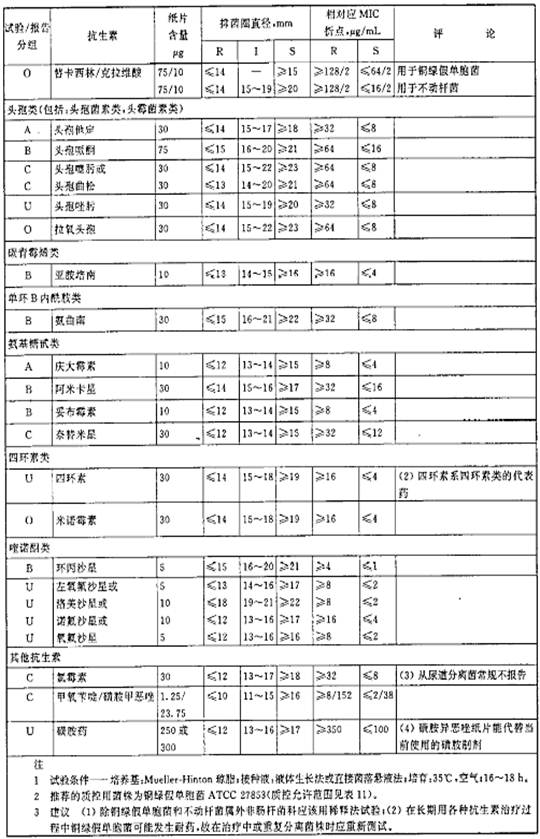
表3 葡萄球菌属的抑菌圈直径解释标准和对应的最小抑菌浓度(MIC)折点
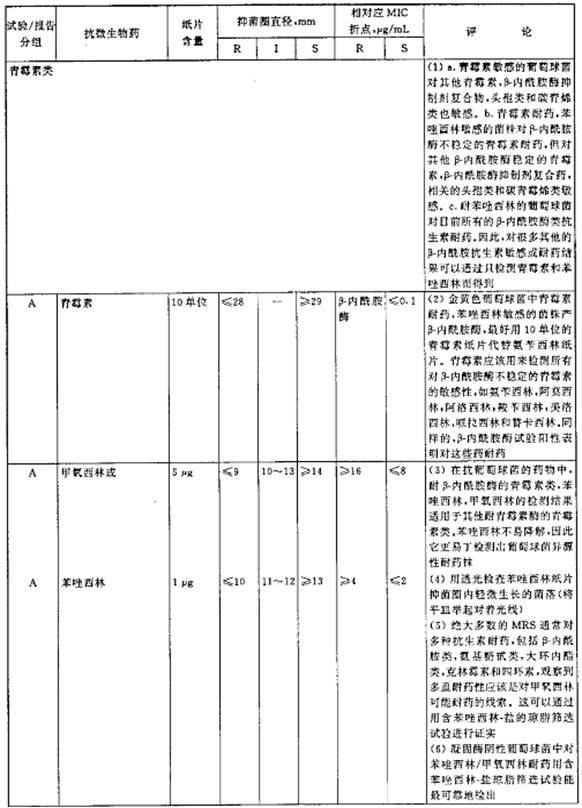
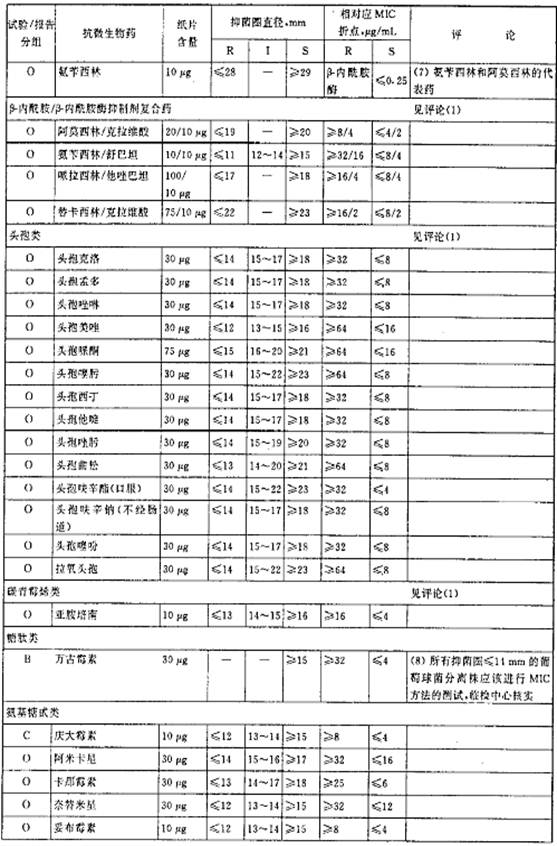
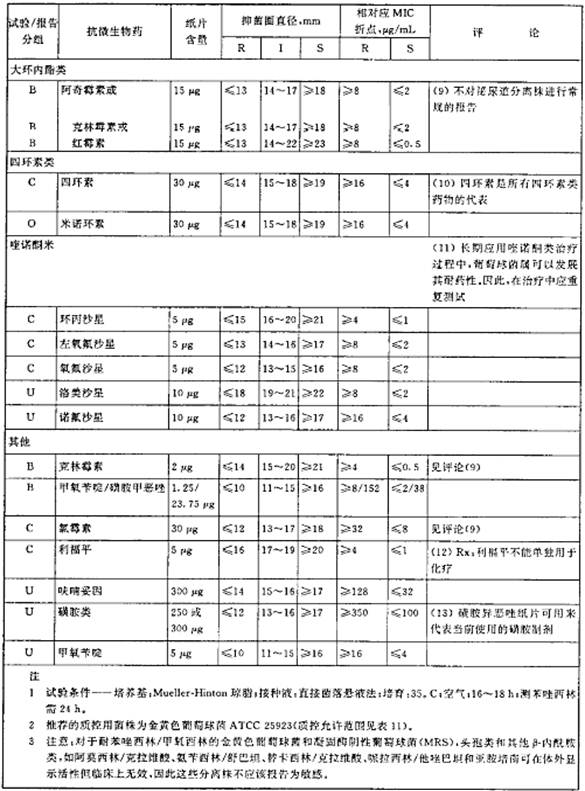
表4 肠球菌属的抑菌圈直径解释标准和对应的最小抑菌浓度(MIC)折点
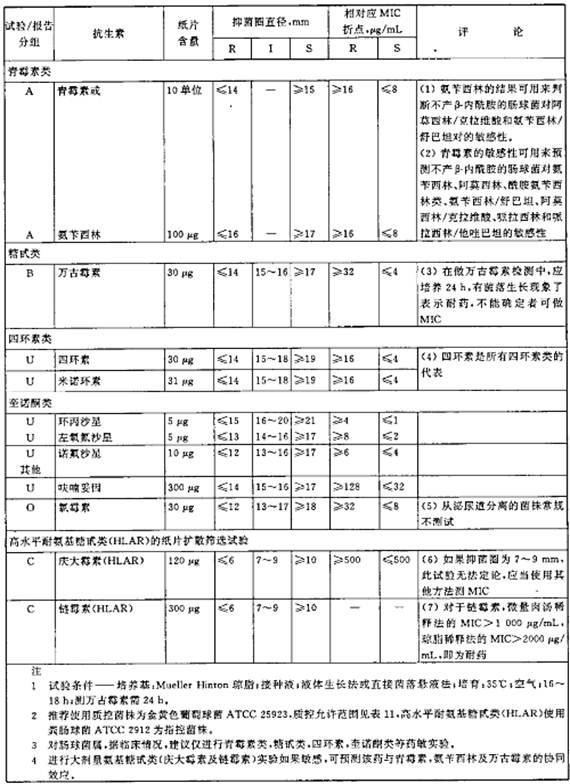
表5嗜血杆菌属的抑菌圈直径解释标准和对应的最小抑菌浓度(MIC)折点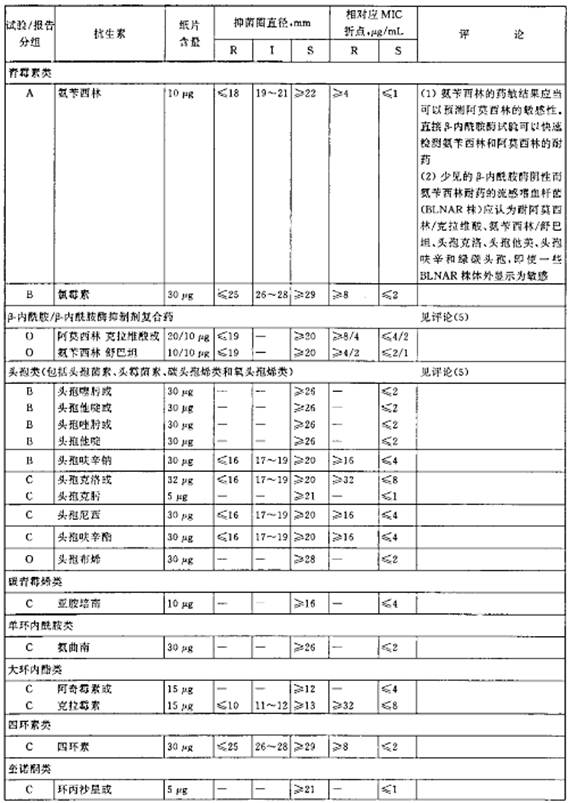
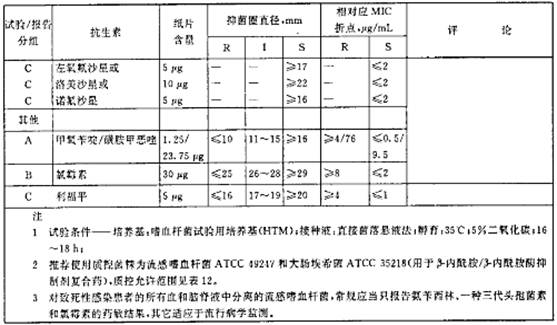
表6淋病奈瑟军的抑菌圈直径解释标准和对应的最小抑菌浓度(MIC)折点
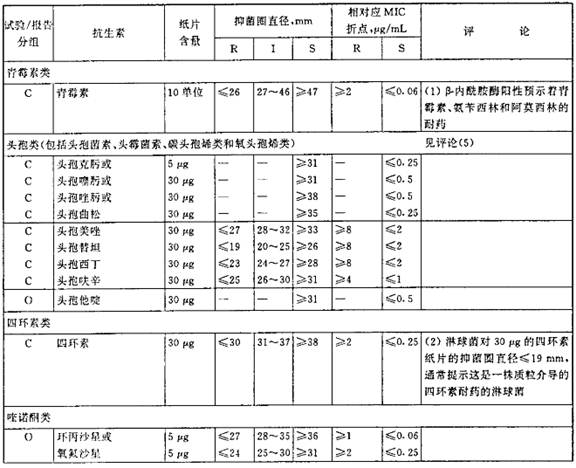
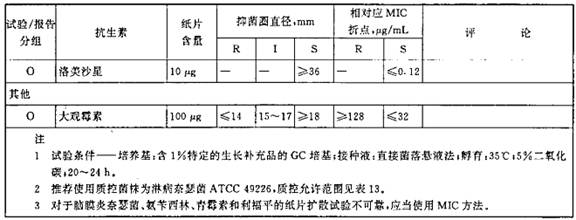
表7 肺炎链球菌的抑菌圈直径解释标准和对应的最小抑菌浓度(MIC)折点
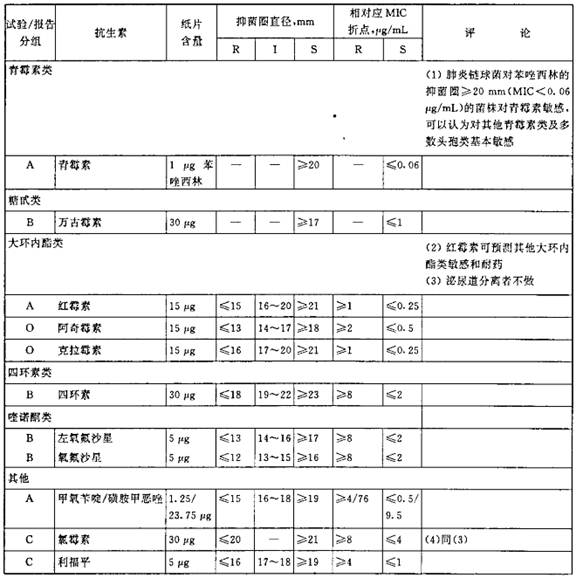
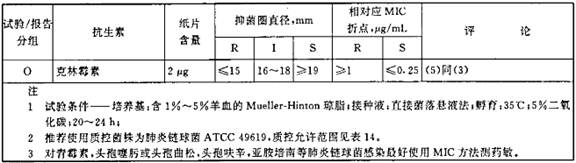
表8 非肺炎链球菌的其他链球菌的抑菌圈直径解释标准和对应的最小抑菌浓度(MIC)折点

10)注意事项
10.1) 戴一次性手套、口罩;
10.2) 注意无菌操作,严防污染。
第二篇:纸片法(KB)药敏实验原理及实际操作方法
纸片扩散药敏试验的原理:将含药物的纸片贴在接种有待测菌的固体培养基上,通过药物在培养基上的扩散,观察是否出现抑菌环,推断是否抑制细菌的生长。药物扩散的距离越远,药物浓度越低抑菌能力越强,因此可根据抑菌环的大小,判定药物对细菌的抑制作用强弱。药敏试验根据美国临床标准委员会 (NCCLS) 推荐的 K–B 琼脂法进行。本实验通过纸片药敏试验法观察多酸化合物对细菌有无抑制作用,为试管二倍稀释法提供有效基础数据。
用无菌棉拭子蘸取已经校正的 0.5 麦氏比浊浓度的菌液,挤掉多余菌液。用棉拭子涂布整个 MH 培养基表面,每次将平板旋转 60°,涂抹三次,最后沿周边擦绕两圈,以保证菌液涂抹均匀。待平板上的水分被琼脂完全吸收后贴含药纸片。用无菌镊子取药敏纸片贴在平板表面,纸片一贴后不可再拿起。每个平板贴 5 张纸片,纸片间距不少于 24 mm,纸片中心距平皿边缘不少于 15 mm。在菌接种后 15 min内贴完纸片。将平板反转,37℃ 恒温孵育 18~24 h 后取出,用游标卡尺测量抑菌圈直径,由平板背面测量最接近的整数毫米数并记录,每个平板各设三个平行组平板,测量抑菌直径时,应取三个平板的平均值为最终结果。抑菌环边缘以肉眼见不到细菌明显生长为限。
每次药敏试验用大肠杆菌 ATCC25922 和金黄色葡萄球菌 ATCC25923 做质控。药敏判读标准根据 CLSI 标准 (2009 年) 所载受试药对质控菌的抑菌环直径范围作为实验质控标准(判读标准见表 5-2)[84]。
表5-2 纸片扩散法-用质控菌株抑菌环直径(mm)允许范围监测抗菌药物敏感性试验准确
性
Table 5-2 Disc diffusion test - according the admissible range of quality-control strain’s inhibition zone diameter to monitor the accuracy of antibiotics susceptibility test (mm) 抗菌 药物 KF AMP CIP NOR
纸片含药量(?g) 30 10 5 5
S ≥18 ≥17 ≥21 ≥17
I 15–17 14–16 16–20 13–16
抑菌环直径(mm) R ≤14 ≤13 ≤15 ≤12
大肠埃希菌ATCC25922 16–22 28–35 30–40 15–21
金黄色葡萄球菌ATCC25923 27–35 27–28 22–30 29–37
KF: 头孢噻吩;AMP: 氨苄西林;CIP: 环丙沙星;NOR: 诺氟沙星;S: 敏感;I: 中介;R: 耐药
