中山荣杰医疗器材工业有限公司雾化厂
内部品质稽核报告
页次: 1/2
1. 目的:为保证品质管理系统的持续适宜性和有效性,确保质量管理体系与系统文件的符合性,达到改善和完善质量体系之目的,是公司朝向全面品质管理迈进。
2. 审核范围:ISO13485:2008要素
3. 审核依据:ISO13485:2008标准、品质管理系统文件、法律法规、国家、行业标准、客户合同
内部审核员:审核组长: 李棉深 审核时间:20xx年12月9号
4. 审核过程综述:
本次内部审核是自本公司四个车间按ISO13485:2008标准要求统一建立并实施品质管理系统以来的第一次交叉审核本次审核前管理者代表任命了审核小组组长和审核员。
审核组长在审核前3天发出了审核通知,排定了审核行程计划,并分发至相关人员知悉,由资料中心制作检查表以作为现场审核的指引,在现场审核过程中各审核员利用询问、交谈、查询文件、现场观察、并认真填写了审核记录。各陪审人员均能给予充分配合,使本次审核进行比较顺利。 本次内审高层主管非常重视,总经理和管理者代表对审核全过程进行了监督,发现问题及时予以指正。
5. 审核结论
本次审核本车间共发现不符合项31个,分别分布在标准:
1)资料分析与持续改善管理程序5-2-5、5-5-1,
2)制程检验与测试程序5-3-1、5-2-3、5-4-1、5-4-5
3)检验量测与测试设备校正程序5-4-1、5-6-1、5-1-1、
4)识别与追溯管制程序5-4-2
5)不合格品管制程序5-4-1、5-3-1
6)矫正与预防管制程序
7)风险管理程序
8)设计开发控制程序
9)技术资料管制程序5-5-1、5-6-1、5-6-3、5-7-1
10)机器设备保养管制程序5-7-1、5-4-1
11)仓储管理程序5-1-2、5-10-1、5-12-1、5-12-2、5-1-5-2-5、5-4-3、5-7-2
12)文件与资料管理程序5-7-2
不符合项均在规定的时间内进行了纠正措施,效果明显。
通过本次审核,可评价出本公司按ISO13485:2008《医疗器械 品质管理系统 用于法规的要求》建立的品质管理系统运行基本是符合的,且可利用内部审核这种手段来保持和改进品质管理系统的有效性,但综合此次内部审核有以下作业缺失尚待改进:
1)审核员对品质管理系统熟悉度仍待加强:包括ISO推行小组人员,因品质管理系统建立,对系统要求,尤其ISO13485标准,虽已有受过训练,仍有待籍多次实际参与接触,以提高审核能力。
2)被审核单位主管对品质管理系统不够了解:被审核时无法立即回复,翻阅文件时间过过久,有些程序执行不到位,缺失项比较多尤其是开发课、品保课和仓管。
3)对现场审核人员宣导不够:尚有员工不知道本部门品质目标和品质目标达成情况。
4)审核员技巧不足:审核员审核技巧不足,审核发现缺点的深度及广度不够,除11个程序,有审核出缺点外,其他章节均未查出缺点,不具代表现在系统上的有效性。
核准: 制表:安军红 日期:2010.12.09
文件编号: AJR-QRG-007 版本:A
不符合项分布表 2/2
受审核单位:
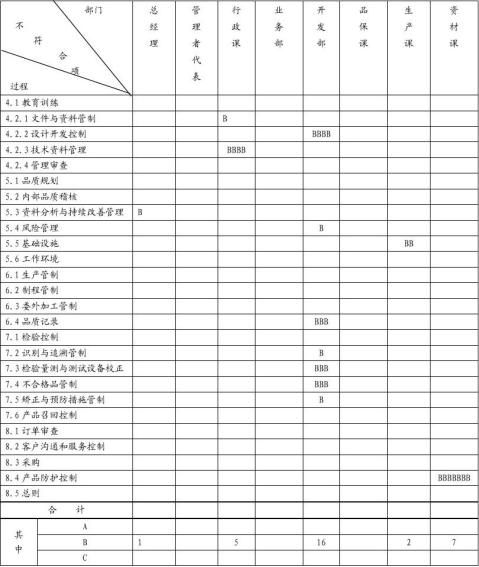
注:①A-系统性不符合,B-实施性不符合,C-效果不符合;②在A、B、C后加▲,如A▲表示其为严重不符合;
③一个不符合项用一个字母表示,二个不符合项用二个字母表示,余同。
文件编号: AJR-QRG-007 版本:A
第二篇:内部品质系统审核报告
内部品质系统审核报告
审核报告编号:2007-1

