实 验 报 告
姓名: 班级: 同组人: 自评成绩:
项目 碱度的测定 课程: 学号:
一、实验目的
1、掌握酸碱滴定法测定碱度的原理和方法。
2、掌握碱度测定结果的计算。
3、熟练滴定操作及相关仪器的操作方法。
二、实验原理
水的碱度主要由碳酸盐、重碳酸盐、及氢氧化物组成,但在某些情况下,如水中存在
磷酸盐、硅酸盐、硼酸盐等也会产生一定的碱度。
碱度的测定是在水样中加入适当的指示剂,用酸标准溶液进行滴定,可分别测出水样
中各种碱度,其反应如下:
OH- + H+ = H2O CO32- + H+ = HCO3- HCO3-+ H+ = H2O + CO2
根据上述到达终点时所用酸的量可计算出溶液中碳酸盐、重碳酸盐及总碱度。
三、仪器和药品
仪器:250mL锥形瓶3个;50mL酸式滴定管1支、20、50 mL移液管、50mL量筒。
试剂:0.1%酚酞指示剂、0.1%甲基橙指示剂、0.1mol/L盐酸标准溶液、0.05000mol/L Na2CO3
四、内容及步骤
(一)0.1mol/L盐酸标准溶液浓度的标定
准确量取20.00mL 已配好的0.05000mol/L Na2CO3标准溶液置于3只250mL锥形瓶中,加水约30mL,温热,摇动使之溶解,以甲基橙为指示剂,以0.lmol/LHCl标准液滴定至溶液由黄色转变为橙色,记下HCl标准溶液的消耗用量(3份测定的平均偏差应小于0.2%,否则应重复测定),并计算出HCl标准溶液的浓度。
(二)碱度的测定(双指示剂法)
准确移取水样l00mL于250mL锥形瓶中,加人酚酞指示剂三滴,如呈红色,用0.1mol/L盐酸溶液滴定至颜色刚好消失,记下盐酸溶液的消耗体积(V1);在此溶液中,再加入2滴甲基橙指示剂,继续用标准盐酸溶液滴定至橙色为止,记下盐酸的消耗量(V)。判断水样中碱度的组成及含量。
五、实验结果记录与计算
(一)盐酸标准溶液浓度的标定
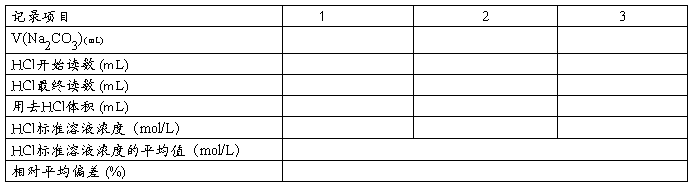
(二)碱度的测定
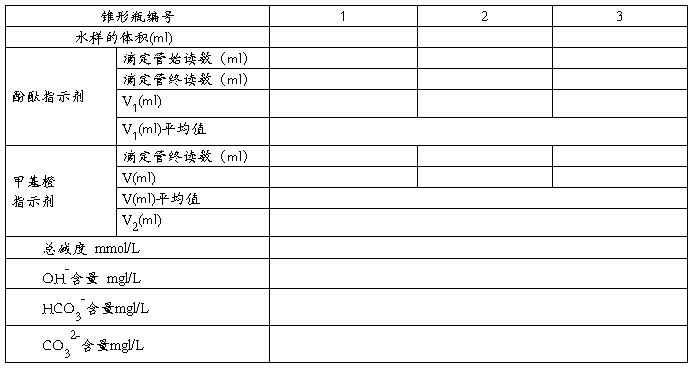
六、思考题:
1、什么叫碱度?如何判断碱度组成?
2、测定结果碱度的计算公式如何表示?
3、用于滴定的锥形瓶或烧杯是否需要干燥?要不要用标准溶液润洗?为什么?
教师评语:
年 月 日
第二篇:化学实验报告 实验__缓冲溶液的配制及pH测定
实 验 报 告
姓名: 班级: 同组人: 自评成绩:
项目: 缓冲溶液的配制及pH测定 课程: 学号:
一、实验目的
1. 学会标准缓冲溶液的配制方法,并验证其性质。
2. 掌握酸度计测定溶液pH的方法。
二、实验原理
1.缓冲原理
缓冲溶液具有抵抗外来少量酸、碱或稀释的干扰,而保持其本身pH基本不变的能力。缓冲溶液由共轭酸碱对组成,其中共轭酸是抗碱成分,共轭碱是抗酸成分,缓冲溶液的pH可通过亨德森-哈塞尔巴赫方程计算。 pH = pKa + lg
pH = pKa + lg 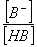
在配制缓冲溶液时,若使用相同浓度的共轭酸和共轭碱,则它们的缓冲比等于体积比。 pH = pKa + lg 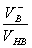
配制一定pH的缓冲溶液的原则:选择合适的缓冲系,使缓冲系共轭酸的pKa尽可能与所配缓冲溶液的pH相等或接近,以保证缓冲系在总浓度一定时,具有较大的缓冲能力;配制缓冲溶液要有适当的总浓度,一般情况下,缓冲溶液的总浓度宜选在0.05~0.2mo1/L之间;按上面简化公式计算出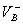 和
和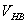 的体积并进行配制。
的体积并进行配制。
三、仪器和药品
仪器: 精密pH试纸,pHs-3C型酸度计,玻璃电极或pH复合电极,塑料烧杯,温度计。
试剂:0.10mol/L的HAc、NaAc、NaOH、HCl溶液,0.20mol/L的Na2HPO4、KH2PO4溶液,1%HCl溶液,1%NaOH溶液待测pH溶液,饱和氯化钾溶液。
pH=4.01的标准缓冲溶液:称取在110℃烘干的分析纯邻苯二甲酸氢钾10.21g,溶于蒸馏水中,再定容至1000mL。
pH=6.86的标准缓冲溶液:称取在110℃烘干的分析纯磷酸二氢钾3.39g和磷酸二氢钠3.53g,溶于蒸馏水中,再定容至1000mL。
pH=9.18的标准缓冲溶液:称取分析纯硼砂3.81g,用蒸馏水溶解后定容至1000mL。四、内容及步骤
1. 缓冲溶液的配制
(1)计算配制100mL pH=5.00的缓冲溶液需要0.1mol/L HAc溶液和0.1moI/L NaAc溶液体积(已知HAc的pKa=4.75)。根据计算出的用量,用吸量管吸取两种溶液置于100mL烧杯中,混匀,用酸度计测定其pH。若pH不等于5.00,可用几滴0.01moI/LNaOH或0.lmol/L NaAc溶液调节使溶液的pH为5.00后,备用待测。
(2)计算配制pH=8.00的缓冲溶液100mL需要的0.2mol/L Na2HPO4和0.2mol/L KH2PO4溶液的体积(H3PO4的pKa2=7.21)。根据计算用量,用碱式滴定管放取Na2HPO4溶液,用吸量管吸取KH2PO4溶液置于100mL烧杯中,混匀,用酸度计测定其pH。若pH不等于8.00,用几滴0.01mol/L NaOH或2mol/L KH2PO4溶液调节至8.00后,备用待测。
2. 缓冲溶液的性质
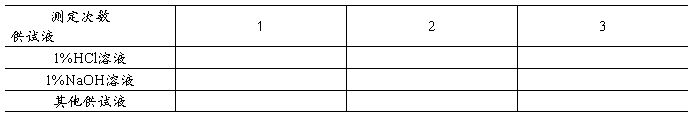
(1)缓冲溶液的抗酸作用:取三支试管,分别加入3mL上述配制的pH为5.00、8.00的缓冲溶液和蒸馏水,各加入2滴0.10mol/L HCl溶液,用酸度计或精密pH试纸测定其pH,并解释实验现象。
(2)缓冲溶液的抗碱作用:取三支试管,分别加入3mL上述配制的pH为5.00、8.00的缓冲溶液和蒸馏水,各加入2滴0.10mol/L NaOH溶液,用酸度计或精密pH试纸测定其pH,并解释实验现象。
(3)缓冲溶液的抗稀释作用:取四支试管,分别加入0.5mL上述配制的pH为5.00、8.00的缓冲溶液、0.10mol/L的NaOH、HCl溶液,各加入5mL蒸馏水,振荡试管,用酸度计或精密pH试纸测定其pH,并解释实验现象。
五、实验结果记录与计算
1.缓冲溶液的性质

2. pH计的使用
六、思考题:
1. 使用pH计应注意哪些事项?
2. 标定后,在什么情况下必须应重新标定?
教师评语: 年 月 日
