注意!!!
本实验报告参考仅供参考,请不要简单抄袭,否则退回重写
同学间亦不要互相抄写,内容雷同者,记零分
实验一气相色谱定性分析
(实验报告不得直接粘贴图片数据,需自己抄写)
一、实验目的:
1.熟悉仪器和基本操作
2.练习基于色谱图的基本计算;
2.练习基于保留值和用已知物对照的的定性分析方法。
二、实验原理:
(自己书写)
三、仪器和试剂
(自己书写)
四、实验步骤
(自己书写)
五、结果与数据处理
1、色谱图
(从下列图表中选择自己需要的,数据是多次实验的结果,自己选择适合自己的,不必全部使用)
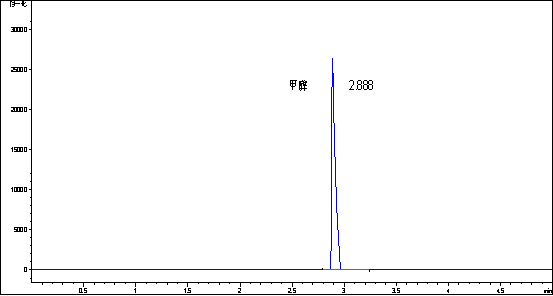
图1:纯甲醇的色谱图
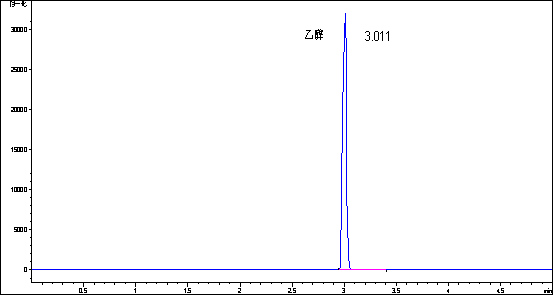
图2:纯乙醇的色谱图
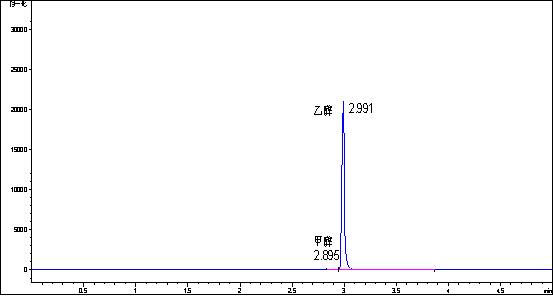
图3:白酒的色谱图
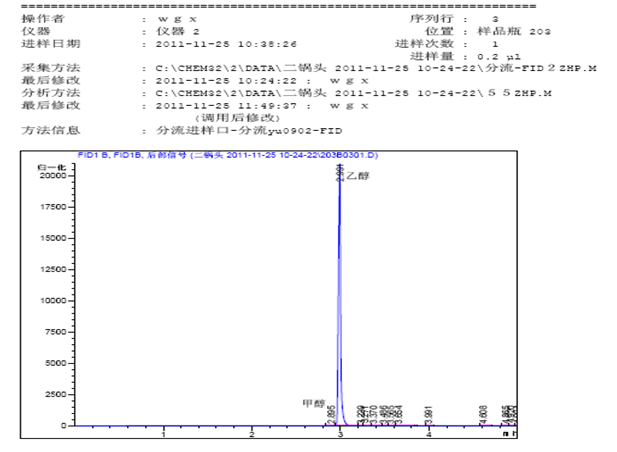
图4:白酒的色谱图(原件供参考)
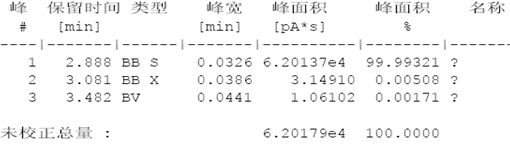
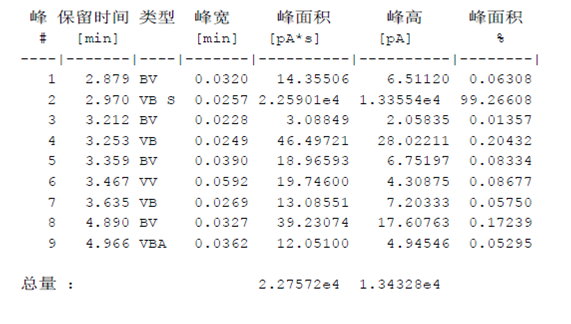
图5:白酒的数据(参考数据)
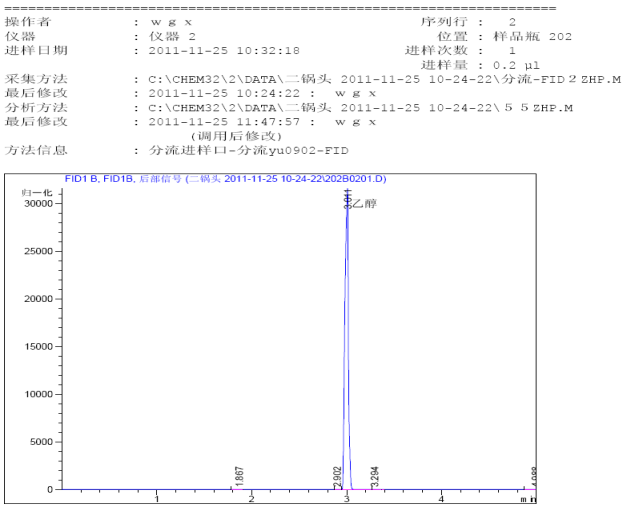
图6:白酒的色谱图(原件供参考)
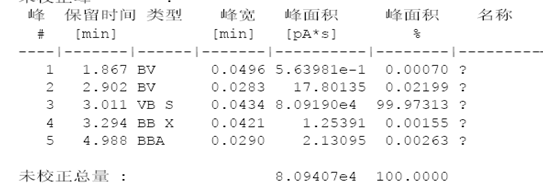
图7:白酒的数据(参考数据)
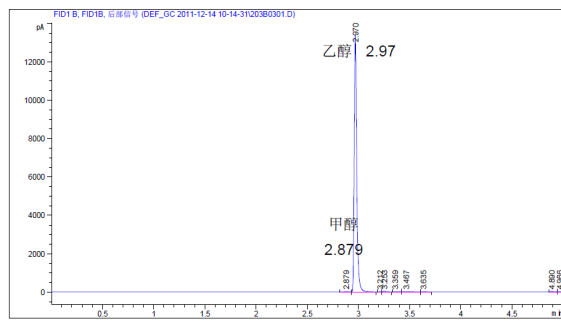
2、分析
(自己书写)
六、讨论
(自己书写)
实验二 苯系物的高效液相色谱法分析
(实验报告不得直接粘贴图片数据,需自己抄写)
一、实验目的
(以下内容仅供参考,具体内容自己写)
1. 掌握高效液相色谱仪器的构造及基本使用方法。
2. 理解和掌握归一化法对组分含量的测定。
二、基本原理
(以下内容仅供参考,具体内容自己写)
采用非极性的十八烷基键合相为固定相和极性的甲醇-水溶液为流动相的反相色谱分离模式特别适合于同系物如苯系物的分离。苯系物具有共轭双键,但因共轭体系的大小和极性不同,因而在固定相和流动相之间的分配系数不同,导致在柱内的移动速率不同而先后流出柱子。苯系物在紫外区有明显的吸收,可以利用紫外检测器进行检测。在相同的实验条件下,将测得的未知物的保留时间与已知纯物质对照进行定性分析。
当试样中的各组分都能流出色谱柱,并在色谱图上显示色谱峰时,可用归一化法定量分析。
设试样中有n个组分,各个组分的质量分别为m1,m2,……..mn,其中组分i的质量分数wi可按下式计算:
wi= mi/m×100%= mi/m1+m2+…+mn×100%=Aifi/ A1f1+ A2f2+…Anfn×100%
fi为质量校正因子,得质量分数,Ai为峰高(峰面积)。
若个组分的f值相同,例如同系物中沸点接近的各组分,上式可简化为:
wi= mi/m×100%= mi/m1+m2+…+mn×100%=Ai/ A1+ A2+…An×100%
三、仪器及试剂
(以下内容仅供参考,具体内容自己写)
1. 高效液相色谱仪(配紫外检测器,检测波长254nm)
2. 超声波清洗机
3. 25µL平头微量注射器
4. 苯、甲苯、联苯
5. 流动相的体积配比为:甲醇:水=80:20
四、实验步骤:
(以下内容仅供参考,具体内容自己写)
1. 打开输液泵电源,仪器自检。
2. 从输液泵显示屏输入流动相流速,启动泵。
3. 打开紫外检测器电源及氘灯。
4. 打开色谱工作站及采集器电源,建立方法。
5. 用流动相冲洗色谱柱,察看基线,基线稳定进样。
6. 实验完成后按顺序关机。
五、结果与数据处理
(从下列图表中选择自己需要的,数据是多次实验的结果,自己选择适合自己的,不必全部使用)
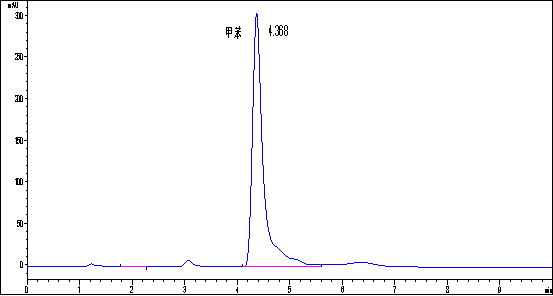
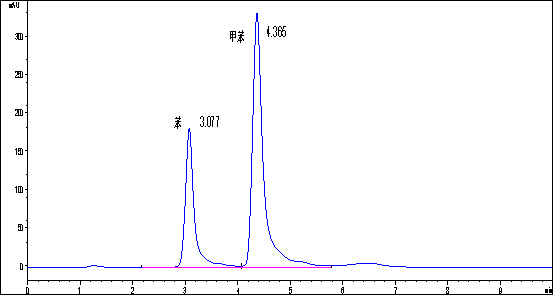
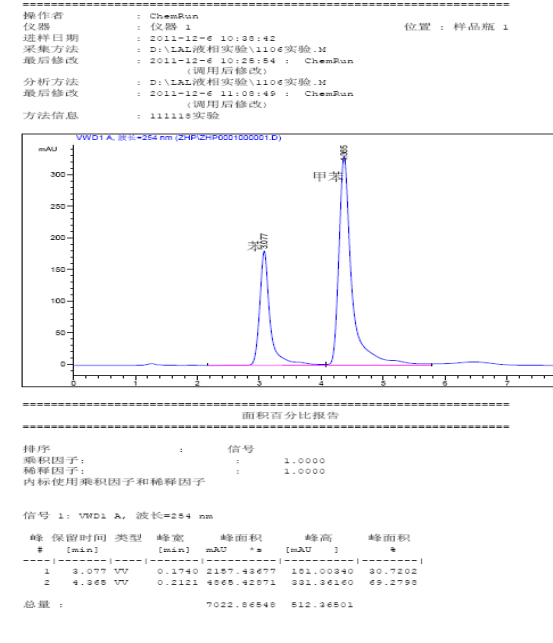
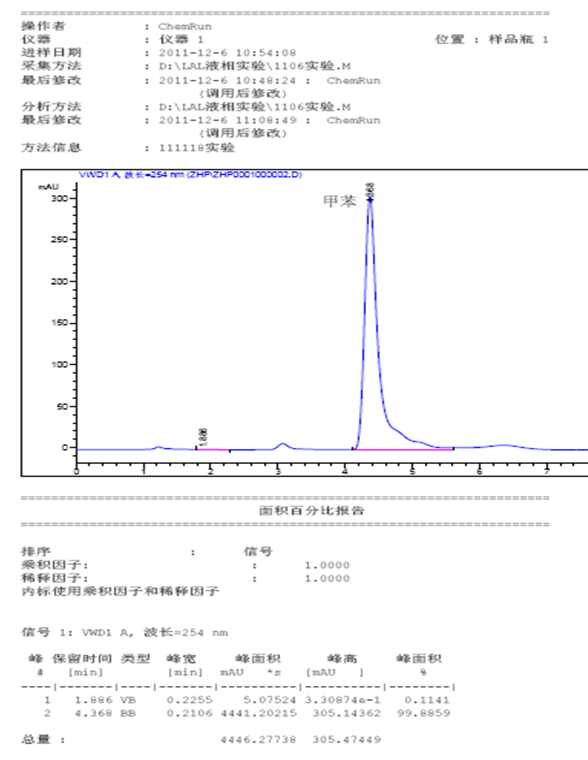
(具体内容自己写)
六、讨论
(具体内容自己写)
实验三 红外分光光度法测定苯甲酸和聚苯乙烯
一、实验目的
(以下内容仅供参考,具体内容自己写)
1、掌握红外光区分析时固态试样的制备方法。
2、了解如何从红外光谱图中识别基团以及如何从这些基团确定未知化合物的主要结构。
3、了解Perkin-Elmer 红外光谱仪的操作规程及使用。
二、红外光谱定性分析原理
(具体内容自己写)
三、红外光谱仪操作规程
(以下内容仅供参考,具体内容自己写)
1.开机
打开电源→开主机→开计算机→打开Spectrum
2.制样(KBr压片法)
取100毫克左右干燥的KBr(市售分析纯KBr可满足一般红外分析要求),1毫克左右样品在玛瑙研钵中混合研磨,使平均颗粒尺寸为2um左右。试样与KBr的比例与试样的结构有关。对于具有强极性官能团的物质样品与KBr的比例可达1:600,对于极性小的样品KBr的比例可减少。
3.压片
4. 测试
四、实验内容
(以下内容仅供参考,具体内容自己写)
1、苯甲酸红外光谱测定(KBr压片)
2、塑料薄膜的红外光谱
五、结果分析
(图可使用,以下文字内容仅供参考,具体内容自己写)
1. 苯甲酸的红外光谱图
(该图需要自己修整或重画,使美观)
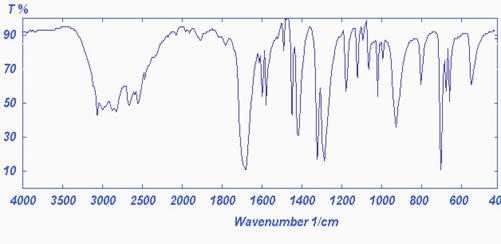
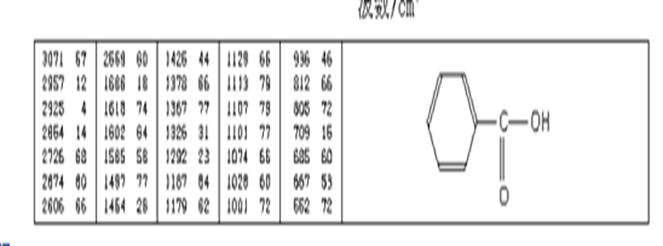
苯甲酸的各峰请对照书上的表10-3自行分析
2. 塑料薄膜的红外光谱图(聚氯乙烯)
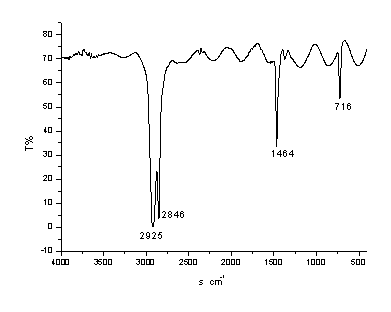
分析: 波数为2925处吸收峰为CH2反对称伸缩振动引起的
波数为2846处吸收峰为CH2 对称伸缩振动引起的
波数为1464处吸收峰为C-C单键的骨架振动引起的
波数为716处吸收峰为(CH2)n >4面内摇摆振动引起的
(以下内容仅供参考,具体内容自己写)
1. 苯甲酸:见苯甲酸红外谱图
υ=C-H(Ar)3077,3012 υC=C(Ar)1600,1582,1495,1450
υ(O-H)(形成氢键二聚体) 3000~2500(多重峰)υ(C=O) 1688
δ(O-H)935δC=O 1428δC-O-H (面内弯曲振动)1250
2. 塑料薄膜
(自己分析)
六、讨论
(具体内容自己写)
实验四、有机化合物的紫外吸收光谱
(以下内容仅供参考,具体内容自己写)
一、实验目的
1、了解紫外光谱仪的结构和原理,学习紫外光谱仪的使用方法;
2、了解有机化合物的两种主要吸收光谱:n→π *、π → π *,掌握溶剂性质和共轭效应对吸收光谱的影响。
3、掌握紫外可见分光光度计的使用。
二、基本原理
1、分子主要有四种跃迁类型,跃迁所需能量为:
σ→σ* > n→σ* ³π→π* > n→π*
π→π*跃迁:
π电子跃迁到反键π* 轨道所产生的跃迁,这类跃迁所需能量比σ→σ*跃迁小,若无共轭,与n→σ*跃迁差不多。200nm左右,吸收强度大,k在104~105范围内。
2、若体系共轭,E减小,λ增大,波长向长波方向移动。含不饱和键的化合物发生π→π*跃迁:如C=O ,C=C 等。
n→π*跃迁:
含杂原子不饱和基团(—C ≡N ,C= O )
能量最小,λ约在200~400nm(近紫外区)
三、仪器与试剂:
1.紫外可见分光光度计(T6:北京普析通用)。
2.苯,苯酚,乙醇:分析纯。
3.苯酚/水、苯/水、苯/乙醇溶液:~10-4mg/ml。
五、实验步骤
1.按实验指导讲义操作仪器;
2.以乙醇为参比,建立基线;
3.依次扫描苯酚/水、苯/水和苯/乙醇溶液的吸收光谱。
六、结果与讨论:
1.实验结果:
(该图可以使用)
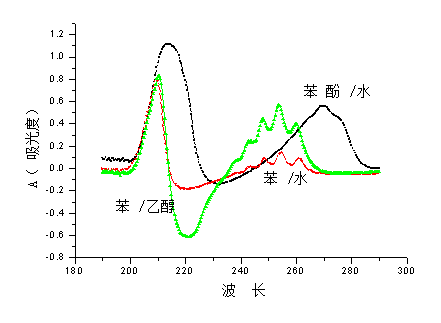
图:苯酚/水、苯/水和苯/乙醇溶液的紫外吸收光谱
2.讨论:
2.1 溶剂的影响:苯的紫外是典型的π→π*跃迁,其波长E1在185nm左右,由于仪器最低测定波长为190,所以观察不到,E2在204nm左右,可以观察到。B吸收带在乙醇作为溶剂得到的光谱中,可以清晰的观察到。水的极性比乙醇大,在以水为溶剂的光谱中,B吸收带变弱。
2.2 苯酚和水之间可以形成氢键,而且由于-OH和苯环之间的共轭作用,使得E2和B吸收带移向长波方向的变化较为明显。并且,苯的B吸收带的精细结构消失。
实验五 离子选择性电极法测定水中氟离子
(以下内容仅供参考,具体内容自己写)
一、实验目的
1、掌握电位测量的基本原理。
2、学会使用离子选择电极的测量方法和数据处理方法。
二、实验原理
氟离子选择电极是以氟化镧单晶片为敏感膜的电位法指示电极,对溶液中的氟离子具有良好的选择性。氟电极与饱和甘汞电极组成的电池可表示为:
Hg| Hg2Cl2,KCl(饱和)|| F—(试液) | LaF3|[10-3mol/L NaF 10-1mol/L NaCl,AgCl| Ag
E(电池)= E(F)— E(SCE)
=κ—RT/F lnα(F) —E(SCE)
=K - RT/F lnα(F)
=K - 0.059 lnα(F)
式中,0.059为25℃时电极的理论响应斜率,其他符号具有通常意义。
用离子选择电极测量的是溶液中的离子活度,而通常定量分析需要测量的是离子的浓度,不是活度。所以必须控制试液的离子强度。
用氟离子选择电极测量F—时,最适宜pH值范围为5.5-6.5。pH值约为6的柠檬酸盐缓冲溶液来控制溶液的pH值。柠檬酸盐还可消除Al3+,Fe3+的干扰。
三、仪器和试剂
1、离子计或pH/ mV计
2、电磁搅拌器
3、氟离子选择电极
4、饱和甘汞电极
5、氟离子标准溶液:0.100mol/L;
6、总离子强度调节缓冲剂(TISAB):0.5 mol/L(用1:1盐酸中和至pH≈6)
四、实验步骤
1、准备
将氟电极和甘汞电极分别与离子计或pH/mV计相接,开启仪器开关,预热仪器。
2、清洗电极
取去离子水50-60mL置于100mL的烧杯中;放入搅拌磁子,插入氟电极和饱和感汞电极。开启搅拌器,2-3min后,若读数大于370mV,则更换去离子水,继续清洗,直至读数不下降。
3、工作曲线法
A、标准溶液的配制及测定。
分别准确移取0.2mL、0.4mL、1.0mL、2.0mL、4.0mL、10.0mL的氟离子标准溶液置于50 mL容量瓶中,加入0.5 mol/L的TISAB缓冲溶液5.0 mL,用去离子水稀释至刻度,摇匀。
将标准溶液分别倒出部分置于塑料烧杯中,放入搅拌磁子,插入已经洗净的电极,一直搅拌,待读数不变稳定后,读取电位值。按顺序从低至高浓度依次测量,每测量1份试液,无需清洗电极,只需用滤纸沾去电极上的水珠。测量结果列表记录。
B、水样的测定
取水样25.0mL置于50mL容量瓶中,加入0.5 mol/L TISAB缓冲溶液5.0mL,用去离子水稀释至刻度并摇匀。倒出部分置于塑料烧杯中,放入搅拌磁子,插入干净的电极进行测定,按操作A中的测定步骤方法读取稳定电位值。
五、结果与数据处理
1、用测量出的系列标准溶液的数据,绘制标准曲线。
2、使用标准曲线根据水样测得的电位值,计算出F-的浓度,再换算得到水样中F-的实际含量。
注意表格的书写格式,表号表名等
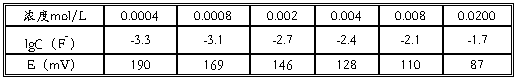
工作曲线:
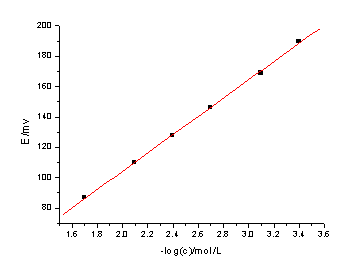
图 :离子选择电极标准曲线
注意图的书写格式,图号图名等
水样中F-离子的计算
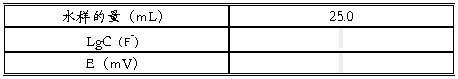
六:讨论
(具体内容自己写)
第二篇:仪器分析实验报告书写
每人一份,复印后按照要求认真写出实验报告。
液相色谱实验一 实验报告的书写要求
实验题目:液相色谱仪的结构和工作原理
实验目的:掌握液相色谱仪的结构,了解其工作原理,学会简单操作。
1、画出液相色谱仪的结构示意图
2、总结各部件的功能
3、实验过程
在本实验中,测定了丙酮在C8柱中的保留,所得色谱图如图1。写出当时的实验过程。 将色谱图裁剪下来,粘在实验报告上。
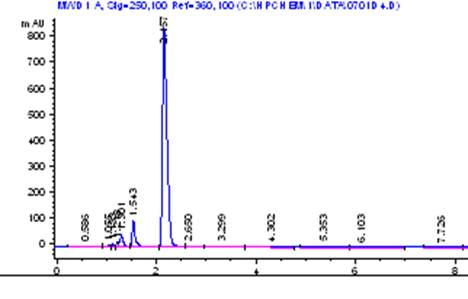
丙酮的液相色谱图(C8柱)
4 、分析为什么在主峰出现之前有时会有几个小峰。
5、实验后习题
根据实验过程和结果,总结在进行液相色谱实验时,应该注意哪些问题。
实验二
离子色谱实验 实验报告的书写要求
实验题目:离子色谱仪的结构和工作原理
实验目的:掌握离子色谱仪的结构,了解其工作原理,学会简单操作。
1 画出离子色谱仪的结构示意图
2 阐述各部件的功能
3 实验过程
在本实验中,测定了氯离子在离子交换柱中的保留,所得色谱图如下图中的第一个峰(第二个峰不要)。写出当时的实验过程。 将色谱图裁剪下来,粘在实验报告上。
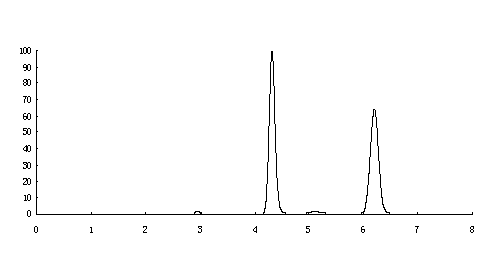
离子色谱分离SO42—离子和Cl—的色谱图
4 分析实验结果,着重说明离子色谱的分离原理
5 总结离子色谱实验过程中应该注意哪些问题。
实验三 实验报告的书写要求
实验题目:反相液相色谱对混合物的分离
实验目的:对两种有机混合物进行反相液相色谱分离,了解其分离原理,进一步熟悉液相色谱的操作。
1 对反相液相色谱的概念和定义和进行阐述。
2 总结反相液相色谱的分离机理和分离特点。
3 实验过程
在本实验中,测定了苯和甲苯混合物的保留特性,所得色谱图如图3。写出当时的实验过程。 将色谱图裁剪下来,粘在实验报告上。
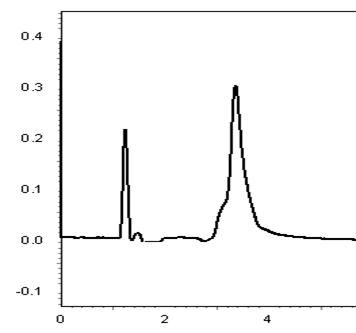
图3
4 、分析这两个峰哪个是苯?哪个是甲苯?写出理由
5、实验后习题
根据实验过程和结果,总结在用液相色谱进行混合物分离分析时,应该注意哪些问题。
 实验四
实验四
实验题目:离子色谱对混合物的分离
实验目的:对两种无机阴离子进行离子色谱分离,了解其分离原理,进一步熟悉离子色谱的操作。
1、 对离子色谱的抑制器原理进行阐述,画出抑制器工作原理图。
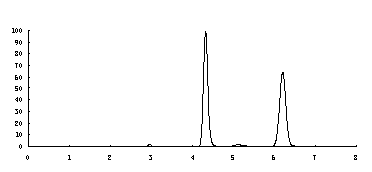
2、 实验过程
在本实验中,测定了氯离子和硫酸根离子在离子交换柱中的保留,所得色谱图如下图。写出当时的实验过程。 将色谱图裁剪下来,粘在实验报告上。
3、总结离子色谱分离规律及特点,并说明出现的两个峰哪个是硫酸跟,哪个是氯离子。
并说明出现的两个峰哪个是硫酸跟,哪个是氯离子。
实验5
实验题目:原子吸收分光光度计的结构、原理和使用
实验目的:1 了解原子吸收分光光度计的结构、原理
2 掌握原子吸收分光光度计使用方法
3 定量测定溶液中元素Cu、Cr的含量。
实验报告: 1 简述原子吸收分光光度计的结构、原理
2 祥述空心阴极灯的工作原理
3 写出实验测定过程
分析实验结果
