年度产品质量回顾分析报告
医用气态氧
回顾日期:20##年01月-20##年12月
目 录
1 概要……………………………….………………………………….…
2 回顾期限…………………………………………………….…….……
3 制造情况………………………………………………….……….……
4 产品描述………………………………………………….……….……
4.1产品工艺………………………………………….……….……..
4.2产品给药途径及适应症………………………….……….……..
4.3关键参数………………………………………….……….……..
5 产品质量标准情况…………………………………………….……….
5.1产品质量标准……………………………………………………..
5.2质量指标统计及趋势分析………………………………………..
6 生产工艺分析………………………………………………………..…
6.1关键工艺参数控制情况…………………………………….…….
6.2工艺变更情况………………….………………………………….
6.3返工与再加工……………………….…………………………….
6.4设施设备情况……………………………………………………..
7 偏差回顾………………..………………………………………………
8 超常超标回顾………………………………..…………………………
9 产品稳定性考察……………………………………..…………………
10 拒绝批次………………………………………………………..………
11 变更控制回顾……………………………………..……………………
12 验证回顾……………………………..…………………………………
13 人员情况……………………………..…………………………………
14 不良反应……………………………………………..…………………
15 产品召回、退货………………………………..………………………
16 投诉…………………..…………………………………………………
17 结论……………………………………..………………………………
附录 年度产品回顾分析表……….…………………………………………
1 概要:
根据《年度产品质量回顾分析管理规程》SMP-ZL019-00的规定,20##年1月对医用气态氧产品进行产品质量回顾分析。本报告在随机抽取12批的基础上重点对该品种进行了统计和趋势分析。
2 回顾期限:20##年01月01日-20##年12月31日
3 制造情况:
本回顾年度共生产医用气态氧产品365批,总产量为110000m3。
4 产品描述:
4.1产品工艺:以医用氧(液态)为原料,用低温贮槽将其以医用氧(贮存)。采用低温液氧泵压缩液体至空温式汽化器复温至≥00C,经管道、充装架、气瓶连接软管及防错装接头连接各气瓶,至医用氧气瓶内。
4.2产品给药途径及适应症:用于缺氧和呼吸困难等引起的临床症状。
4.3关键参数:纯度≥99.5%。
5 成品质量标准情况:
5.1 产品质量标准
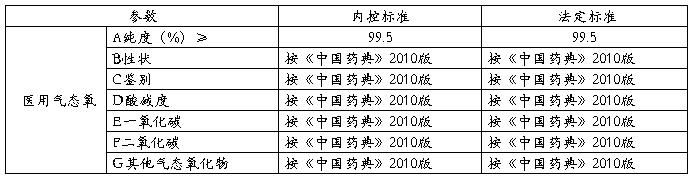
5.2质量指标统计及趋势分析
对5.1的参数项目实际检验数据实施统计与分析
A:符合《中国药典》2010版;
B:符合《中国药典》2010版;
C:符合《中国药典》2010版;
D:符合《中国药典》2010版;
E:符合《中国药典》2010版;
F:符合《中国药典》2010版;
G: 符合《中国药典》2010版;
小结:本公司医用气态氧质量标准符合法定标准。
6 生产工艺分析:
6.1关键工艺参数控制情况:液氧贮罐压力≤0.8mpa,液体纯度≥99.6%等等。
6.2工艺变更情况:无工艺变更。
6.3返工与再加工:无返工与再加工。
6.4设备设施情况
变更情况:无
维护情况:无
维修情况:本年度给低温液体充装泵电机更换轴承。
小结:本年度设备设施运行稳定。
7 偏差回顾:无严重偏差。
8 超常超限回顾:无超常超限现象。
9产品稳定性考察:
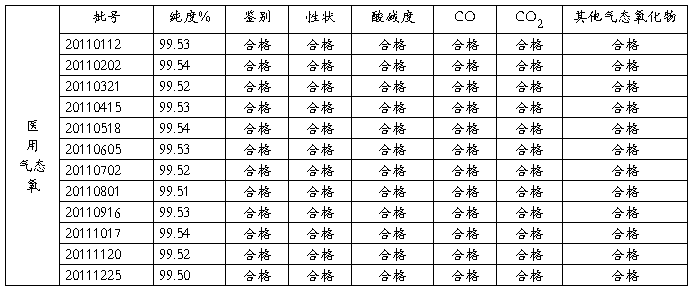
评价:本年度产品质量稳定,符合《中国药典》2010版。
10 拒绝批次:无拒绝批次。
11 变更控制回顾:无变更控制。
12 验证回顾:

评价:经过验证,确认设备、系统、工艺完全满足生产需要,可以继续使用。
13 新增人员:化验员,检验员
变更人员:化验员,检验员
人员体检及培训情况:所有人员均参加每年度的正常体检,并取得健康证。本年度组织化验员,质检员,参加黑龙江省食品药品监督管理人员培训中心举办的“药品生产企业化验员,质检员培训班”学习;
14 不良反应:无不良反应。
15 产品召回、退货:无产品召回、退货。
16 投诉:无投诉
17 结论:
综合以上分析,在回顾期20##年01月01日到20##年12月31日内:本公司所生产医用气态氧质量稳定,符合《中国药典》2010版。
附录 年度产品回顾分析表
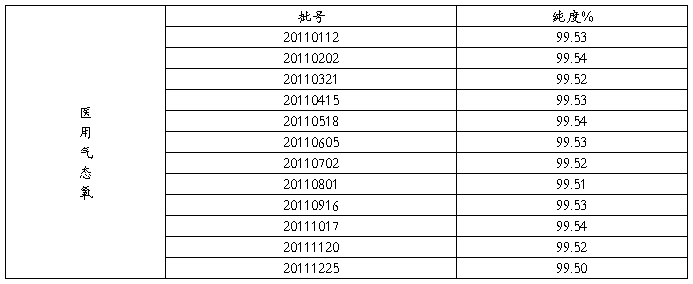
样本平均差X=0.025
样本标准偏差S=0.0369
第二篇:年度产品质量回顾分析报告模板
年度产品质量回顾分析报告模板
【说明】
一、应开展年度质量回顾分析的产品如下:
1) 常年生产、产量较大的品种;
2) 高风险品种:如注射剂类产品、毒性药品、精神药品、麻醉药品、放射性药品、血液制品、疫苗等。
二、企业应使用风险管理理念,对产品进行分类后,选取具代表性的品种或品规开展质量回顾分析。 分类原则如下:
1)生产工艺和质量控制相似、共线生产的非高风险类产品,经质量受权人批准,可按剂型或产品系列进行分类。
2)高风险产品,经质量受权人批准,可按品种或产品系列进行分类。
3)常年生产的产品,经质量受权人批准,可按剂型、产品或产品系列进行分类。
4)无菌原料药,经质量受权人批准,可按产品或产品系列进行分类。
5)该年度变更工艺或关键生产设备等变更(如注射剂灌装设备变更、除菌过滤系统变更、灭菌设备改变)的产品,经质量受权人批准,可按剂型、产品或产品系列进行分类。
6)委托加工的产品,经质量受权人批准,可按产品或产品系列进行分类。
三、本模版是企业撰写《年度产品质量回顾分析报告》的基本要求,仅供企业参考。各企业可根据实际情况,在积极学习和充分借鉴国外先进经验的基础上,不断完善相关内容。
(见附件)
年度产品质量回顾分析概要模板
【说明】
本模板是企业撰写《年度产品质量回顾分析概要》的基本要求,仅供企业参考。各企业可根据实际情况,在积极学习和充分借鉴国外先进经验的基础上,不断完善相关内容。
一、基本情况概述:
1.回顾年度的生产状况,品种、批次、数量,不合格批次、数量;
2.停产产品有哪些,停产原因;
3.生产线状况;
4.委托生产、委托检验情况;
5.哪些产品进行了年度质量回顾(哪些按品种、哪些按剂型、哪些按产品系列进行了回顾)
二、生产和质量控制情况分析评价
1.原辅料、内包材、工艺用水、直接接触药品的气体情况:稳定性、适应性、变更情况概述,不合格情况及措施详述。
2.生产工艺情况概述
(1)生产工艺过程控制、中间体及成品检测数据稳定性、趋势分析概述、评价。
(2)工艺变更情况概述:变更种类,是否进行验证等。
3.变更控制情况概述
4.偏差处理情况概述
5.成品的检验:结果、趋势分析 6.厂房设施设备情况概述:变更、维修、验证、监测等情况概述及评价。 7.稳定性考察情况概述:在考察期内的品种数量、结果趋势分析、结论。
8.验证情况概述
9.向药品监管部门的申报及批准情况概述
10.新获得注册批准的药品和注册批准有变更的药品上市后的质量状况
11.对委托生产、委托检验的情况概述
三、自检情况、接受监督检查(包括药品GMP认证检查、跟踪检查等)和抽检情况
1.次数
2.关键问题的整改措施概述
3.市场产品质量抽检情况:不合格情况、原因分析、处理情况
四、产品不良反应情况概述:数量、类别、处理结果、上报情况
五、产品质量投诉、退货和不合格或产品召回:原因、处理
六、结论:
1.对产品质量的评价;
2.改进措施;
3.建议
