江苏省医疗器械生产企业质量体系考核自查表
(适用于质量体系考核标准)
一、企业基本情况
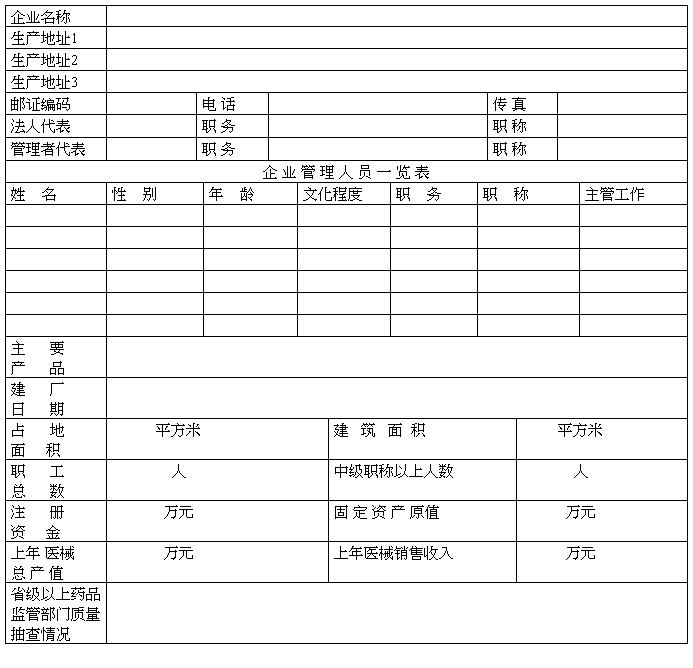
二、 企业质量体系标准及认证计划
1. 按YY/T0287-2003 + GB/T19001-2000标准建立本企业质量体系 是□ 否□
2. 按YY/T0287-2003 标准建立本企业质量体系 是□ 否□
3. 企业有______人接受了YY/T0287-2003标准的培训。取得医疗器械内审员证书的有______ 人。
4. 企业已通过何种质量体系认证______ ,证号______;如未通过质量体系认证,企业打算在____年申请质量体系认证,或尚无计划。
5. 企业通过质量体系认证的困难是:
费用问题 □ ; 无人指导 □; 管理水平低 □;
认识不够 □ ; 迫切性不大 □
三、 本次申请体系考核覆盖产品:

四、企业质量管理职责
1. 与质量有关的管理、执行、验证工作人员是否规定了质量职责并形成文件。
有□ 无□
2.企业的管理者代表是______。 或未指定□
3. 能否提供企业质量体系组织结构图。 能□ 否□
4.是否收集并保存与生产、经营有关的法律、法规、行政规章,各级质量标准。
是□ 否□
5. 企业法人代表或管理者代表是否经过了YY/T0287-2003标准的培训。
是□ 否□
五、设计控制
1.是否建立并保持设计控制和验证的形成文件的程序或相应要求。
是□ 否□
2. 在设计过程中是否进行了风险分析 是□ 否□
3. 是否建立并保存了申请注册产品的技术文件(含技术文件清单、图纸、工艺规
范) 是□ 否□
4. 是否保存了产品设计修改的记录。 是□ 否□
六、采购控制
1. 是否建立并保持控制采购过程的形成文件的程序。 是□ 否□
2. 是否建立了申请注册产品的主要材料采购清单,并确定了合格分供方。
是□ 否□
3. 申请注册产品的采购资料是否清楚、明确、齐全。 是□ 否□
七、过程控制
1. 是否确定了申请注册产品的关键过程和特殊过程(工序)并制定了相应的控制
文件或作业指导书。 是□ 否□
2. 无菌医疗器械是否按照《无菌医疗器械生产管理规范》组织生产(适用于无菌
产品)。 是□ 否□
3. 是否具备申请注册产品所需的设备、工装、检验仪表,并能满足产品制造过程
的要求。 是□ 否□
4. 参加产品的施工制造人员是否具备相应资格或经过针对性的培训。
是□ 否□
5. 是否确定了申请注册产品过程检验的内容、规程和记录。 是□ 否□
6. 是否对申请注册产品的作业环境,产品清洁作出规定。 是□ 否□
7. 是否建立了用于申请注册产品安装、查验的技术资料和接受准则。
是□ 否□
8.是否规定了申请注册产品生产过程控制中应形成的记录。 是□ 否□
9.是否对申请注册产品的可追溯性范围和程度进行了确定。(材料、元件、过程
和去向)。 是□ 否□
10.现场能否看到产品标识(包括最终产品的标签)及检验试验状态的标识。
是□ 否□
八、产品检验和试验
1. 是否设有专职的检验试验机构,并规定了其职责和权限。检测记录是否有检验
人员和复核人员签字。 是□ 否□
2. 是否建立了进行检验和试验,形成文件的程序。 是□ 否□
3. 是否进行进货检验和验证。 是□ 否□
列出进货检验和验证规程名称_____________________________________
4. 是否进行过程检验。 是□ 否□
列出过程检验的检验规程、名称___________________________________
5. 最终产品的检验试验是否覆盖了该产品适用标准中全部出厂检验项目。
是□ 否□
6. 上述检验试验记录及最近一次型式试验报告是否保存。 是□ 否□
7. 企业有无相应的测试设备。 是□ 否□
8.企业是否建立并实施了对检验、测量和试验设备进行控制、校准和维护的
规定文件。 是□ 否□
九、其它方面
1. 企业是否定期对产品质量及质量管理工作进行审核,评审和评价(适用于重新
注册)。 是□ 否□
2. 是否保留了前款评价活动的记录(适用于重新注册)。 是□ 否□
3. 是否对不合格品如何评价处理作出规定。 是□ 否□
4. 是否按一定程序处理顾客投诉并保留记录(适用于重新注册)。
是□ 否□
5. 有无实施纠正和预防措施的规定文件。 是□ 否□
十、企业对自查结果的判定意见:
(法人代表签字并加盖企业印章)
年 月 日
第二篇:质量体系总结
×××年质量体系运行情况工作总结
×××年×××部门坚持“质量第一、顾客满意、科技创新、持续改进”的质量方针,以保障全所科研日常管理工作,维系拓宽各种项目申报渠道为工作思路,圆满完成了如下几个方面的重点工作:
一、完善内部管理,构建质量管理体系文件标准化体系。
1.为进一步确保文件和技术资料的完整性和保密性,购置了文件柜,并专人负责管理。做到及时登记整理,及时归档。
2.严格执行科研项目和研究经费管理制度,依据《所创新基金管理办法》、《所创新基金管理条例》、《所创新基金奖励办法》对所内科研项目进行立项、中期检查、成果鉴定、获奖奖励工作,并配合产业化基地建设组织完成项目的成果推广。
3.从合同履约率,顾客满意率和组织开发研制自主创新产品三方面努力完成×××部门质量分目标,为×××年完成全所质量目标的奠定良好的基础。
二、所内科研项目管理
严格执行科研项目和研究经费管理制度,依据《所创新基金管理办法》、《所创新基金管理条例》《所创新基金奖励办法》对所内科研项目进行立项、中期检查、成果鉴定、获奖奖励工作,并配合产业化基地建设组织完成项目的成果推广。
×××年继续实施对科研项目的监督检查管理,我所在研项目分布情况如下:聚氨酯研究部8项,精细研究部7项,橡胶助剂研究部3项。汇总各研究部在研项目进展情况,掌握在研项目实施概况,为
所技术委员会提供决策依据。
三、承担国家、省、市及企业委托项目的组织管理
1 项目申报及立项完成情况
组织完成了省科技厅、太原市科技局×××年项目申报和考察工作,其中申报省级项目3项,市级项目1项,申报科技奖励2项
2、申请基础设施改造、仪器设备购置情况
申请省属科研院所技术开发实验室建设项目《山西省精细化工技术开发实验室》经费预算;申请省科技厅大型仪器设备改造项目经费预算;申请省财政厅中央补助地方科技基础条件专项资金,通过招投标完成了扫描电镜、差热分析仪的采购工作;申请太原市科技局市级工程技术中心科研基础设施升级改造项目,配置的4台仪器设备已经投入使用。
3、项目验收、成果鉴定、申请专利授权及获奖情况
圆满完成中石化委托项目验收评议工作;组织完成2个项目通过省科技厅组织的成果鉴定,前者鉴定结论达到国际先进水平,后者达到了国内领先水平。
×××年组织了7项专利申请,其中6项发明专利,1项实用新型,目前1项发明专利获得受理通知书,其余正进行初步审查。 “××ד项目获得×××年年度太原市科技局优秀科技项目三等奖;“×××”项目获得×××年度山西省科技进步三等奖
四、质量目标完成情况
1. ×××年我所承担的省、市科研项目共12项(包括以往项目),
目前已经完成结题验收或成果鉴定的6项(包括以往项目),准备结题2项,继续研发的4项,所有承担的项目已经按规定合同完成或正在完成,合同履约率达到100%。
2.根据上级对我所承担项目提出的要求和结题项目的验收结论判断,都达到了预期目标,符合验收条件,圆满完成验收,因此顾客满意率和顾客意见处理率都达到了100%。
3. ×××年我所在研项目总数达到了22项,已经完成结题验收或成果鉴定的5项,签订技术转让合作协议1项,本所产业化基地进行成果转化推广项目2项,因此圆满完成每年组织开发3种具有自主知识产权、技术含量高、附加值高的新产品的质量目标。
通过总结与回顾,×××部门的质量管理虽然取得一定的成效,但是仍然存在着不少问题,以后的工作中应从以下几方面加强管理:加强内部沟通与协调,加强在研项目的日常检查和完结验收,及时发现问题解决问题;加强对外联系,密切关注政府重点扶持方向,拓宽申报项目渠道;主动寻求市场信息和需求,为我所科研创新,持续改进提供更有价值的决策和依据。
