药品、医疗器械企业反商业贿赂承诺书
为认真贯彻落实中央纪委六次全会和国务院第四次次廉政工作会议精神,认真开展治理商业贿赂,加强药品、医疗器械市场信用体系建设,维护市场公平竞争,保证人民群众用药用械安全有效。本企业承诺如下:
1.严格依照《药品管理法》、《医疗器械监督管理条例》及国家有关法律、法规合法经营,保证经营的药品、医疗器械安全、有效;
2.坚决抵制制售假冒伪劣药品、医疗器械,绝不销售假劣及过期失效、霉变的药品、医疗器械,发现假冒伪劣药(更多精彩文章来自“秘书不求人”)品、医疗器械后,及时向有关部门举报;
3.积极参与药品、医疗器械市场信用体系的建设,建立完善药品、医疗器械安全信用档案,如实申报企业及主要负责人的资格资质信息、药品(医疗器械)质量安全信息和经营活动中的相关信用信息,接受食品药品监督部门的信用评级考核和分类管理,同意向社会公示本企业的所有优良或不良经营行为、奖惩记录,自觉遵守药品、医疗器械安全信用档案管理规章制度,共同树立信用自律的道德观念和行业风尚;
4.销售药品医疗器械的过程中,不以各种名义给予医疗机构、医务人员回扣、提成等财物;
5.原料采购、广告宣传和参与药品、医疗器械投标竞标过程中,不采取非正常手段获取商业机会或商业利益;
6.药品、医疗器械审评、认证发证、检验检测等环节中,不采取非正常手段获得准入资质;
7.接受食品药品监管部门的监督过程中,不以各种名义给予食品药品监管部门及其工作人员现金、有价证券和支付凭证。
我(公司)已对本责任书内容有了全面了解,本人同意上述承诺约定并保证严格遵照执行。以签字为证。
签名: 时间:
第二篇:药品批发企业药品、医疗器械及非药品验收标准
药品验收的基本标准
药品的验收包括:包装质量验收、外观质量验收、有关证明文件的验收。
一、包装质量验收:
药品的包装分内包装与外包装,内包装是指直接与药品接触的包装(如安瓿、铝箔等),内包装应能保证药品在生产、运输、贮藏及使用过程中的质量并便于医疗使用,药品内包装材料、容器的更改,应根据所选用药包材的材质,做稳定性试验,考查药包材与药品的相容性。外包装是指内包装以外的包装,按由里向外分为中包装和大包装、外包装应根据药品的特性运用不易破损的包装,以保证药品在运输、贮藏、使用过程中的质量。
1、首先检查包装箱是否牢固、干燥、封签、封条有无破损。
2、再检查包装箱有无渗液、污损及破损,若影响药品质量和正常销售,应即时拒收。
药品的标签分内包装标签与外包装标签,按国家药监局23号令要求,药品的包装、标签及说明书必须按国家药监局规定的要求印制,其文字及图案不得加入任何未经审批同意的内容。
3、大包装标签应注明药品名称、规格、贮藏条件、生产日期、生产批号、有效期、批准文号、生产企业、包装数量、运输注意事项等。
4、中包装标签应注明药品名称、主要成份、性状、适应症或功能主治、用法用量、不良反应、禁忌症、规格、贮藏、生产日期、生产批号、有效期、批准文号、生产企业等内容,若由于尺寸原因,中包装标签不能全部注明的,均应注明“详见说明书”字样。
5、内包装标签根据其尺寸的大小,尽可能包含药品名称、适应症或者功能主治、用法用量、规格、贮藏、生产日期、生产批号、有效期、生产企业等标示内容,由于包装尺寸的原因而无法全部标明上述内容的,可适当减少,但必须标注药品名称、规格及生产批号,请注意药品的内包装是指直接接触药品的包装(如按瓿、铝箱板等)并不是指最小销售单元,有很多厂家误以为只要在最小销售单元如盒上注明品名、规格、批号即可,而没有理解为内包装,所以造成每板、每支、每小瓶上未注明品名、规格、批号,这也是不对的,但是按国药监注[2001]482
号文“关于印发《药品包装、标签规范细则(暂行)》的通知,中药蜜丸蜡壳可以只标注药品名称,如安宫牛黄丸。
6、药品的每个最小销售单元的包装必须按规定印有或贴有标签并附说明书。
7、包装标签有效期的表达方法,按年月顺序,其具体表述形式应为:有效期至×年×月,按国药监注[2001]482号文规定,年份要用四位数字表示,1至9月份数字前须加0以两位数表示月份。
8、麻醉药品、精神药品、医疗用毒性药品、放射性药品等特殊管理的药品、外用药品、非处方药品在其大包装、中包装、最小销售单元和标签上必须印有符合规定的标志,其中麻醉药品、精神药品、医疗用毒性药品、放射性药品必须双人验收,在验收中必须注意上述品种的标志是否与国家药监局的规定相符。
9.OTC品种,红色OTC为甲类非处方药,绿色OTC为乙类非处方药,若印刷为单色,则应文字注明甲类、乙类。
10.




间;

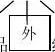
中间一个“放”字,图案黄红相间;
11、药品的商品名必须经国家药监局批准后方可在包装、标签上使用商品名不得与通用名同行书写,应分行,商品名字体以单字面积计不得大于通用名称所用字体的二分之一。注册商标必须在标签或包装上标明“注册商标”字样或标明注册标记:“注”或R加一圆圈,应当印刷在药品标签的边角,含文字的,其字体以单字面积计不得大于通用名称所用字体的四分之一。正在办理注册的标注“TM”, 禁止使用未经注册的商标以及其他未经国家食品药品监督管理局批准的药品名称。
12、凡在中国境内销售和使用的药品,包装、标签所用文字必须以中文为主。
13、药品的每个整件包装中,应有产品合格证,合格证的内容一般包括药品的通用名称、规格、生产企业、生产批号、化验单号、检验依据、出厂日期、包装人、检验部门和检验人员签章。
14、目前有四种药品包装国家已明文规定被淘汰:软木塞、铅锡管、口服液的
易折安瓿、冻干粉的安瓿包装。
15、根据药品说明书上的[功能主治]或[适应症]与药品最小销售单位包装盒上的[功能主治]或[适应症]相比较,包装盒上[功能主治]或[适应症]内容不能超过说明书,包装盒主体展示面上的适应症内容或宣传疗效也不能超过说明书内容。
16、核实药品的生产日期、有效期至,应与说明书上的有效期相符。
17、注意药品包装、标签、说明书的贮藏条件是否一致。
18、对于包装上打有曾用名的品种,应予拒收,特殊情况,应查询后方可进仓销售。
19、药品组合包装的验收:
药品组合包装是指两种或两种以上具有独立的适应症和用法用量的药物制剂组成的包装。
*药品组合包装的名称表述为“X/Y/Z组合包装”,其中XYZ分别代表各制剂的通用名称
*药品组合包装标注的有效期应为各制剂中最短的有效期。
22、药品注射剂与一次性使用注射器或输液器的包装、药品注射剂与其专用溶媒的包装不属于药品组分包装,但包装中涉及的药品、注射器、溶媒必须已获注册,也就是验收过程中药品包装、说明书上要标示其涉及药品、注射器、溶媒的注册证号或注册文号,而且包装中的一次性使用注射器、输液器也必须在灭菌有效期内。
23、按照国家药监局24号令要求,20xx年6月1日前批准注册且20xx年6月1日前生产出厂的药品,其说明书和标签符合国家药监局23号令要求的,可在药品有效期内销售使用。20xx年6月1日起生产出厂的所有药品,其说明书应符合国家药监局24号令要求:
*药品生产企业生产供上市销售的最小包装必须附有说明书。
*药品说明书和标签中的文字应当清晰易辨,标识应当清楚醒目,不得有印字脱落或者粘贴不牢等现象,不得以粘贴、剪切、涂改等方式进行修改或者补充。
*药品说明书应当列出全部活性成份或者组方中的全部中药药味。注射剂和非处方药还应当列出所用的全部辅料名称。药品处方中含有可能引起严重不良反应的成份或者辅料的,应当予以说明。
*药品说明书核准日期和修改日期应当在说明书中醒目标示。
*药品的内标签应当包含药品通用名称、适应症或者功能主治、规格、用法用量、生产日期、产品批号、有效期、生产企业等内容。包装尺寸过小无法全部标明上述内容的,至少应当标注药品通用名称、规格、产品批号、有效期等内容。
*药品外标签应当注明药品通用名称、成份、性状、适应症或者功能主治、规格、用法用量、不良反应、禁忌、注意事项、贮藏、生产日期、产品批号、有效期、批准文号、生产企业等内容。适应症或者功能主治、用法用量、不良反应、禁忌、注意事项不能全部注明的,应当标出主要内容并注明“详见说明书”字样。
*同一药品生产企业生产的同一药品,药品规格和包装规格均相同的,其标签的内容、格式及颜色必须一致;药品规格或者包装规格不同的,其标签应当明显区别或者规格项明显标注。
同一药品生产企业生产的同一药品,分别按处方药与非处方药管理的,两者的包装颜色应当明显区别。
*对贮藏有特殊要求的药品,应当在标签的醒目位置注明。
*药品标签中的有效期应当按照年、月、日的顺序标注,年份用四位数字表示,月、日用两位数表示。其具体标注格式为“有效期至XXXX年XX月”或者“有效期至XXXX年XX月XX日”;也可以用数字和其他符号表示为“有效期至XXXX.XX.”或者“有效期至XXXX/XX/XX”等。
预防用生物制品有效期的标注按照国家食品药品监督管理局批准的注册标准执行,治疗用生物制品有效期的标注自分装日期计算,其他药品有效期的标注自生产日期计算。
有效期若标注到日,应当为起算日期对应年月日的前一天,若标注到月,应当为起算月份对应年月的前一月。
*药品通用名称和商品名称的命名原则,应与药品批准证明文件的相应内容一致。
*药品通用名称应当显著、突出,其字体、字号和颜色必须一致,并符合以下要求:
——对于横版标签,必须在上三分之一范围内显著位置标出;对于竖版标签,必须在右三分之一范围内显著位置标出;
——字体颜色应当使用黑色或者白色,与相应的浅色或者深色背景形成强烈反差;
——除因包装尺寸的限制而无法同行书写的,不得分行书写。
*药品商品名称不得与通用名称同行书写,其字体和颜色不得比通用名称更突出和显著,其字体以单字面积计不得大于通用名称所用字体的二分之一。 *药品说明书和标签中禁止使用未经注册的商标以及其他未经国家食品药品监督管理局批准的药品名称。
药品标签使用注册商标的,应当印刷在药品标签的边角,含文字的,其字体以单字面积计不得大于通用名称所用字体的四分之一。
二、外观质量验收:
由验收员根据药品质量标准(说明书)中规定的性状与自己的业务知识和实践经验,来检验药品的形状、颜色、嗅味等外观质量,应根据药品说明书检查药品性状是否与说明书相符。
* 片剂:检查性状是否与说明书相符,有无明显裂片、暗斑、麻面、黑点、花斑、霉变、吸潮等。
* 胶囊剂:检查性状是否与说明书相符,硬胶囊剂检查是否有囊壳破裂、漏粉、变色、空胶囊等情况,软胶囊剂检查是否有粘连、漏油、畸形丸、破裂等情况,若有上述情况均属不合格,应特别注意漏粉、空胶囊及囊壳破裂的情况,这几种情况比较容易发生。
* 注射剂:注射用粉针需检查是否有粘瓶、吸潮、结块、色点、色块、铝盖松动等现象,注射液需检查性状、色泽是否符合要求,是否有瓶盖松动,裂纹等情况,注射液的可见异物检查每批根据实际需要开展,但通过可见异物检查可保证有白块、玻屑、纤维、异物的注射液不被使用。
* 颗粒剂:检查是否有结块、潮解、软化、破漏、胀气等现象,比较常见的有由于包装问题,颗粒剂有吸潮软化的现象,也有漏粉的现象。
* 软膏剂:检查是否有酸败、霉变、漏药等现象。
* 丸剂:检查是否大小均匀、软硬适中,异物、裂开等现象,如果对大小均匀度无把握判断,可抽样做“丸重差异”检测,即可得出结论。
* 栓剂:检查是否有霉变、酸败、干裂、软化,走油出汗等情况,一般情况下走油出汗的情况较易发生,在夏季,若说明书上注明软化通过低温保存后使用,则可根据软化的具体情况验收合格入库。
* 滴眼液:检查是否有色点、色块、纤维、沉淀、异物、漏液等现象,一般漏液情况较易发生,应着重检查。
* 糖浆剂:根据说明书的性状检查其澄清度,检查是否有沉淀、结晶析出、 酸败、霉变、渗漏等情况,一般霉变情况较易发生,特别是瓶盖附近,即便当时合格入库,以后养护也应重点养护。
* 酊水剂:检查是否有混浊、异物、异嗅、霉变、渗漏等现象,注意检查其
澄清度,一般漏液现象比较容易碰到,应特别注意检查。
以上是几种常规剂型的外观质量检查项目和检查时容易发生的问题,但如果验收员对以上项目检查有怀疑,无法直接下结论,如怀疑口服液、注射液装量不符合要求,怀疑丸剂大小均匀度不符合要求,怀疑颗粒剂水分含量超标,怀疑软膏剂装量不够等均可抽样送验收养护室检查或送药检所检验,根据检验结果下验收结论,但有些情况是靠验收员认真态度和熟练的业务知识是可以发现的,验收员在验收时一定要有这个概念:从生产厂家出来的药品不一定全部是合格品,要保证不合格品不到达消费者手中,需要流通各环节的把关,而药品验收关是一个很重要的环节。
三、有关证明文件的验收:
1、进口药品必须有《进口药品注册证》或《医疗产品注册证》、《进口药品检验报告单》或《进口药品通关单》复印件并加盖供应商质量管理机构原印章或企业公章。
按国药管注[1999]101号“关于实施《进口药品管理办法》有关问题的通知”19xx年10月1日前《进口药品注册证》到期但尚未完成换证审批的品种,其在注册证失效之日前签订了购货合同,注册证失效后6个月内到岸的货物,口岸药品检验所可继续报验,19xx年10月1日后《进口药品注册证》到期的品种,按
《管理办法》的规定,在注册证失效之日前签订了合同,注册证失效后1个月内到岸的货物,口岸药品检验所可继续报验,超过1个月的,一律不予受理检验,验收时在检查进口药品注册证有效期与进口药品检验报告书收检日期时,按此原则掌握,若进口药品注册证有效期与进口药品检验报告书收检日期不符合上述原则,则应有一个针对某批号的进口药品批件,否则其《进口药品注册证》或《进口药品检验报告单》就不合格。
《进口药品注册证》或《医疗产品注册证》与《进口药品检验报告单》或《进口药品通关单》应逐项核对,检查是否符合要求,是否有被涂改的痕迹。
2、进口预防性生物制品,血液制品应有《生物制品进口批件》复印件加盖供应商质量管理机构原印章。
3、进口药材应有《进口药材批件》复印件,并加盖供应商质量管理机构原印章或企业公章。
4、按20xx年1月15日实行的国家药监局36号令《生物制品批签发管理办法》国家对疫苗类制品,血液制品,用于血源筛查的体外生物诊断试剂以及国家药品监督管理局规定的其他生物制品,每批制品出厂销售或进口时实行强制性审查,检验和批准的制度,依据本办法规定实行批签发的生物制品未经批签发的,不得销售或进口,禁止使用,现在开展生物制品批签发的品种为人血白蛋白、重组乙型肝炎疫苗(酵母及CHO细胞的)、麻疹减毒活疫苗、口服脊髓灰质炎减毒活疫苗、卡介苗、吸附百白破联合疫苗等6种制品,那么在我公司人血白蛋白入库验收时,必须有《生物制品批签发合格证》复印件并加盖供应商质量管理机构原印章或企业公章。通关日期在20xx年1月1日以后的进口人血白蛋,应提供《进口药品注册证》、《进口药品检验报告单》或《进口药品通关单》、《生物制品批签发合格证》复印件并加盖供应商质量管理机构原印章或企业公章。
中药饮片验收原则
一、 基本要求:
对验收人员而言,应熟悉公司所经营中药饮片各品种的质量要求,其饮片鉴别特征和炮制;对中药饮片验收而言,主要对其外观性状特征、片形、表面颜色、质地、断面、气味进行验收,有无伪、劣,是否含杂质(如泥土、它物等)和非药用部位,有等级、规格规定的是否符合等级、规格要求,有无虫蛀、长霉、变
色、泛油、变味等变异现象,加工炮制是否符合当地用药习惯要求。
二、验收内容和验收细则:
(一)验收内容:
1、确定供货企业的合法性,商业公司是否有经营中药饮片的经营范围,生产企业是否具备中药饮片的生产资格,特殊管理中药材是否有生产、经营特殊中药材的生产、经营范围。
2、抽样应具有代表性,在其包装上、中、下不同部位抽取样品验收。
3、验收方法:采取眼看、手摸、耳听、鼻闻、口尝、水试、火烧等方法,必要时借用仪器进行鉴别,如显微镜、水分测定仪;核对标本、查阅工具书进行进一步证实。
4、批准文号管理的品种:冰片、人工牛黄、血竭、胆南星、滑石粉、青黛、胶类、石膏、煅石膏、芒硝、水牛角浓缩粉、松节油、龙胆草浸膏等。
5、按毒性中药饮片管理共28种:砒石(红砒、白砒)、砒霜、水银、生白附子、生附子、生川乌、生草乌、斑蝥、青娘子、红娘子、生马钱子、生巴豆、生半夏、生南星、生狼毒、藤黄、生甘遂、洋金花、闹羊花、生千金子、生天仙子、蟾酥、雪上一枝蒿、轻粉、红粉、药升丹、白降丹、雄黄。(各地卫生厅可结合当地实际增订管理品种,并报卫生部备案,验收员应对此了解)
6、对进口中药材饮片,必须按规定提供《进口中药材批件》和进口检验报告单,并加盖供货企业质量管理机构原印章。
7、验收中药材、中药饮片应有包装,并附有质量合格的标志,每批包装上,中药材标明品名、产地、供货单位,中药饮片标明品名、规格、产地、生产企业、生产日期、批号等,实施批准文号的管理的中药材和中药饮片,在包装上还应标明批准文号。
8、若属分装的中药饮片,每批包装上应标明品名、规格、产地、原生产企业、分装企业、分装日期、分装批号等,并附有质量合格的标志。
(二)验收细则:
1、应根据送货单或随货同行联核对实物,包括品名、规格、产地、生产企业(是否为合法的中药饮片生产企业)、生产日期、批号,实施批准文号管理的是否在其包装标注批准文号等内容。
2、熟悉中药材、饮片的特征和加工特点和常见的伪品。
*鉴别特征:如板蓝根的金井玉栏,苍术朱砂点,何首乌的云锦状花纹,黄芪、甘草的车轮纹,川贝、天麻、蕲蛇、羚羊角、白花蛇等都有很明显的鉴别特征,需验收员加强学习和积累。
*其炮制加工存在很大的地区差异,如苏木、乳香、没药等。
3、不同的中药饮片其验收的要求又有差异:
*矿物类中药饮片:注意颜色、质地、性状特征是否符合标准,有无炮制加工(是生品还是炮制品),如龙骨粉,生、熟石膏。
*动物类中药饮片:是否洁净,无虫伤、鼠咬、霉变,炮制加工到位,规格等级符合要求,如蛤蚧除了是正品,等级是否相符,无虫伤、长霉、断尾等现象。 *植物类中药饮片:首先注意入药部位是否符合要求、炮制是否加工到位,是否掺杂非入药部位,性状是否有异之处,再就是对药材水分、灰分、杂质等进行检查。
4、中药饮片质量必须符合《中药饮片质量标准通则(试行)》要求: *根茎、藤木、叶、花、皮类,泥沙和非药用部位等杂质不得超过2%。 *果实、种子类,泥沙和非药用部位等杂质不得超过3%。
*全草类不允许有非药用部位,泥沙等杂质不得超过3%。
*动物类、附着物,腐肉的非药用部位不得超过2%。
*矿物类、夹石,非药用部位等杂质不得超过2%。
*树脂类,杂质不得超过3%。
*需去毛、刺的药材,其末去净茸毛和硬刺的药材不得超过10%。
*中药材、中药饮片验收时不得有吸潮、变色、走油、结块、蛛网、虫霉等现 象。
5、片形规定(存在很大的地区差异):根据中国药典和当地中药炮制规范的要 求进行。
医疗器械验收基本标准
1、凭送货单(随货同行联)或入库验收通知单开始验收。
2、验收时,按要求抽取样品,根据实物进行验收,医疗器械外观性状应符合 其质量标准的要求。
3、国家对医疗器械实行分类管理:
*第一类是指,通过常规管理足以保证其安全性、有效性的医疗器械; *第二类是指,对其安全性、有效性应当加以控制的医疗器械;
*第三类是指,植入人体,用于支持、维持生命,对人体具有潜在危险,对其安全性、有效性必须严格控制的医疗器械;
医疗器械分类目录由国家药监局根据医疗器械分类规则,国务院卫生行政部门制定、调查、公布;
*三类一次性使用灭菌医疗器械有:一次性使用灭菌注射器,一次性使用输液器,一次性使用输血器,一次性使用滴定管式输液器,一次性使用灭菌注射针,一次性使用静脉输液针,一次性使用塑料血袋,一次性使用采血器
4、国家对医疗器械实行产品生产注册制度
*生产第一类医疗器械,由市药监局审查批准,并发给产品生产注册证书 *生产第二类医疗器械,由省药监局审查批准,并发给产品生产注册证书 *生产第三类医疗器械,由国家药监局审查批准,并发给产品生产注册证书
5、进口医疗器械应索取《医疗器械进口注册证书》复印件;
6、医疗器械注册证书有效期4年,在审核时一定注意注册号的编排,医疗器械注册证书有效期4年,过效期不得审核。
7、计量器具产品上必须标注MC标识;
8、 我国自20xx年7月28日起陆续公布了三批实施强制性产品认证产品目录,在第一批强制性认证产品目录中有:橡胶避孕套,因此,避孕套包装上必须标注“CCC”或“3C”标识;
9、进口医疗器械需提供《进口医疗器械注册证》复印件、《医疗器械产品注册登记表》复印件,注意审核有效性;
10、安全套包装、标签验收中一定要注意不能含有药物成分,含杀精剂的安全套不符合要求,不能有标识有杀菌、消炎、延时等作用;
11、按20xx年7月8日局令10号令《医疗器械说明书、标签和包装标识管理规定》要求:
*医疗器械说明书应当符合国家标准或者行业标准有关要求,一般应当包括以下内容:
——产品名称、型号、规格;
——生产企业名称、注册地址、生产地址、联系方式及售后服务单位; ——《医疗器械生产企业许可证》编号(第一类医疗器械除外)、医疗器械注册证书编号;
——产品标准编号;
——产品的性能、主要结构、适用范围;
——禁忌症、注意事项以及其他需要警示或者提示的内容;
——医疗器械标签所用的图形、符号、缩写等内容的解释;
——安装和使用说明或者图示;
——产品维护和保养方法,特殊储存条件、方法;
——限期使用的产品,应当标明有效期限;
——产品标准中规定的应当在说明书中标明的其他内容。
*医疗器械标签、包装标识一般应当包括以下内容:
——产品名称、型号、规格;
——生产企业名称、注册地址、生产地址、联系方式;
——医疗器械注册证书编号;
——产品标准编号;
——产品生产日期或者批(编)号;
——电源连接条件、输入功率;
——限期使用的产品,应当标明有效期限;
——依据产品特性应当标注的图形、符号以及其他相关内容。
*一些简单易用的医疗器械,按国家药监局的规定,可以省略说明书、标签和包装标识三项中的某一项或某两项;
*医疗器械说明书、标签和包装标识不得有下列内容:
——“疗效最佳”、“保证治愈”、“包治”、“根治”、“即刻见效”、“完全无毒副作用”等表示功效的断言或者保证的;
——说明治愈率或者有效率的;
——与其他企业产品的功效和安全性相比较的;
*医疗器械有商品名称的,可以在说明书、标签和包装标识中同时标注商品名称,但是应当与医疗器械注册证书中标注的商品名称一致。同时标注产品名称与商品名称时,应当分行,不得连写,并且医疗器械商品名称的文字不得大于产品名称文字的两倍;
12、产品标明的医疗器械注册证号有效期4年,验收时应注意不能是过期的注册证号;
13、消毒器械整件应有灭菌批号、灭菌日期,单包装上应注明有效期;
14、简单易用的医疗器械,按照国家药监局的规定,可以省略说明书、标签和包装标识三项中的某一项或者某两项。
非药品验收基本标准
一、 保健食品、食品的验收:
保健食品、食品的验收包括外观质量验收、包装质量(标签、说明书)验收。 验收原则:不得涉及药品的预防、诊断、治疗作用,不得涉及假药。按20xx年4月11日卫法监发[2001]109号文《卫生部关于印发健康相关产品命名规定的通知》要求,健康相关产品命名时禁止使用已经批准的药品名。不能模仿药品的包装。
1、凭送货单(随货同行联)或入库验收通知单开始验收。
2、根据实物核对其外观性状是否符合规定要求,不得有变质现象。
(一)保健食品的验收:
20xx年11月1日之前,保健食品由国家卫生部审批,《保健食品批准证书》,批准文号为:卫食健字()第()号
20xx年11月1日起,保健食品由国家药监局审批,《保健食品注册批件》批准文号为:国食健字G********
1、保健食品核准的功能一般不会超过2个。可以核准的功能有:(1)辅助降糖;(2)辅助改善记忆力;(3)促进排铅;(4)辅助降血压;(5)促进泌乳;
(6)减肥;(7)增加骨密度;(8)对胃粘膜损伤有辅助保护功能;(9)促进消化;(10)辅助降脂;(11)抗氧化;(12)清咽功能;(13)改善生长发育;
(14)改善营养性贫血;(15)通便功能;(16)调节肠道菌群;(17)祛黄褐斑;(18)改善皮肤油分;(19)缓解视疲劳;(20)祛痤疮;(21)改善皮肤水分;(22)增强免疫力;(23)提高缺氧耐受力;(24)对化学性肝损伤有辅助保护;(25)改善睡眠;(26)缓解体力疲劳;(27)对辐射危害有辅助保护功能。
2、验收保健食品时,一定要注意审核其成份是否符合要求。
——保健食品禁用物品名单:八角莲、八里麻、千金子、土青木香、山莨菪、川乌、广防己、马桑叶、马钱子、六角莲、天仙子、巴豆、水银、长春花、甘遂、生天南星、生半夏、生白附子、生狼毒、白降丹、石蒜、关木通、农吉痢、夹竹桃、朱砂、米壳(罂粟壳)、红升丹、红豆杉、红茴香、红粉、羊角拗、羊踯躅、丽江山慈姑、京大戟、昆明山海棠、河豚、闹羊花、青娘虫、鱼藤、洋地黄、洋金花、牵牛子、砒石(白砒、红砒、砒霜)、草乌、香加皮(杠柳皮)、骆驼蓬、鬼臼、莽草、铁棒槌、铃兰、雪上一枝蒿、黄花夹竹桃、斑蝥、硫磺、雄黄、雷公藤、颠茄、藜芦、蟾酥。;
3、包装、说明书、样品的验收:
*保健食品标注的内容概括起来说有12项:
3.1.名称 保健食品应使用表明食品真实属性的准确名称。在使用“新创名称”、“奇特名称”、“牌号名称”或“商品名称”时,应同时使用表明食品真实属性的准确名称或经批准认可表明功能作用的名称,如延缓衰老食品、减肥食品、抗疲劳食品等。不得以药品名称或类似药品的名称命名产品,并不得只标注外文缩写名称、代号名称或汉语拼音名称。按20xx年7月1日起实行的《保健食品注册管理办法(试行)》明确规定,保健食品名称不得使用明示或暗示治疗作用的文字。
3.2保健食品标志与保健食品批准文号:保健食品标志与保健食品批准文号应并排或上下排列标于“主要展示版面”的左上方。保健食品的批准文号分为上下两行,上行为“卫食健字()第()号”,下行为“中华人民共和国卫生部批准”或“国食健字G********”下行为“国家食品药品监督管理局批准”。
3.3.配料表(配料)根据标准要求,保健食品的配料、添加剂、营养强化剂等应标明具体名称。
3.4.功能成分和营养成分表 保健食品中的功能成分和营养成分应列表标明每 100g 或 100ml保健食品中起主导作用和辅助作用功效的成分含量。含有活性生物体(如活性乳酸菌等)的保健食品,应标明每 100g 或 100ml 各种活性生物体的数量。现代科学技术难以确定功效成分的产品,应标明起主导作用和辅助作用的原料名称及加入量。按有关规定,应列表标明营养成分(营养素)的含量。
3.5.保健功能 标明的保健功能应与批准确认的功能相一致,不得描述、介绍或暗示产品“治疗”疾病作用。
3.6适宜人群:与批件一致,当保健食品不适宜某类人群时,应在“适宜人群”之后标示不适宜使用的人群,其字体应略大于“适宜人群”的内容。
3.7.净含量及固形物含量 在标注中应按规定标明净含量及固形物含量。
3.8.制造者的名称和地址 应标明保健食品制造、包装或分装单位经依法登记注册的名称和地址。进口保健食品可以免予标明制造、包装或分装单位经依法登
记注册的名称和地址,但应标注原产国或地区(指香港、澳门、台湾)的名称,以及总经销或代理商在国内依法登记注册的名称和地址。
3.9.生产日期、保质期/保存期 应按年月日顺序标明保健食品的生产日期。同时根据规定标明保健食品的保质期/保存期。
3.10.贮藏方法(条件)如果保健食品的保质期或保存期与贮藏方法(条件)有关,必须标明贮藏要求。
3.11.食用方法 应按规定标明产品的食用方法,标明产品的食用对象(即适用于的特定人群)和每日或每次的适宜食用量(应按产品适于的特定人群分别标注)。
3.12.执行标准:必须标示所执行的标准代号和编号
(二)食品的验收:
1、食品名称不得使用已有药品名称;
2、食品的最小销售单元包装上必须有生产方的卫生许可证号、品名、生产日期、保质期;
3、验收食品时,一定要注意审核其成份是否符合要求。
—— 保健食品禁用物品名单:八角莲、八里麻、千金子、土青木香、山莨菪、川乌、广防己、马桑叶、马钱子、六角莲、天仙子、巴豆、水银、长春花、甘遂、生天南星、生半夏、生白附子、生狼毒、白降丹、石蒜、关木通、农吉痢、夹竹桃、朱砂、米壳(罂粟壳)、红升丹、红豆杉、红茴香、红粉、羊角拗、羊踯躅、丽江山慈姑、京大戟、昆明山海棠、河豚、闹羊花、青娘虫、鱼藤、洋地黄、洋金花、牵牛子、砒石(白砒、红砒、砒霜)、草乌、香加皮(杠柳皮)、骆驼蓬、鬼臼、莽草、铁棒槌、铃兰、雪上一枝蒿、黄花夹竹桃、斑蝥、硫磺、雄黄、雷公藤、颠茄、藜芦、蟾酥;
“保健食品禁用物品的名单”中提及的成分普通食品禁用。
4、对“新十类食品”(米、面、油、酱、醋、肉制品、罐头食品、乳制品、饮料、冷饮、速冻米面制品、糖、味精、方便面、饼干、膨化食品)应有蓝白相间的QS安全标示;
5、20xx年1月1日起对委托生产加工的食品,其产品的最小销售包装必须在标签和说明书的同一展示版面上,分别标注委托方和受委托方双方的单位名
称、地址和卫生许可证文号等内容;如该食品有其它企业监制,需在包装上注明。
6、蜂蜜的验收:
20xx年10月26日,《蜂蜜》(GB18796-2005)强制性国家标准正式公布。根据规定,生产企业于20xx年3月1日起、流通领域于20xx年6月1日起执行这一新标准。据悉,新《蜂蜜》标准明确界定了蜂蜜的定义,即“蜂蜜是蜜蜂采集植物的花蜜、分泌物或蜜露,与自身分泌物结合后,经充分酿造而成的天然甜物质”。标准要求:蜂蜜中不得添加或混入任何蜂蜜以外的物质,如淀粉类、糖类物质以及防腐剂、澄清剂等。在蜂蜜标识中也不能用“女人蜜”、“老人蜜”等含糊不清、误导消费者的定义或标注。蜂蜜中含有任何包括可食添加剂在内的物质的产品均不能叫蜂蜜,只能叫蜂蜜制品。新标准对蜂蜜产品名称的要求规定得十分详细,主要有以下几款:
——.符合本标准定义的产品方可称为"蜂蜜"或简称为"蜜"。
——.采用过滤工艺除去了花粉的蜂蜜应称为"过滤蜂蜜"。
——.可以在"蜂蜜"前加上表示色泽的形容词,如:白色蜂蜜。
——.如果蜂蜜主要产自一种植物或花,并具有此种蜂蜜的物理、化学和微观特性,可以在"蜂蜜"前加上这种植物或花的名称,例如:刺槐蜂蜜。
——.可以采用"液态蜂蜜"、"结晶蜂蜜"名称,表明物理状态。
——.如果蜂蜜是一种蜜蜂酿造,可以在产品名称前加上这种蜜蜂的名称,写在括号内,如:(东北黑蜂)蜂蜜。
新标准规定了蜂蜜产品等级,因此在标签上应按照标准规定标示其等级:"一级品"或"二级品"。蜂蜜刚刚从巢脾中分离出来就达到一级品水平的蜂蜜,一般是成熟蜂蜜。然而,许多蜂蜜往往是经过进一步加工才达到一级品水平的。因此,尚不能认为一级品就是成熟蜂蜜。但是二级品蜂蜜肯定不是成熟蜂蜜。
7、进口食品的验收:
自20xx年4月1日起,进口食品的标签审核与检验检疫结合进行,因此验
收进口食品时要求供应商提供加盖供应商公章的“进口检验证明文件”(加注“标签经审核合格”)复印件。
20xx年4月1日之前进口的食品,仍按要求加盖供应商公章或质管部门印鉴的《中华人民共和国出入境检验检疫卫生证书》复印件。
8、饮料酒的验收:
饮料酒是指供人们饮用且乙醇(酒精)含量在0.5%—65.0%(V/V)的饮料。包括各种发酵酒、蒸馏酒及配制酒。
——标签的基本内容与要求:
8.1酒名:必须采用表明饮料酒真实属性的专用名称。当产品标准中规定了几个名称时,可使用其中一个。
8.2配料表:饮料酒标签上必须标有配料表。配料表的标题可以用“原料”或“原料与配料”标注。如:啤酒 原料:水、麦芽、大米、酒花。
8.3酒精度:凡是饮料酒,均须标明酒精度,即乙醇含量。酒精度标注方式为:啤酒为%(m/m)或换算成%(V/V)表示。其他酒均以%(V/V)表示。
8.4原汁量
啤酒须标注原麦汁浓度(含量)。标注方式为:在数字右上角加小圆圈表示“度”,如:12度啤酒应标为“12°啤酒”。
果酒(包括葡萄酒)须标注原果汁含量。标注方式为:用百分数加括号表示,如:“苹果酒(50%)”表示含有百分之五十的原果汁。
8.5净含量:必须在标签上标明每个包装容器(瓶、罐、桶)中酒的净含量。
8.6制造者、经销者的名称和地址
8.7批号
8.8生产日期(灌装日期):标签上必须标明产品的生产日期,日期的标注顺序为年、月、日。
8.9保质期(或保存期):保质期(或保存期)超过18个月的饮料酒(全汁葡萄酒、蒸馏酒或以蒸馏酒为酒基的配制酒)可不标保质期(或保存期),其他酒必须标注保质期(或保存期)。
8.10产品标准号与质量等级
8.11产品类型(或糖度):果酒,葡萄酒和黄酒须标注类型(或糖度);如葡萄酒,类型:半干(或糖度:7.0g/L);配制酒中的露酒须标注糖度;白酒须标注香型。
二、化妆品的验收:
化妆品的验收包括外观质量验收、包装质量(标签、说明书)验收。
验收原则:不得涉及药品的预防、诊断、治疗作用,不得涉及假药。按20xx年4月11日卫法监发[2001]109号文《卫生部关于印发健康相关产品命名规定的通知》要求,健康相关产品命名时禁止使用已经批准的药品名。不能模仿药品的包装。
1、凭送货单(随货同行联)或入库验收通知单开始验收。
2、外观性状的验收应符合规定要求,不得有变质、漏液等现象。
3、化妆品通用标签规定必须标注的9大内容
*产品名称:需符合国家、行业、企业产品标准或反映化妆品真实性,要简明、易懂。在使用新创名称时,必须同时使用化妆品分类规定的名称、反映产品的真实性。产品的名称也必须标注在主视面。
*制造者的名称和地址:应标明产品制造、包装、分装者经依法登记注册的名称和地址。进口化妆品也要标明原产国名、地区名(指香港、澳门、台湾)、制造者的名称、地址或经销商、进口商、在华代理商在华依法登记注册的名称和地址。 *内装物量:要标明产品的净含量或净容量。
*日期标注:日期标注包括生产曰期、保质期、生产批号和限期使用日期,且除生产批号外都要标在产品装的可视面。
*生产企业的生产许可证号、卫生许可证号和产品标准号。
*进口化妆应表明进口化妆品卫生许可证批准文号。
*特殊用途化收品还须标注特殊用途化妆品卫生批准文号。特殊化妆品包括:育发、染发、烫发、脱毛、美乳、去斑、防晒、除臭化妆品。
*必要时要标明产品的安全警告和使用指南。
*必要时应注明满足保质期和安全性要求的储存条件。
4、许可证标识
1) 化妆品生产许可证标记为 XKl6—108—****
2) 化妆品卫生许可证标记为 (**)卫妆准字**—XK—****
3) 进口化妆品卫生许可证标记: (**)卫妆准字**—JK—****
4) 特殊用途化收品许可证标记为:(**)卫妆特字**—QG—**—****
5、按国家规定:20xx年11月1日后取得生产许可证的化妆品企业,应从准予许可之日起6个月内,完成再产品、包装、说明书上标注“QS”和编号;而在20xx年11月1日前,取得生产许可证的企业过渡时间为1年,过渡期后,市场上所有的化妆品都须加贴“QS”标识才能销售。
6、进口化妆品的验收:
自20xx年4月1日起,进口化妆品的标签审核与进口化妆品检验检疫结合进行,不再实行预先审核,因此验收进口化妆品时要求供应商提供加盖供应商公章或质管部门印鉴的“进口检验证明文件”(加注“标签经审核合格”)复印件。 20xx年4月1日之前进口的化妆品,仍按要求提供《进口化妆品卫生许可批件》复印件、《中国疾病预防控制中心环境与健康相关产品安全所检验报告》复印件。
三、消毒产品的验收:
消毒产品包括:消毒剂类、消毒器械类、卫生用品类和一次性使用医疗用品类。
消毒产品的验收包括外观质量验收、包装质量(标签、说明书)验收。 验收原则:不得涉及药品的预防、诊断、治疗作用,不得涉及假药。按20xx年4月11日卫法监发[2001]109号文《卫生部关于印发健康相关产品命名规定的通知》要求,健康相关产品命名时禁止使用已经批准的药品名。不能模仿药品的包装。
1、凭送货单(随货同行联)或入库验收通知单开始验收。
2、外观性状的验收应符合规定要求,不得有变质、漏液等现象。
3、包装、说明书、标签不得含药用成分
4、包装、说明书、标签不得宣传预防、诊断、治疗作用
5、根据卫监督发[2005]208号文“卫生部关于调整消毒产品监管和许可范围的通知”
* 自20xx年5月30日起,卫生行政部门不再将以下产品纳入消毒产品进行受理、审批、监督:
— 专用于人体足部、眼睛、指甲、腋部、头皮、鼻粘膜等特定部位的具有消毒或抗(抑)菌功能的产品;
— 口罩;
—避孕套;
* 对已获得消毒产品卫生许可批件的特定部位消毒(抑菌)功能的产品,在卫生许可批件有效期内继续生产销售,批件到期后不予换发;
* 对已获得卫生用品备案凭证的以上三类品种,自20xx年1月1起,新产品不得以消毒产品的名义销售;
* 对未获得卫生用品备案凭证的以上三类产品,20xx年6月1日起,新产品不得以消毒产品的名义销售。
6、按20xx年1月25日卫监督发[2006]29号文《卫生部关于实施<消毒产品标签说明书管理规范>有关问题的通知》要求,20xx年5月1日起生产的消毒产品使用的标签、说明书应符合《规范》的要求。
*产品名称应当符合《卫生部健康相关产品命名规定》,应包括商标名(或品牌名)、通用名、属性名;有多种消毒或抗(抑)菌用途或含多种有效杀菌成分的消毒产品,命名时可以只标注商标名(或品牌名)和属性名。
*消毒剂、消毒器械的名称、剂型、型号、批准文号、有效成分含量、使用范围、使用方法、有效期/使用寿命等应与省级以上卫生行政部门卫生许可或备案时的一致;卫生用品主要有效成分含量应当符合产品执行标准规定的范围。
*在标注生产企业信息时,应同时标注产品责任单位和产品实际生产加工企业的信息(两者相同时,不必重复标注)。
*未列入消毒产品分类目录的产品不得标注任何与消毒产品管理有关的卫生许可证明编号。
*消毒产品的最小销售包装应当印有或贴有标签。
——消毒剂最小销售包装标签应标注以下内容:产品名称;产品卫生许可批件号;生产企业(名称、地址);生产企业卫生许可证号(进口产品除外);原
产国或地区名称(国产产品除外);主要有效成分及其含量;生产日期和有效期/生产批号和限期使用日期;用于粘膜的消毒剂还应标注“仅限医疗卫生机构诊疗用”内容。
——消毒器械最小销售包装标签或铭牌应标注以下内容:产品名称;产品卫生许可批件号;生产企业(名称、地址);生产企业卫生许可证号(进口产品除外);原产国或地区名称(国产产品除外);生产日期;有效期(限生物指示剂、化学指示剂和灭菌包装物);注意事项。
——卫生用品最小销售包装标签应标注以下内容:产品名称;主要原料名称;生产企业(名称、地址、联系电话、邮政编码);生产企业卫生许可证号(进口产品除外);原产国或地区名称(国产产品除外);生产日期和有效期(保质期)/生产批号和限期使用日期;消毒级产品应标注“消毒级”字样;卫生湿巾还应标注杀菌有效成分及其含量、使用方法、使用范围和注意事项。
——抗(抑)菌剂最小销售包装标签除要标注卫生用品最小销售包装标签规定的内容外,还应标注产品主要原料的有效成分及其含量;含植物成分的抗(抑)菌剂,还应标注主要植物拉丁文名称;对指示菌的杀灭率大于等于90%的,可标注“有杀菌作用”;对指示菌的抑菌率达到50%或抑菌环直径大于7mm的,可标注“有抑菌作用”;抑菌率大于等于90%的,可标注“有较强抑菌作用”。
用于阴部粘膜的抗(抑)菌产品应当标注“不得用于性生活中对性病的预防”。 *同一个消毒产品标签和说明书上禁止使用两个及其以上产品名称。卫生湿巾和湿巾名称还不得使用抗(抑)菌字样。
*消毒产品标签及说明书禁止标注以下内容:
——卫生巾(纸)等产品禁止标注消毒、灭菌、杀菌、除菌、药物、保健、除湿、润燥、止痒、抗炎、消炎、杀精子、避孕,以及无检验依据的抗(抑)菌作用等内容。
——卫生湿巾、湿巾等产品禁止标注消毒、灭菌、除菌、药物、高效、无毒、预防性病、治疗疾病、减轻或缓解疾病症状、抗炎、消炎、无检验依据的使用对象和保质期等内容。卫生湿巾还应禁止标注无检验依据的抑/杀微生物类别和无检验依据的抗(抑)菌作用。湿巾还应禁止标注抗/抑菌、杀菌作用。
——抗(抑)菌剂产品禁止标注高效、无毒、消毒、灭菌、除菌、抗炎、
消炎、治疗疾病、减轻或缓解疾病症状、预防性病、杀精子、避孕,及抗生素、激素等禁用成分的内容;
——隐形眼镜护理用品禁止标注全功能、高效、无毒、灭菌或除菌等等的字样。
——消毒剂禁止标注广谱、速效、无毒、抗炎、消炎、治疗疾病、减轻或缓解疾病症状、预防性病、杀精子、避孕,及抗生素、激素等禁用成分内容;禁止标注用于人体足部、眼睛、指甲、腋部、头皮、头发、鼻粘膜、肛肠等特定部位等内容。
——消毒产品的标签和使用说明书中均禁止标注无效批准文号或许可证号以及疾病症状和疾病名称(疾病名称作为微生物名称一部分时除外,如“脊髓灰质炎病毒”等)。
