三、常见气体的实验室制备
1、气体发生装置的类型
(1)设计原则:根据反应原理、反应物状态和反应所需条件等因素来选择反应装置。
(2)装置基本类型:
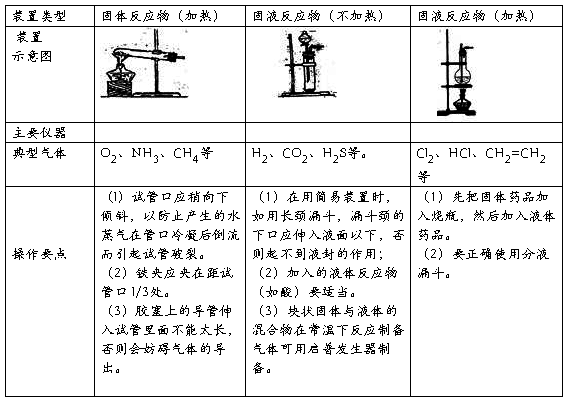
几种气体制备的反应原理
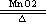 1、O2 2KClO3 2KCl+3O2↑
1、O2 2KClO3 2KCl+3O2↑
2KMnO4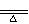 K2MnO4+MnO2+O2↑
K2MnO4+MnO2+O2↑
2H2O2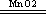 2H2O+O2↑
2H2O+O2↑
2、NH3 2NH4Cl+Ca(OH)2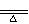 CaCl2+2NH3↑+2H2O
CaCl2+2NH3↑+2H2O
NH3·H2O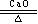 NH3↑+H2O
NH3↑+H2O
3、CH4 CH3COONa+NaOH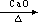 Na2CO3+CH4↑
Na2CO3+CH4↑
4、H2 Zn+H2SO4(稀)=ZnSO4+H2↑
5、CO2 CaCO3+2HCl=CaCl2+CO2↑+H2O
6、SO2 Na2SO4+H2SO4(浓)=Na2SO4+SO2↑+H2O
7、NO2 Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O
8、NO 3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O
9、C2H2 CaC2+2H2O→Ca(OH)2+CH≡CH↑
10、Cl2 MnO2+4HCl(浓)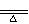 MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O
11、C2H4 C2H5OH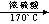 CH2=CH2↑+H2O
CH2=CH2↑+H2O
12、N2 NaNO2+NH4Cl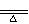 NaCl+N2↑+2H2O
NaCl+N2↑+2H2O
2、收集装置
(1)设计原则:根据氧化的溶解性或密度
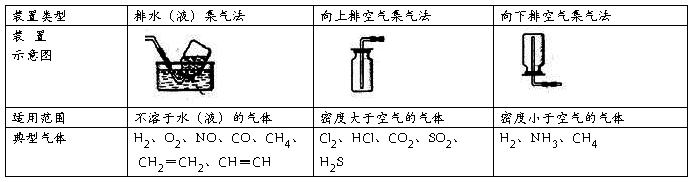
(2)装置基本类型:
3、净化与干燥装置
(1)设计原则:根据净化药品的状态及条件
(2)装置基本类型:
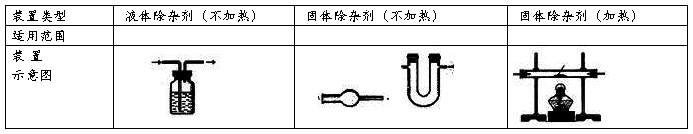
(3)气体的净化剂的选择
选择气体吸收剂应根据气体的性质和杂质的性质而确定,所选用的吸收剂只能吸收气体中的杂质,而不能与被提纯的气体反应。一般情况下:①易溶于水的气体杂质可用水来吸收;②酸性杂质可用碱性物质吸收;③碱性杂质可用酸性物质吸收;④水分可用干燥剂来吸收;⑤能与杂质反应生成沉淀(或可溶物)的物质也可作为吸收剂。
(4)气体干燥剂的类型及选择
常用的气体干燥剂按酸碱性可分为三类:
①酸性干燥剂,如浓硫酸、五氧化二磷、硅胶。酸性干燥剂能够干燥显酸性或中性的气体,如CO2、SO2、NO2、HCI、H2、Cl2 、O2、CH4等气体。
②碱性干燥剂,如生石灰、碱石灰、固体NaOH。碱性干燥剂可以用来干燥显碱性或中性的气体,如NH3、H2、O2、CH4等气体。
③中性干燥剂,如无水氯化钙等,可以干燥中性、酸性、碱性气体,如O2、H2、CH4等。
在选用干燥剂时,显碱性的气体不能选用酸性干燥剂,显酸性的气体不能选用碱性干燥剂。有还原性的气体不能选用有氧化性的干燥剂。能与气体反应的物质不能选作干燥剂,如不能用CaCI2来干燥NH3(因生成 CaCl2·8NH3),不能用浓 H2SO4干燥 NH3、H2S、HBr、HI等。
气体净化与干燥注意事项
一般情况下,若采用溶液作除杂试剂,则是先除杂后干燥;若采用加热除去杂质,则是先干燥后加热。
对于有毒、有害的气体尾气必须用适当的溶液加以吸收(或点燃),使它们变为无毒、无害、无污染的物质。如尾气Cl2、SO2、Br2(蒸气)等可用NaOH溶液吸收;尾气H2S可用CuSO4或NaOH溶液吸收;尾气CO可用点燃法,将它转化为CO2气体。
4、气体实验装置的设计
(1)装置顺序:制气装置→净化装置→反应或收集装置→除尾气装置
(2)安装顺序:由下向上,由左向右
(3)操作顺序:装配仪器→检验气密性→加入药品
典型例题
[例1]下列反应适用于实验室制氢气的是( )。
①锌与稀硫酸反应②甲烷热分解③电解稀硫酸④赤热的炭与水蒸气反应
A.只有① B.①② C.①③ D.①②④ (1994年全国高考题)
分析与解答:
实验室里制备气体要操作简单,容易分离,经济实惠,切实可行。甲烷在高温下才能分解成 H2和 C,实验室里难办到。赤热的炭和水蒸气反应生成 CO和 H2,既难反应,又难分离,难以在实验里实现。可用锌和稀硫酸反应、电解稀硫酸的方法制取氢气。本题答案为C
[例2]今有下列气体:H2、Cl2、CH4、HCl、NH3、NO、H2S、SO2,用右图装置进行实验,填写下列空白:
①当烧瓶干燥时,从A口进气可收集的气体是_ _ _,从B口进气可收集的气体
是 。
②当烧瓶中充满水时.可用来测量 等气体的体积。
③当烧瓶中装入洗液,用于洗气时,气体应从 口进入烧瓶。
分析与解答:
(1)本题考查学生思维的敏捷性。用排空气法来收集气体要注意气体的密度。由于H2、CH4、NH3的密度比空气小,不与空气发生反应,可用向下排空气的方法来收集,结合本题干燥烧瓶的位置特征,H2、CH4、NH3应从A口进气,把空气从B口赶出。Cl2、HCl、H2S、SO2气体的密度比空气大,与空气不发生反应,应从 B口进气,将空气从A口赶出。NO能与空气中的O2反应,不能用排空气法收集。
(2)对于难溶于水的气体可用排水取气法收集;可以用来收集、测量的气体有H2、CH4、NO。
(3)当烧瓶中装有洗液时,被净化、干燥的气体应从B口进入。
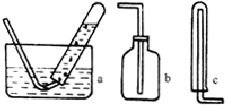
[例3] (1)在没有现成的CO2气体发生器的情况下,请你选用下图中的部分仪器,装配成一个简易的、能随开随用、随关随停的CO2气体发生装置。应选用的仪器是(填入仪器的编号) 。
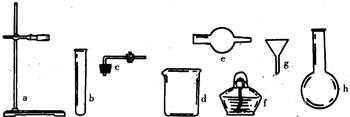
(2)若用上述装置制取CO2气体,而实验室只有稀硫酸、浓硝酸、水、块状纯碱、块状大理石,比较合理的方案应选用的药品是
。
(1992年上海市高考题)
分析与解答:本题要求组装一个随开随用、随关随停的CO2发生装置。即利用启普发生器的原理来制备CO2气体。细心观察所给仪器,可用球形干燥管来代替启普发生器的球形漏斗,烧杯代替反应容器,应选用的仪器是a、c、d、e。
大理石与稀硫酸反应生成了微溶于水的CaSO4,阻碍了反应的进行,因而不能同时选用这两种药品。又因为块状 Na2CO3晶体溶于水,不能用启普发生器来制备 CO2。只能将浓硝酸加水稀释为稀硝酸,再与CaCO3反应制备CO2。应选用的药品是浓硝酸、水、块状大理石。
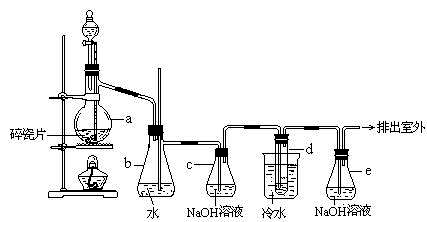
[例4]1,2 - 二溴乙烷可作汽油抗爆剂的添加剂,常温下它是无色液体,密度2.18 g·cm -3,沸点131.4℃,熔点9.79℃,不溶于水,易溶于醇、醚、丙酮等有机溶剂.在实验室中可以用下图所示装置制备1,2- 二溴乙烷.其中分液漏斗和烧瓶a中装有乙醇和浓硫酸的混合液,试管d中装有液溴(表面覆盖少量水)
填写下列空白:
(1)写出本题中制备1,2-二溴乙烷的两个化学反应方程式.
___________________________________________________________
___________________________________________________________
(2)安全瓶b可以防止倒吸,并可以检查实验进行时试管d是否发生堵塞.请
写出发生堵塞时瓶b中的现象._________________________________.
(3)容器c中NaOH溶液的作用是:__________________________________.
(4)某学生在做此实验时,使用一定量的液溴,当溴全部褪色时,所消耗乙醇和浓硫酸混合液的量,比正常情况下超过许多.如果装置的气密性没有问题,试分析其可能的原因.
分析与解答:
本题是是一道综合性的的实验简答题,意在考查学生的观察能力、实验能力和思维能力。解题时依据试题信息,细心观察实验装置图,善于联系已经掌握的基础知识,进行知识的迁移,发散思维,用准确的化学语言来解答实际问题。
本题的正确答案及评分标准为:
(1) 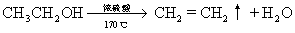
CH2=CH2+Br2→CH2BrCH2Br (每式1分,共2分)
(2)b中水面会下降,玻璃管中的水柱会上升,甚至溢出. (2分)
(3)除去乙烯中带出的酸性气体.或答除去CO2、SO2. (2分)
(4)原因:
①乙烯发生(或通过液溴)速度过快
②实验过程中,乙醇和浓硫酸的混合液没有迅速达到170℃(答"控温不当"亦可)
(两点各2分,共4分.答其它原因不给分也不扣分)
第二篇:高中化学常见气体的制法
常见气体实验室制法
中学化学教材重点介绍了十四种常见气体制备,它们是:①三种单质:O2、H2、Cl2;②三种氢化物:HCl、H2S、NH3;③五种氧化
物:CO2、SO2、NO2、NO、CO;④三种烃:CH4、C2H4、C2H2。
1.常见气体的反应原理、装置和收集
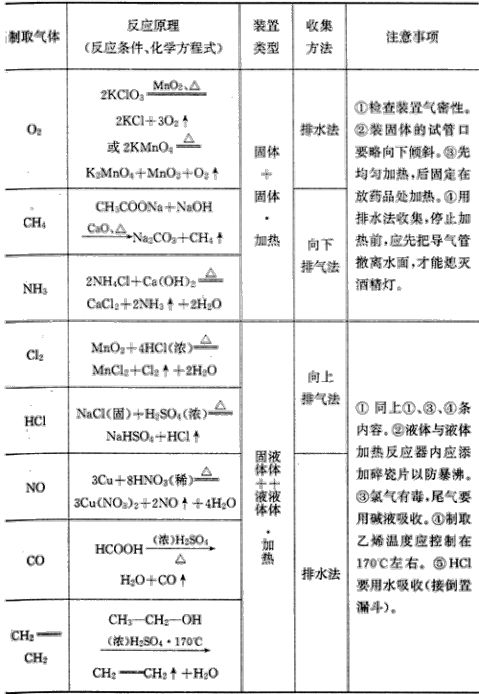
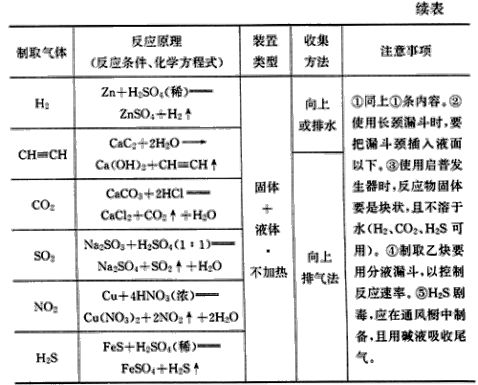
2.常见气体的干燥
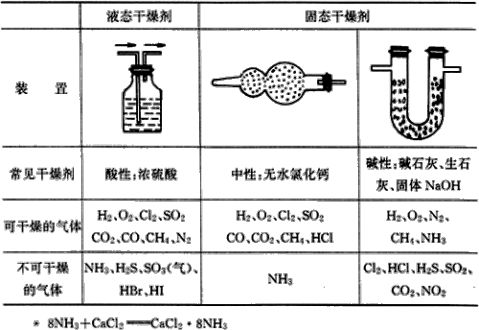
二、气体的发生装置、收集装置和检验
1.气体的发生装置
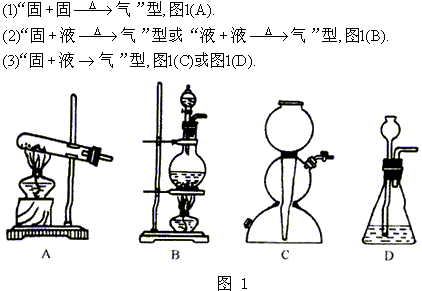
2.气体的收集装置
(1)排水(溶液)集气法,图2(a)。
(2)向上排空气法,图2(b)。
(3)向下排空气法,图2(c)。
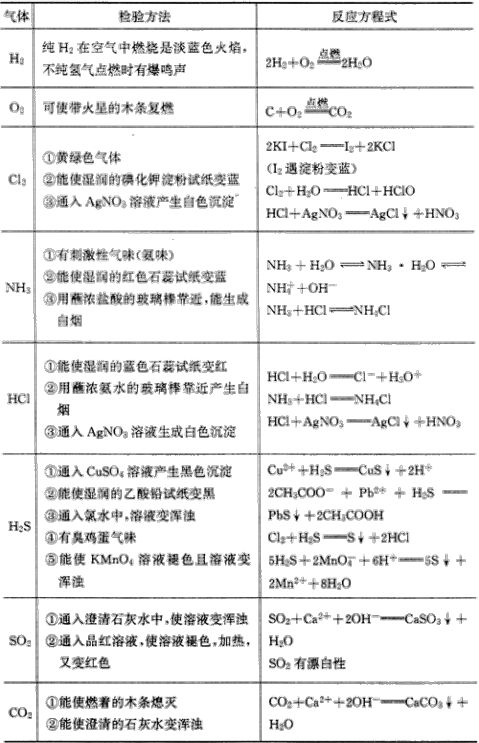
3.常见气体的检验方法